Clear Sky Science · nl
Gemanipuleerde buitenmembraanblaasjes versterken CAR-T-celtherapie tegen solide tumoren
Het immuunsysteem van het lichaam herstarten
Veel van de meest spectaculaire kankergenesen van de afgelopen jaren komen voort uit CAR-T-celtherapie, waarbij de eigen immuuncellen van een patiënt worden herprogrammeerd om kanker te bestrijden. Bij solide tumoren zoals borst- en leverkanker stokt deze aanpak echter vaak: de beschermende omgeving van de tumor en veranderende moleculaire “identiteitslabels” maken het mogelijk dat kwaadaardige cellen zich verbergen of terugvechten. Deze studie introduceert een slimme hulpmethode gebaseerd op kleine blaasje afkomstig van bacteriën die zowel de afweer van de tumor kan openen als duidelijke doelen op tumorcellen kan aanbrengen, zodat CAR-T-cellen ze beter kunnen vinden en vernietigen.
Waarom supercharged T-cellen moeite hebben bij solide tumoren
CAR-T-cellen herkennen kankercellen door zich te hechten aan specifieke markers op hun oppervlak. Bloedkankers tonen die markers meestal consistent, maar solide tumoren zijn ongelijk: sommige cellen dragen het doel, andere niet, en overlevende cellen kunnen simpelweg stoppen met het tonen ervan. Tegelijkertijd worden solide tumoren omgeven door een vijandige omgeving vol cellen en signalen die T-cellen uitschakelen. Een belangrijke rem is een moleculaire handdruk tussen PD-L1 op tumorcellen en PD-1 op T-cellen, die het immuunsysteem instrueert zich terug te trekken. Wanneer CAR-T-cellen beginnen aan te vallen, geven ze ontstekingsmoleculen vrij die paradoxaal genoeg PD-L1-niveaus verder kunnen verhogen, waardoor hun eigen effect nog meer wordt afgezwakt.
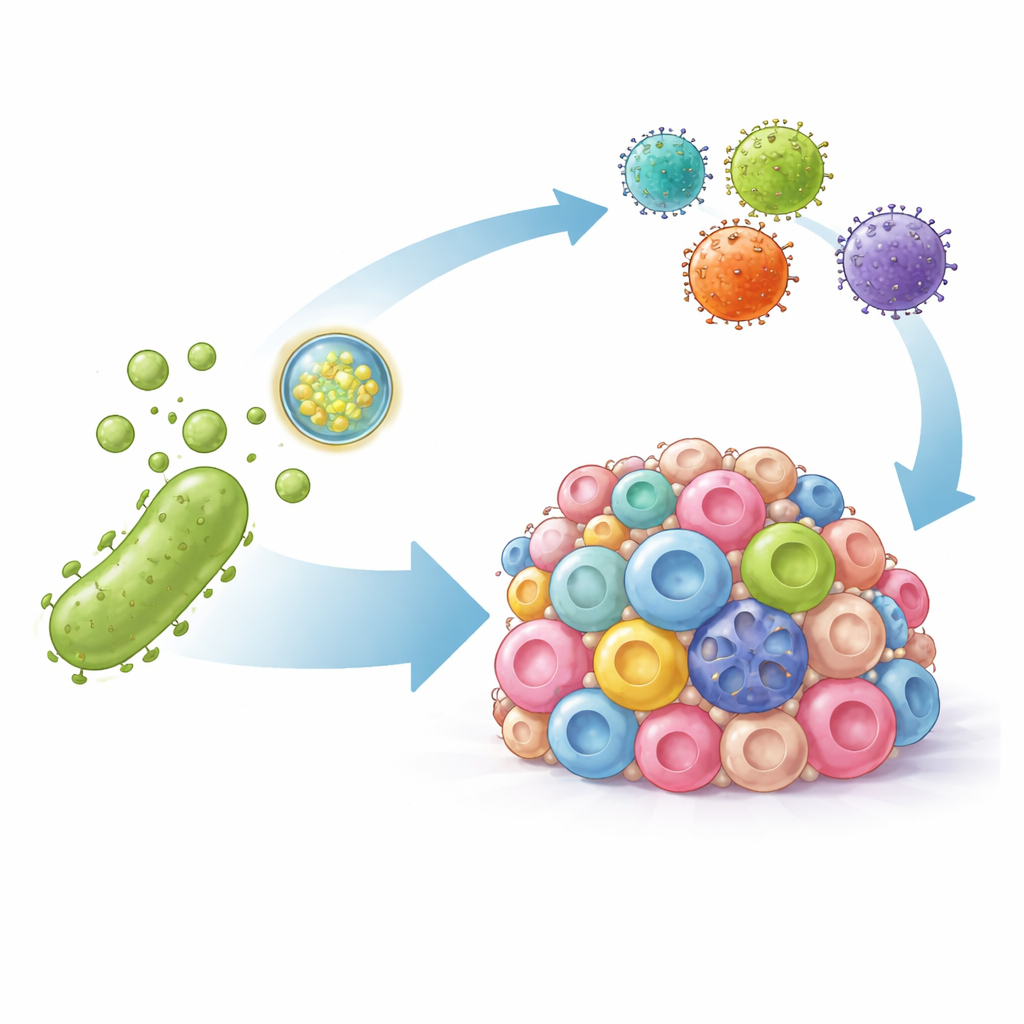
Bacteriële blaasje als precisiekoeriers
De onderzoekers wendden zich tot bacteriële buitenmembraanblaasjes—natuurlijk voorkomende nanoschaalblaasjes die door bacteriën worden afgescheiden en immuunreacties kunnen opwekken. Ze hebben deze blaasje op twee manieren gemodificeerd. Ten eerste versierden ze het oppervlak met een fragment van een antilichaam dat sterk aan PD-L1 bindt, zodat de blaasje naar tumorcellen worden geleid en dit immuunonderdrukkende signaal fysiek blokkeren. Ten tweede vulden ze de blaasje met DNA-instructies die een kunstmatige versie van de HER2-marker coderen, een bekende doelwit voor CAR-T-cellen. Zodra dit DNA in tumorcellen wordt afgeleverd, zorgt het ervoor dat de cellen tijdelijk HER2 op hun oppervlak tonen, en zo zelfs eerder onzichtbare kankercellen markeren voor aanval.
De tumorumgeving herschrijven
In muismodellen van borstkanker stapelden de gemodificeerde blaasje zich efficiënt op in de tumoren en herschikten ze het lokale immuunsysteem. Tumoren die met deze blaasje werden behandeld, vertoonden minder onderdrukkende celtypen, zoals regulerende T-cellen, bepaalde macrofagen en myeloïde-afgeleide onderdrukkende cellen, en meer agressieve verdedigers zoals cytotoxische T-cellen en natural killer-cellen. Deze T-cellen produceerden meer perforine en granzyme—moleculen die gaten in kankercellen slaan—en meer ontstekingsboodschappers zoals interferon-gamma en tumor necrosefactor. Door PD-L1 te blokkeren en tegelijkertijd de aangeboren immuniteit te activeren, veranderden de blaasje een koude, beschermende tumorumgeving in één die een immuunaanslag verwelkomt en ondersteunt.
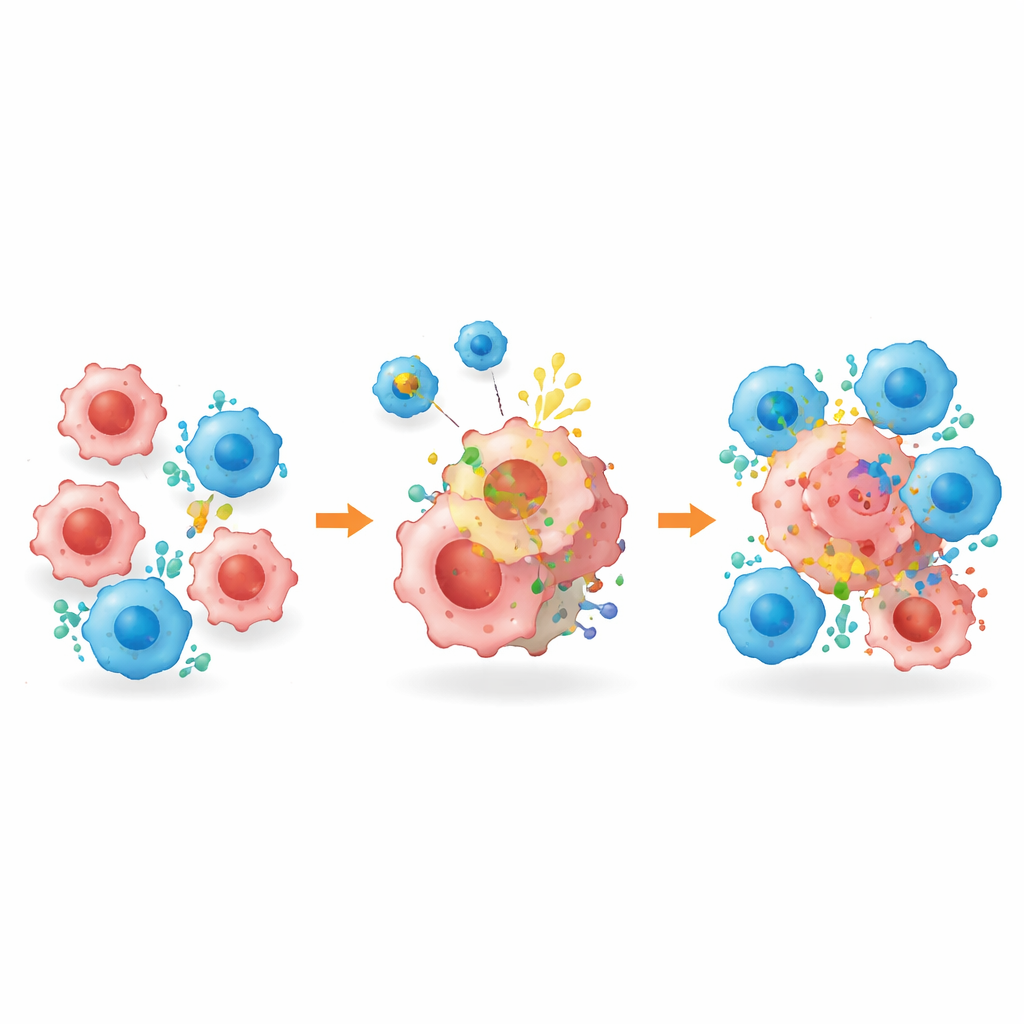
Verborgen tumorcellen markeren voor eliminatie
Buiten het herschikken van de tumorumgeving pakte het platform—BROAD-CAR genoemd—direct het probleem van ontbrekende doelen aan. In gemengde tumoren met zowel HER2-positieve als HER2-negatieve cellen kromp conventionele HER2-gerichte CAR-T-therapie aanvankelijk de tumoren, maar liet cellen achter die het doel hadden verloren, wat leidde tot opnieuw aangroei. In combinatie met BROAD-CAR werden tumoren echter vrijwel uitgeroeid: de blaasje zorgden ervoor dat HER2 verscheen op voorheen negatieve cellen, waardoor CAR-T-cellen ze konden herkennen en doden. Dezelfde strategie werkte bij levertumoren die oorspronkelijk geen HER2 hadden. Belangrijk is dat gedetailleerde analyses lieten zien dat HER2-versiering beperkt bleef tot tumormateriaal, zonder detecteerbare expressie in gezonde organen of immuuncellen, en dat de behandeling geen duidelijke orgaanschade of gewichtsverlies bij muizen veroorzaakte.
Langdurige bescherming tegen terugkeer en uitzaaiing
De voordelen reikten verder dan de initiële tumor. In borstkankermodellen verkleinde de gecombineerde BROAD-CAR- en CAR-T-behandeling niet alleen de primaire tumoren, maar verminderde ze ook scherp het aantal longmetastasen. Muizen die volledig genezen waren, waren bestand tegen een latere herkansing met kankercellen, ongeacht of die cellen HER2 uitdrukten, wat suggereert dat de intense initiële strijd een bredere, langdurige immuunherinnering tegen de tumor opwekte. Dit wijst erop dat het platform mogelijk niet alleen een enkel toegepast T-celproduct kan versterken, maar ook het bredere immuunsysteem kan helpen de kanker vollediger te leren herkennen.
Wat dit kan betekenen voor toekomstige kankerzorg
Samenvattend toont de studie aan dat bacteriële blaasje kunnen worden omgevormd tot veilige, aanpasbare helpers die CAR-T-therapie veel effectiever maken tegen hardnekkige solide tumoren. Door zowel de immuunremmen op te heffen als duidelijke, tijdelijke doelen op tumorcellen te schilderen, stelde het BROAD-CAR-systeem gemodificeerde T-cellen in staat diverse en zelfs doelwitloze kankers bij muizen te ruimen, terwijl gezonde weefsels werden gespaard. Als vergelijkbare resultaten bij mensen blijken te gelden, zou deze aanpak CAR-T-behandelingen kunnen uitbreiden naar veel meer patiënten met solide tumoren en terugvallen door verlies van antigenen minder waarschijnlijk maken, en daarmee een krachtige nieuwe manier bieden om het immuunsysteem te helpen voltooien wat het is begonnen.
Bronvermelding: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Trefwoorden: CAR-T-celtherapie, solide tumoren, tumormicro-omgeving, bacteriële buitenmembraanblaasjes, kankerimmunotherapie