Clear Sky Science · pl
Zmodyfikowane pęcherzyki zewnętrznej błony poprawiają terapię CAR‑T przeciw nowotworom litym
Przeładowanie naturalnych wojowników organizmu przeciw nowotworom
Wiele z najbardziej spektakularnych remisji nowotworowych w ostatnich latach zawdzięczamy terapii CAR‑T, w której własne komórki odpornościowe pacjenta są przeprogramowywane do tropienia raka. Jednak w przypadku nowotworów litych, takich jak rak piersi czy wątroby, podejście to często napotyka przeszkody: ochronne otoczenie guza i zmienne molekularne „identyfikatory” pozwalają komórkom nowotworowym ukrywać się lub odpierać atak. W tym badaniu przedstawiono sprytny system pomocniczy oparty na drobnych pęcherzykach pochodzenia bakteryjnego, który jednocześnie otwiera obronę guza i namalowuje czytelne cele na komórkach nowotworowych, dzięki czemu komórki CAR‑T mogą je skuteczniej odnaleźć i zniszczyć.
Dlaczego superdoładowane komórki T zawodzą w guzach litych
Komórki CAR‑T rozpoznają komórki nowotworowe, przyczepiając się do określonych markerów na ich powierzchni. W nowotworach krwi te markery zwykle występują stabilnie, ale guzy lite są niejednorodne: niektóre komórki mają cel, inne go nie mają, a komórki przetrwałe mogą po prostu przestać go wykazywać. Równocześnie guzy lite otoczone są wrogim środowiskiem pełnym komórek i sygnałów, które hamują komórki T. Jednym z kluczowych hamulców jest molekularne uściski dłoni między PD‑L1 na komórkach guza a PD‑1 na komórkach T, które nakazują układowi odpornościowemu wstrzymanie działania. Gdy komórki CAR‑T zaczynają atakować, uwalniają zapalne czynniki, które paradoksalnie mogą jeszcze zwiększać poziom PD‑L1, dodatkowo osłabiając ich własny efekt.
Przekształcanie bakteryjnych pęcherzyków w precyzyjne kurierzy
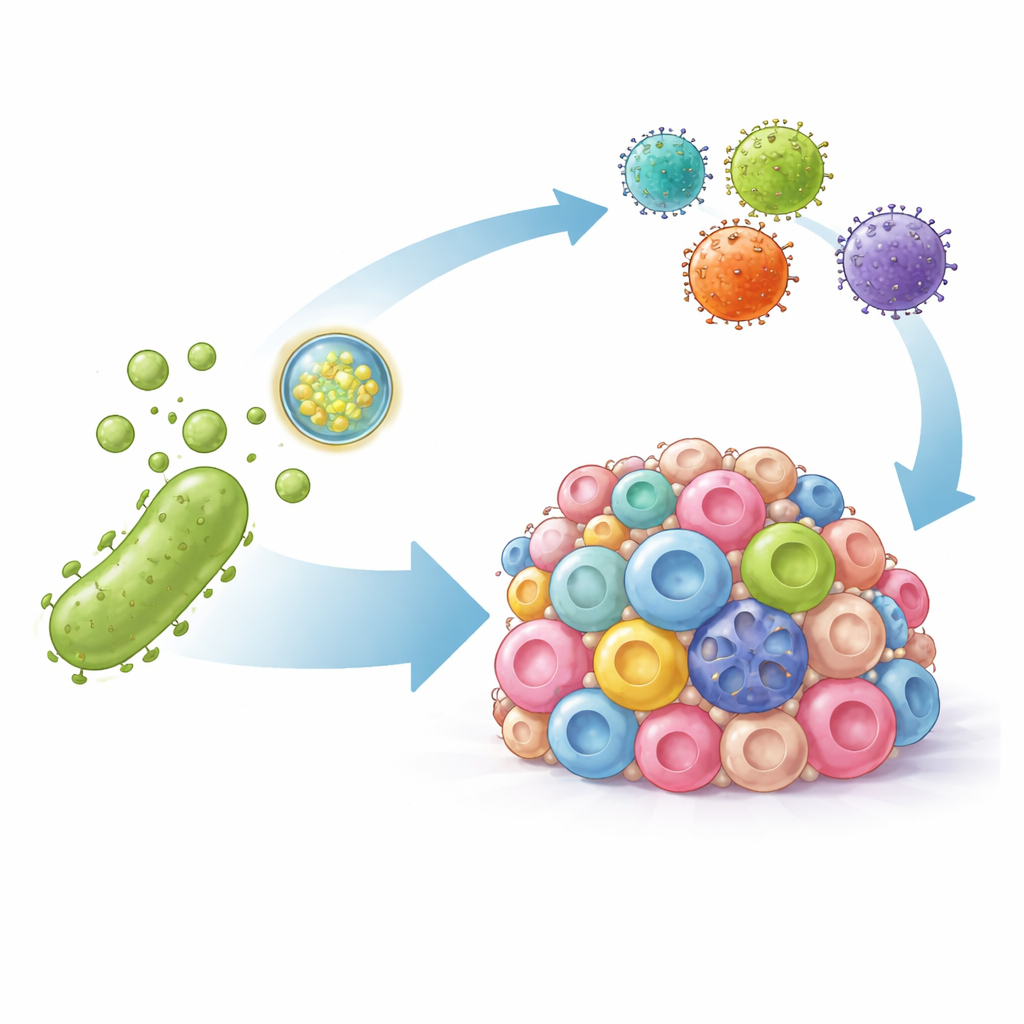
Naukowcy sięgnęli po zewnętrzne pęcherzyki błony bakteryjnej — naturalnie występujące nanoskali pęcherzyki uwalniane przez bakterie, które potrafią pobudzać odpowiedź odpornościową. Zmodyfikowali te pęcherzyki na dwa sposoby. Po pierwsze, ozdobili ich powierzchnię fragmentem przeciwciała mocno wiążącego PD‑L1, dzięki czemu pęcherzyki celują w komórki guza i fizycznie blokują ten immunosupresyjny sygnał. Po drugie, spakowali do pęcherzyków instrukcje DNA kodujące sztuczną wersję markera HER2, dobrze znanego celu dla komórek CAR‑T. Po dostarczeniu do komórek guza to DNA sprawia, że komórki tymczasowo eksponują HER2 na swojej powierzchni, efektywnie znakując nawet wcześniej niewidoczne komórki nowotworowe do ataku.
Przepisanie sąsiedztwa guza
W modelach mysich raka piersi zmodyfikowane pęcherzyki kumulowały się efektywnie w guzach i przekształcały lokalny krajobraz odpornościowy. Guzy leczone tymi pęcherzykami wykazywały mniej typów komórek supresyjnych, takich jak limfocyty regulatorowe, niektóre makrofagi czy mieloidalne komórki supresorowe, a więcej agresywnych obrońców, takich jak cytotoksyczne limfocyty T i komórki NK. Te komórki T produkowały więcej perforyny i granzymy — cząsteczek tworzących dziury w komórkach nowotworowych — oraz więcej zapalnych mediatorów, takich jak interferon‑gamma i czynnik martwicy nowotworu. Blokując PD‑L1 i jednocześnie aktywując odporność wrodzoną, pęcherzyki zamieniły zimne, ochronne mikrośrodowisko guza w takie, które sprzyja i podtrzymuje atak immunologiczny.
Oznaczanie ukrytych komórek guza do eliminacji
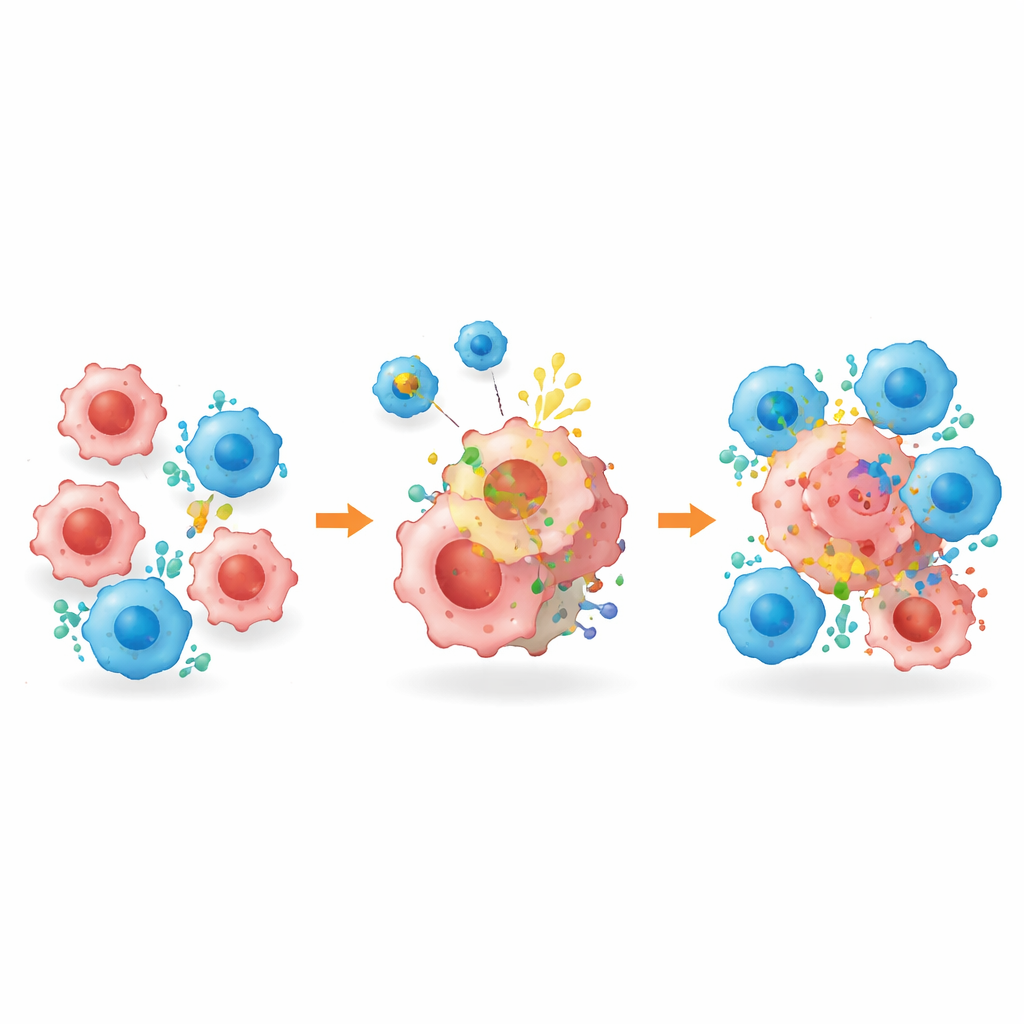
Poza przebudową otoczenia guza, platforma nazwana BROAD‑CAR bezpośrednio rozwiązała problem brakujących celów. W mieszanych guzach zawierających komórki HER2‑dodatnie i HER2‑ujemne konwencjonalna terapia CAR‑T ukierunkowana na HER2 początkowo zmniejszała guzy, ale pozostawiała komórki, które utraciły cel, prowadząc do odrostu. W połączeniu z BROAD‑CAR jednak guzy zostały niemal całkowicie zniszczone: pęcherzyki spowodowały pojawienie się HER2 na wcześniej ujemnych komórkach, co umożliwiło komórkom CAR‑T ich rozpoznanie i zabicie. Ta sama strategia zadziałała w guzach wątroby, które początkowo nie miały HER2. Co ważne, szczegółowe analizy wykazały, że dekoracja HER2 ograniczała się do tkanki guza, bez wykrywalnej ekspresji w zdrowych narządach czy komórkach odpornościowych, a leczenie nie powodowało widocznego uszkodzenia narządów ani utraty masy ciała u myszy.
Trwała ochrona przed nawrotem i przerzutami
Korzyści wykraczały poza początkowy guz. W modelach raka piersi skojarzone leczenie BROAD‑CAR z CAR‑T nie tylko zmniejszyło guzy pierwotne, lecz także zdecydowanie ograniczyło przerzuty do płuc. Myszy, które zostały całkowicie wyleczone, były odporne na późniejsze ponowne podanie komórek nowotworowych, niezależnie od tego, czy te komórki eksponowały HER2, co sugeruje, że intensywna początkowa konfrontacja wywołała szerszą, długotrwałą pamięć odpornościową przeciw guzowi. Wskazuje to, że platforma może nie tylko wzmocnić pojedynczy produkt komórek inżynieryjnych, lecz także pomóc całemu systemowi odpornościowemu w pełniejszym rozpoznawaniu nowotworu.
Co to może znaczyć dla przyszłej opieki onkologicznej
Podsumowując, badanie pokazuje, że pęcherzyki bakteryjne można przekształcić w bezpiecznych, adaptowalnych pomocników, którzy znacznie poprawiają skuteczność terapii CAR‑T przeciw uporczywym nowotworom litym. Poprzez zarówno znoszenie hamulców immunologicznych, jak i tymczasowe malowanie wyraźnych celów na komórkach guza, system BROAD‑CAR pozwolił zainżynieryzowanym komórkom T oczyścić różnorodne, a nawet pozbawione naturalnych antygenów nowotwory u myszy, unikając przy tym uszkodzeń tkanek zdrowych. Jeśli podobne wyniki potwierdzą się u ludzi, podejście to mogłoby rozszerzyć terapię CAR‑T na znacznie większą liczbę pacjentów z nowotworami litymi i zmniejszyć ryzyko nawrotów związanych z utratą antygenu, oferując potężne nowe narzędzie do wspierania układu odpornościowego w dokończeniu tego, co zaczął.
Cytowanie: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Słowa kluczowe: terapia komórkami CAR‑T, nowotwory lite, mikrośrodowisko guza, zewnętrzne pęcherzyki błony bakteryjnej, immunoterapia nowotworów