Clear Sky Science · de
Gentechnisch veränderte äußere Membranvesikel verbessern CAR‑T‑Zelltherapie gegen solide Tumore
Die körpereigenen Krebsbekämpfer neu starten
Viele der spektakulärsten Krebsremissionen der letzten Jahre stammen von CAR‑T‑Zelltherapien, bei denen die Immunzellen eines Patienten umprogrammiert werden, um Krebszellen zu jagen. Bei soliden Tumoren wie Brust‑ und Leberkrebs scheitert dieser Ansatz jedoch häufig: die schützende Umgebung des Tumors und wechselnde molekulare „Ausweis‑marker“ ermöglichen es malignen Zellen, sich zu verstecken oder Gegenwehr zu leisten. Diese Studie stellt ein pfiffiges Unterstützungssystem vor, das auf winzigen Bläschen aus Bakterien basiert und sowohl die Verteidigung des Tumors öffnet als auch klare Ziele auf Tumorzellen anbringt, sodass CAR‑T‑Zellen sie effektiver finden und zerstören können.
Warum aufgerüstete T‑Zellen bei soliden Tumoren trotzdem scheitern
CAR‑T‑Zellen erkennen Krebszellen, indem sie an bestimmte Marker auf deren Oberfläche andocken. Hämatologische Krebserkrankungen zeigen diese Marker meist gleichmäßig, während solide Tumoren heterogen sind: Einige Zellen tragen das Ziel, andere nicht, und überlebende Zellen können die Darstellung einfach einstellen. Zugleich ist der Tumor von einer feindseligen Umgebung umgeben, voller Zellen und Signale, die T‑Zellen ausschalten. Ein zentraler Bremspunkt ist die molekulare Wechselwirkung zwischen PD‑L1 auf Tumorzellen und PD‑1 auf T‑Zellen, die dem Immunsystem signalisiert, sich zurückzuhalten. Wenn CAR‑T‑Zellen beginnen anzugreifen, setzen sie entzündliche Moleküle frei, die paradoxerweise die PD‑L1‑Spiegel noch weiter erhöhen können und so ihre eigene Wirkung abschwächen.
Bakterielle Bläschen als präzise Überbringer
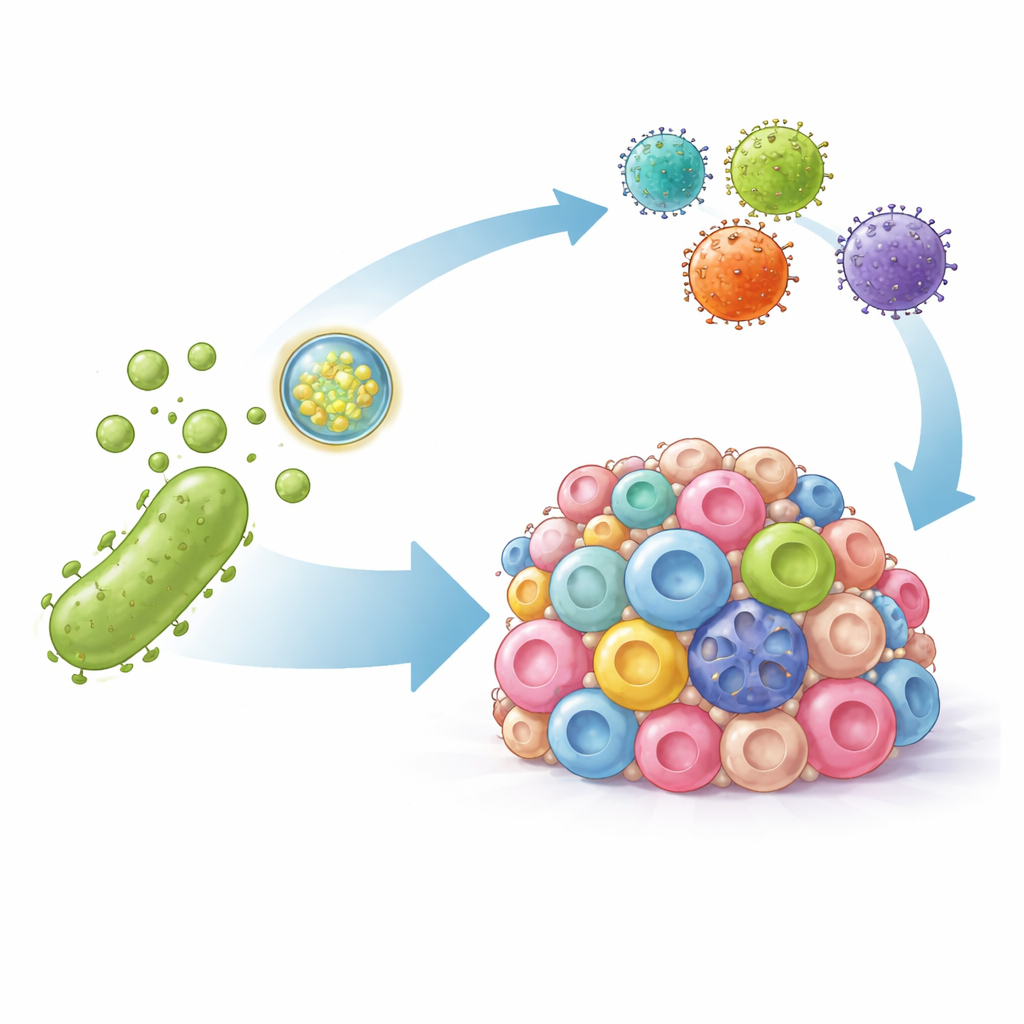
Die Forschenden nutzten bakterielle äußere Membranvesikel—natürlich vorkommende nanoskalige Bläschen, die Bakterien abgeben und Immunreaktionen anheizen können. Sie modifizierten diese Vesikel auf zwei Arten. Erstens schmückten sie die Oberfläche mit einem Antikörperfragment, das stark an PD‑L1 bindet, sodass die Vesikel Tumorzellen ansteuern und dieses immununterdrückende Signal physisch blockieren. Zweitens luden sie die Vesikel mit DNA‑Instruktionen, die eine künstliche Version des HER2‑Markers codieren, einem bekannten Ziel für CAR‑T‑Zellen. Nach der Abgabe in Tumorzellen lässt diese DNA die Zellen vorübergehend HER2 auf ihrer Oberfläche präsentieren und markiert so auch zuvor unsichtbare Krebszellen für den Angriff.
Die Tumorumgebung umschreiben
In Mausmodellen des Brustkrebses reichten sich die modifizierten Vesikel effizient in Tumoren an und veränderten die lokale Immunlandschaft. Tumoren, die mit diesen Vesikeln behandelt wurden, zeigten weniger unterdrückende Zelltypen wie regulatorische T‑Zellen, bestimmte Makrophagen und myeloide‑abgeleitete Suppressorzellen, und mehr aggressive Verteidiger wie zytotoxische T‑Zellen und natürliche Killerzellen. Diese T‑Zellen produzierten mehr Perforin und Granzyme—Moleküle, die Löcher in Krebszellen reißen—und mehr entzündliche Botenstoffe wie Interferon‑gamma und Tumornekrosefaktor. Durch das Blockieren von PD‑L1 und gleichzeitig die Aktivierung der angeborenen Immunität verwandelten die Vesikel eine kalte, schützende Tumorumgebung in eine, die einen Immunangriff begrüßt und aufrechterhält.
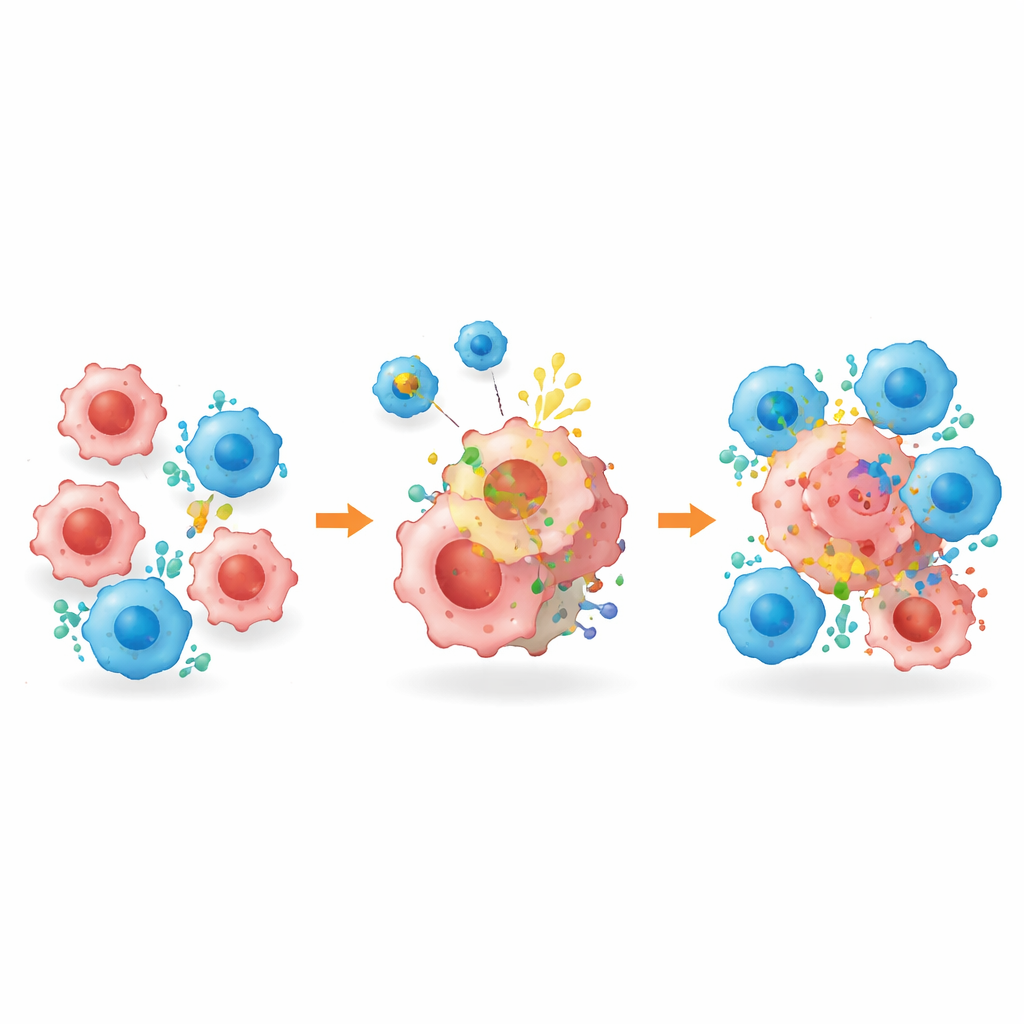
Verborgene Tumorzellen zur Eliminierung markieren
Neben der Umgestaltung des Tumormilieus ging die Plattform—BROAD‑CAR genannt—direkt das Problem fehlender Zielantigene an. In gemischten Tumoren mit sowohl HER2‑positiven als auch HER2‑negativen Zellen schrumpfte die konventionelle HER2‑gerichtete CAR‑T‑Therapie zunächst die Tumoren, ließ jedoch Zellen zurück, die das Ziel verloren hatten, was zu einem Wiederwachstum führte. In Kombination mit BROAD‑CAR wurden die Tumoren jedoch nahezu ausgelöscht: Die Vesikel sorgten dafür, dass HER2 auch auf zuvor negativen Zellen erschien, sodass CAR‑T‑Zellen sie erkennen und töten konnten. Die gleiche Strategie funktionierte in Lebertumoren, die ursprünglich gar kein HER2 aufwiesen. Wichtig ist, dass detaillierte Analysen zeigten, dass die HER2‑Dekoration auf das Tumorgewebe beschränkt blieb—ohne nachweisbare Expression in gesunden Organen oder Immunzellen—und die Behandlung keine offensichtlichen Organschäden oder Gewichtsverluste bei den Mäusen verursachte.
Lang anhaltender Schutz gegen Rückkehr und Ausbreitung
Der Nutzen ging über den anfänglichen Tumor hinaus. In Brustkrebsmodellen führte die kombinierte BROAD‑CAR‑ und CAR‑T‑Behandlung nicht nur zur Schrumpfung der Primärtumoren, sondern reduzierte auch Lungenmetastasen deutlich. Mäuse, die vollständig geheilt waren, widerstanden späteren erneuten Tumorherausforderungen—unabhängig davon, ob die Zellen HER2 exprimierten—was darauf hindeutet, dass die intensive Erstreaktion eine breitere, langlebige immunologische Erinnerung gegen den Tumor auslöste. Das legt nahe, dass die Plattform nicht nur ein einzelnes gentechnisch verändertes T‑Zellprodukt verbessert, sondern auch dem gesamten Immunsystem helfen könnte, den Krebs umfassender zu erkennen.
Was das für die künftige Krebsbehandlung bedeuten könnte
Insgesamt zeigt die Studie, dass bakterielle Vesikel in sichere, anpassbare Helfer verwandelt werden können, die CAR‑T‑Therapien gegen hartnäckige solide Tumoren deutlich wirksamer machen. Indem sie sowohl Immunbremsen lösen als auch klare, vorübergehende Ziele auf Tumorzellen anbringen, ermöglicht das BROAD‑CAR‑System den gentechnisch veränderten T‑Zellen, vielfältige und sogar ziellose Krebserkrankungen bei Mäusen zu beseitigen, ohne gesunde Gewebe anzugreifen. Wenn sich ähnliche Ergebnisse beim Menschen bestätigen, könnte dieser Ansatz die CAR‑T‑Behandlung auf viele mehr Patienten mit soliden Tumoren ausdehnen und Rückfälle durch Antigenverlust weniger wahrscheinlich machen—ein vielversprechender neuer Weg, um das Immunsystem das beenden zu lassen, was es begonnen hat.
Zitation: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Schlüsselwörter: CAR‑T‑Zelltherapie, solide Tumoren, Tumormikroumgebung, bakterielle äußere Membranvesikel, Krebsimmuntherapie