Clear Sky Science · fr
Des vésicules membranaires externes conçues améliorent la thérapie CAR-T contre les tumeurs solides
Relancer les soldats immunitaires de l’organisme
Beaucoup des rémissions cancéreuses les plus spectaculaires de ces dernières années proviennent de la thérapie CAR-T, où les propres cellules immunitaires d’un patient sont reprogrammées pour traquer le cancer. Pourtant, pour les tumeurs solides comme celles du sein ou du foie, cette approche échoue souvent : l’environnement protecteur de la tumeur et les « étiquettes d’identité » moléculaires changeantes permettent aux cellules malignes de se cacher ou de riposter. Cette étude présente un système auxiliaire astucieux basé sur de petites bulles provenant de bactéries qui peuvent à la fois ouvrir les défenses tumorales et peindre des cibles nettes sur les cellules tumorales, afin que les CAR-T les repèrent et les détruisent plus efficacement.
Pourquoi les cellules T surpuissantes peinent dans les tumeurs solides
Les cellules CAR-T reconnaissent les cellules cancéreuses en se fixant sur des marqueurs spécifiques à leur surface. Les cancers du sang présentent généralement ces marqueurs de façon homogène, mais les tumeurs solides sont hétérogènes : certaines cellules portent la cible, d’autres non, et les cellules survivantes peuvent simplement cesser de l’exprimer. Parallèlement, les tumeurs solides sont entourées d’un milieu hostile rempli de cellules et de signaux qui inhibent les cellules T. Un frein clé est la poignée de main moléculaire entre PD-L1 sur les cellules tumorales et PD-1 sur les cellules T, qui intime au système immunitaire de se calmer. Lorsque les CAR-T attaquent, ils libèrent des molécules inflammatoires qui, paradoxalement, peuvent augmenter encore le niveau de PD-L1, affaiblissant davantage leur propre efficacité.
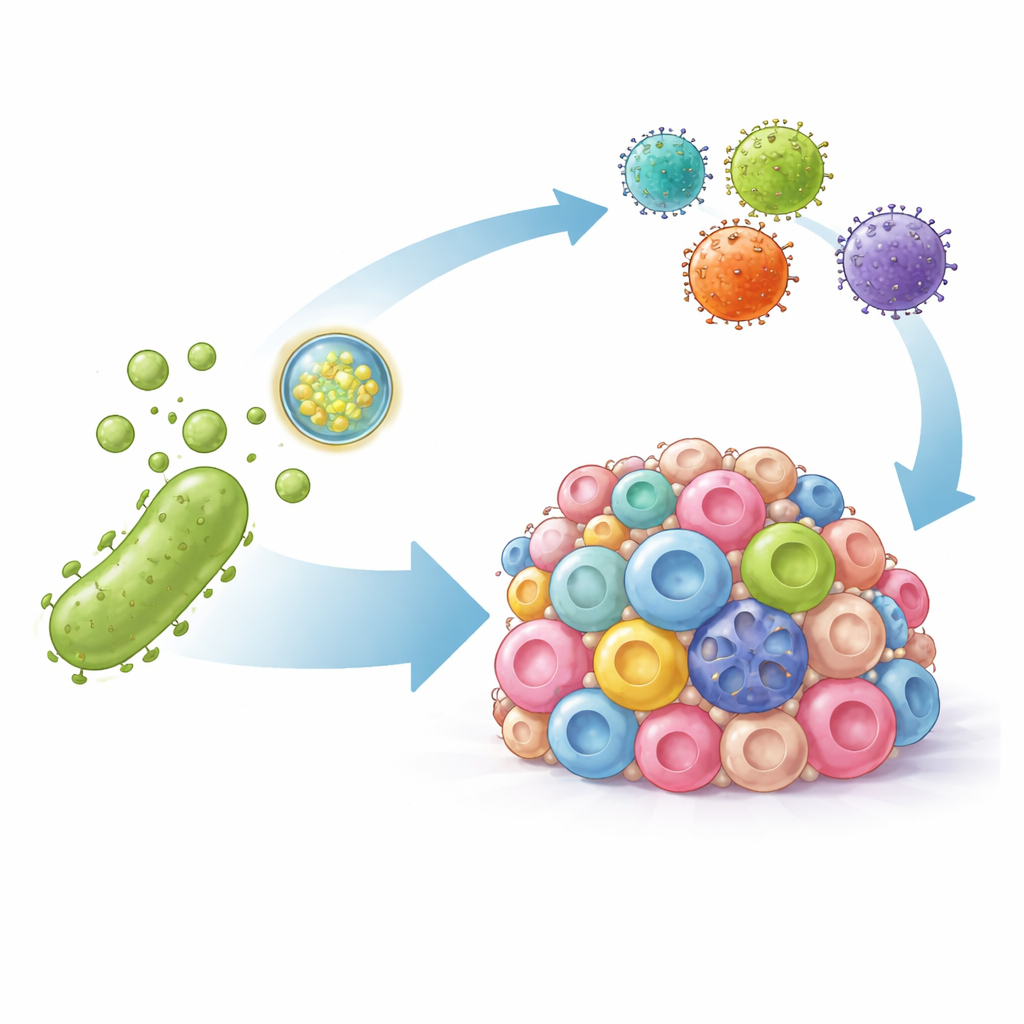
Transformer des bulles bactériennes en coursiers de précision
Les chercheurs se sont tournés vers les vésicules de membrane externe bactérienne — de petites bulles nanoscale naturelles émises par les bactéries qui peuvent stimuler des réponses immunitaires. Ils ont ingénieusement modifié ces vésicules de deux manières. D’abord, ils ont décoré leur surface avec un fragment d’anticorps qui se fixe fortement à PD-L1, de sorte que les vésicules ciblent les cellules tumorales et bloquent physiquement ce signal d’inhibition immunitaire. Ensuite, ils ont chargé les vésicules avec des instructions d’ADN codant une version artificielle du marqueur HER2, une cible bien connue des CAR-T. Une fois délivré dans les cellules tumorales, cet ADN fait en sorte que les cellules expriment temporairement HER2 à leur surface, marquant ainsi même les cellules auparavant invisibles pour l’attaque.
Réécrire le voisinage tumoral
Chez des modèles murins de cancer du sein, les vésicules modifiées se sont accumulées efficacement dans les tumeurs et ont remodelé le paysage immunitaire local. Les tumeurs traitées avec ces vésicules montraient moins de types cellulaires suppressifs, tels que les lymphocytes T régulateurs, certains macrophages et cellules myéloïdes suppressives, et plus de défenseurs agressifs comme les lymphocytes T cytotoxiques et les cellules NK. Ces cellules T produisaient davantage de perforine et de granzyme — molécules qui perforent les cellules cancéreuses — et plus de médiateurs inflammatoires tels que l’interféron-gamma et le facteur de nécrose tumorale. En bloquant PD-L1 tout en activant l’immunité innée, les vésicules ont transformé un microenvironnement tumoral froid et protecteur en un milieu favorable et soutenant une attaque immunitaire.
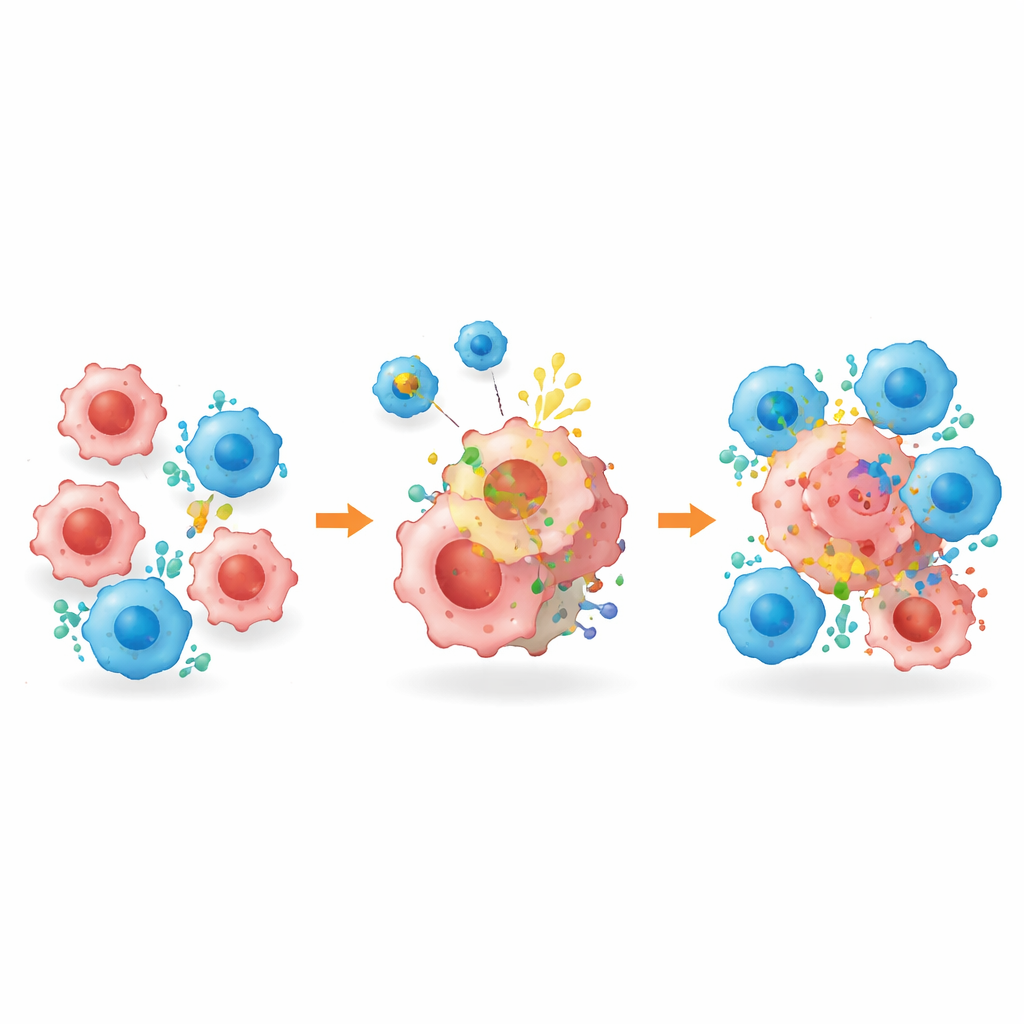
Marquer les cellules tumorales cachées pour les éliminer
Au-delà du remodelage de l’environnement tumoral, la plateforme — nommée BROAD-CAR — a abordé directement le problème des cibles manquantes. Dans des tumeurs mixtes contenant à la fois des cellules HER2-positives et HER2-négatives, la thérapie CAR-T conventionnelle dirigée contre HER2 réduisait initialement les tumeurs mais laissait des cellules ayant perdu la cible, entraînant une repousse. Lorsqu’elle était combinée au système BROAD-CAR, toutefois, les tumeurs ont été presque anéanties : les vésicules ont induit l’apparition de HER2 sur des cellules auparavant négatives, permettant aux CAR-T de les reconnaître et de les tuer. La même stratégie a fonctionné pour des tumeurs du foie dépourvues de HER2 au départ. De manière importante, des analyses détaillées ont montré que la décoration en HER2 restait confinée au tissu tumoral, sans expression détectable dans les organes sains ou les cellules immunitaires, et le traitement n’a causé aucun dommage organique évident ni perte de poids chez les souris.
Protection durable contre récidive et dissémination
Les bénéfices dépassaient la tumeur initiale. Dans des modèles de cancer du sein, la combinaison BROAD-CAR et CAR-T non seulement réduisait la tumeur primaire mais diminuait fortement les métastases pulmonaires. Les souris totalement guéries résistaient à une réinoculation ultérieure de cellules cancéreuses, qu’elles expriment ou non HER2, ce qui suggère que l’intense bataille initiale a déclenché une mémoire immunitaire plus large et durable contre la tumeur. Cela laisse entendre que la plateforme pourrait non seulement renforcer un produit unique de cellules T modifiées, mais aussi aider le système immunitaire global à mieux reconnaître le cancer de façon plus complète.
Ce que cela pourrait signifier pour les soins du cancer à l’avenir
Dans l’ensemble, l’étude montre que les vésicules bactériennes peuvent être transformées en auxiliaires sûrs et adaptables qui rendent la thérapie CAR-T bien plus efficace contre les tumeurs solides récalcitrantes. En levant les freins immunitaires et en peignant des cibles claires et temporaires sur les cellules tumorales, le système BROAD-CAR a permis aux cellules T modifiées d’éliminer des cancers divers et même dépourvus de cibles chez la souris, tout en épargnant les tissus sains. Si des résultats similaires se confirment chez l’humain, cette approche pourrait étendre la thérapie CAR-T à beaucoup plus de patients atteints de tumeurs solides et rendre les rechutes dues à la perte d’antigène moins probables, offrant un nouveau moyen puissant d’aider le système immunitaire à achever ce qu’il commence.
Citation: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Mots-clés: thérapie par cellules CAR-T, tumeurs solides, microenvironnement tumoral, vésicules de membrane externe bactérienne, immunothérapie du cancer