Clear Sky Science · pt
Vesículas de membrana externa projetadas aumentam a terapia CAR-T para tumores sólidos
Reiniciando os combatentes do corpo contra o câncer
Muitas das remissões de câncer mais dramáticas nos últimos anos vieram da terapia CAR-T, na qual as próprias células imunes do paciente são reprogramadas para caçar o câncer. Ainda assim, em tumores sólidos como os de mama e fígado, essa abordagem frequentemente emperra: o bairro protetor do tumor e as “etiquetas de identificação” moleculares em mudança permitem que as células malignas se escondam ou revidem. Este estudo introduz um sistema auxiliar engenhoso baseado em pequenas bolhas de origem bacteriana que podem tanto abrir as defesas do tumor quanto pintar alvos claros nas células tumorais, para que as células CAR-T possam encontrá-las e destruí-las com mais eficácia.
Por que células T supercarregadas têm dificuldade em tumores sólidos
Células CAR-T reconhecem células cancerosas ao se ligarem a marcadores específicos na sua superfície. Cânceres do sangue normalmente exibem esses marcadores de forma consistente, mas tumores sólidos são heterogêneos: algumas células apresentam o alvo, outras não, e células sobreviventes podem simplesmente deixar de mostrá-lo. Ao mesmo tempo, tumores sólidos estão cercados por um ambiente hostil repleto de células e sinais que desligam as células T. Um freio importante é o aperto molecular entre PD-L1 nas células tumorais e PD-1 nas células T, que manda o sistema imune recuar. Quando as células CAR-T começam a atacar, elas liberam moléculas inflamatórias que, paradoxalmente, podem elevar ainda mais os níveis de PD-L1, diminuindo ainda mais seu próprio impacto.
Transformando bolhas bacterianas em mensageiros de precisão
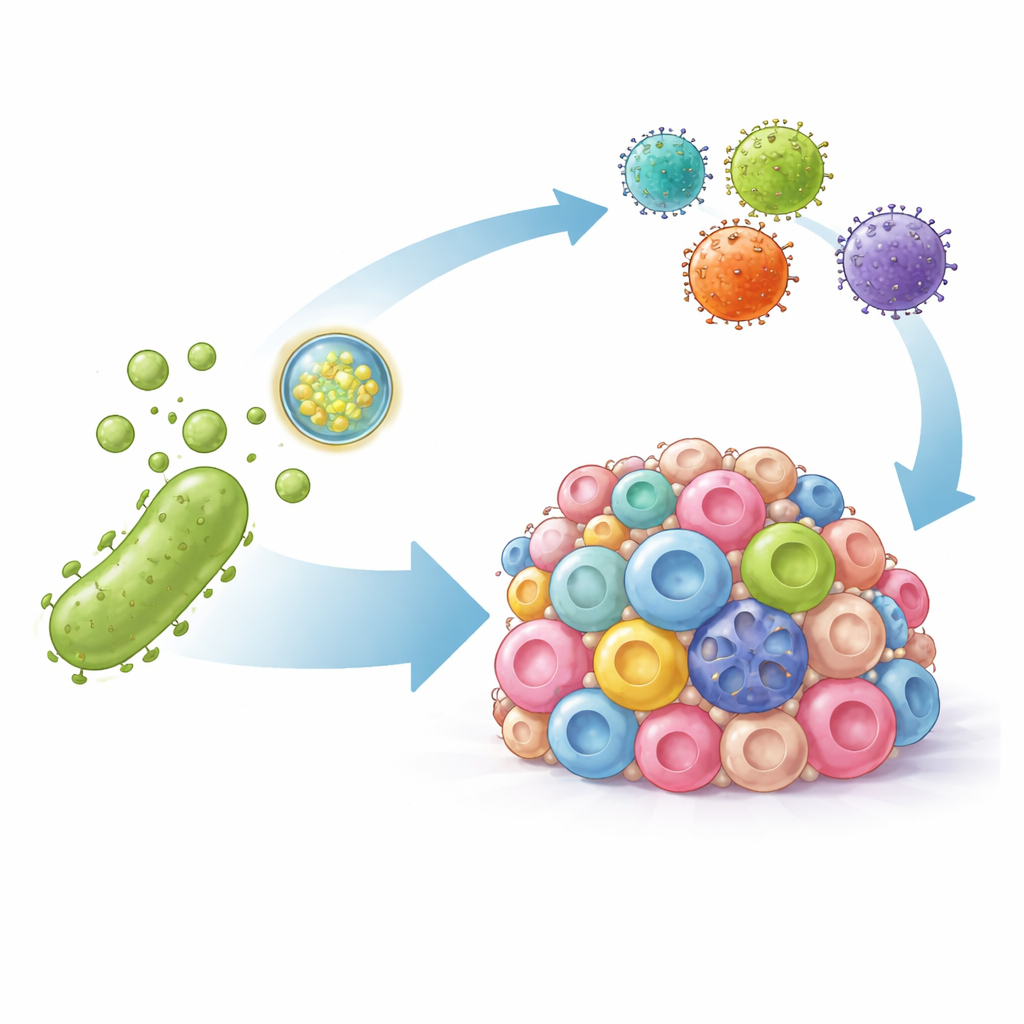
Os pesquisadores recorreram às vesículas de membrana externa bacterianas—bolhas em escala nanométrica produzidas naturalmente por bactérias que podem estimular respostas imunes. Eles modificaram essas vesículas de duas maneiras. Primeiro, decoraram sua superfície com um fragmento de anticorpo que se liga fortemente ao PD-L1, de modo que as vesículas se direcionam às células tumorais e bloqueiam fisicamente esse sinal que suprime a imunidade. Segundo, embalaram as vesículas com instruções de DNA que codificam uma versão artificial do marcador HER2, um alvo bem conhecido para células CAR-T. Uma vez entregues às células tumorais, esse DNA faz com que as células exibam temporariamente HER2 na superfície, marcando efetivamente mesmo as células cancerosas antes invisíveis para o ataque.
Reescrevendo o bairro tumoral
Em modelos de camundongos com câncer de mama, as vesículas modificadas se acumularam de forma eficiente nos tumores e remodelaram a paisagem imune local. Tumores tratados com essas vesículas apresentaram menos tipos celulares supressores, como células T reguladoras, certos macrófagos e células supressoras derivadas de mieloides, e mais defensores agressivos como células T citotóxicas e células natural killer. Essas células T produziram mais perforina e granzima—moléculas que perfuram células cancerosas—e mais mensageiros inflamatórios como interferon-gama e fator de necrose tumoral. Ao bloquear PD-L1 enquanto também ativavam a imunidade inata, as vesículas transformaram um bairro tumoral frio e protegido em um ambiente que acolhe e sustenta um assalto imune.
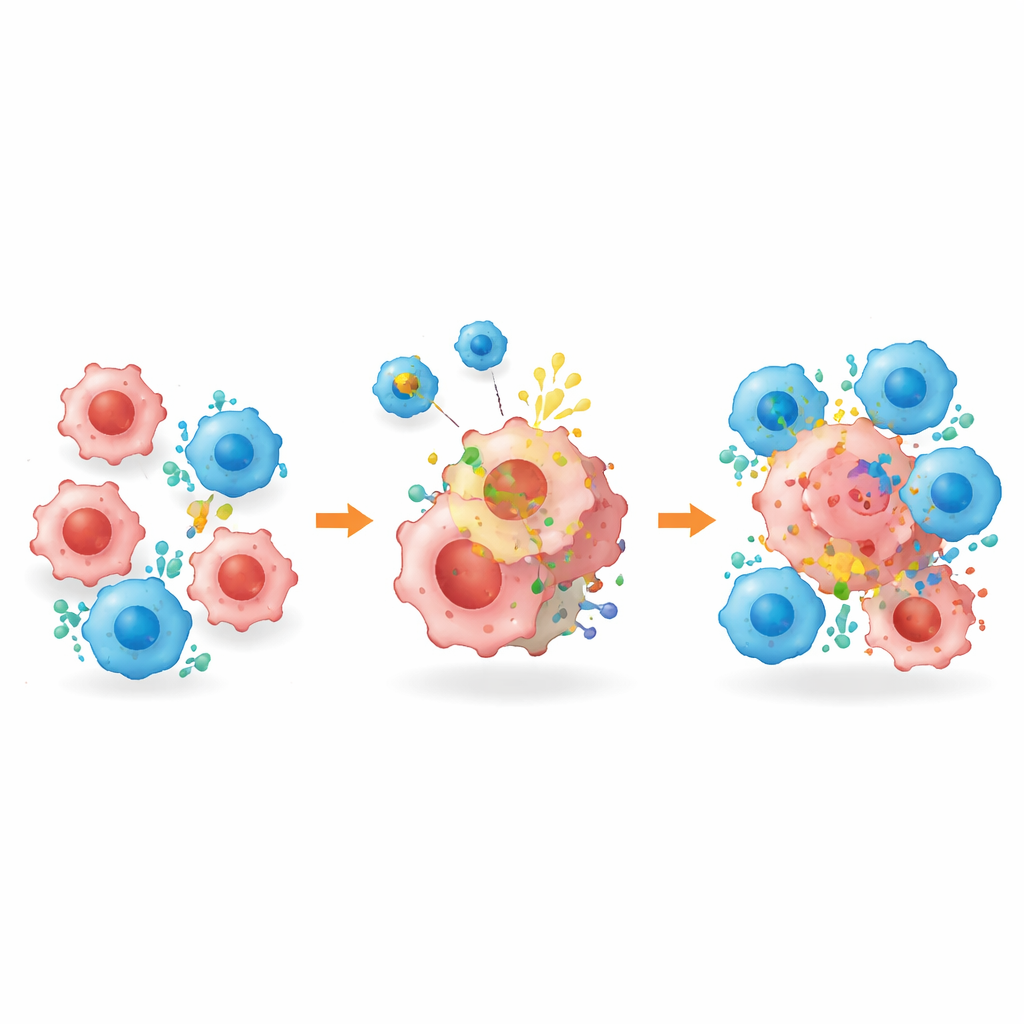
Marcando células tumorais ocultas para eliminação
Além de remodelar o ambiente tumoral, a plataforma—batizada BROAD-CAR—enfrentou diretamente o problema da ausência de alvos. Em tumores mistos contendo células HER2-positivas e HER2-negativas, a terapia CAR-T convencional dirigida a HER2 inicialmente reduziu os tumores, mas deixou para trás células que haviam perdido o alvo, levando ao recrudescimento. Quando combinada com BROAD-CAR, no entanto, os tumores foram quase erradicados: as vesículas provocaram a aparição de HER2 em células anteriormente negativas, permitindo que as células CAR-T as reconhecessem e as matassem. A mesma estratégia funcionou em tumores hepáticos que originalmente não tinham HER2. Importante, análises detalhadas mostraram que a decoração com HER2 permaneceu confinada ao tecido tumoral, sem expressão detectável em órgãos saudáveis ou em células imunes, e o tratamento não causou danos orgânicos óbvios nem perda de peso nos camundongos.
Proteção duradoura contra recidiva e disseminação
Os benefícios se estenderam além do tumor inicial. Em modelos de câncer de mama, o tratamento combinado BROAD-CAR e CAR-T não apenas reduziu os tumores primários como também diminuiu drasticamente as metástases pulmonares. Camundongos que foram totalmente curados resistiram a um novo desafio posterior com células cancerosas, quer essas células expressassem HER2 ou não, sugerindo que a batalha inicial intensa desencadeou uma memória imune mais ampla e duradoura contra o tumor. Isso indica que a plataforma pode não apenas potencializar um único produto de células T modificadas, mas também ajudar o sistema imune mais amplo a aprender a reconhecer o câncer de forma mais completa.
O que isto pode significar para o cuidado do câncer no futuro
De modo geral, o estudo mostra que vesículas bacterianas podem ser transformadas em auxiliares seguros e adaptáveis que tornam a terapia CAR-T muito mais eficaz contra tumores sólidos resistentes. Ao tanto liberar os freios imunes quanto pintar alvos claros e temporários nas células tumorais, o sistema BROAD-CAR permitiu que células T modificadas eliminassem cânceres diversos e até sem alvos aparentes em camundongos, evitando tecidos saudáveis. Se resultados semelhantes forem observados em humanos, essa abordagem poderia expandir o tratamento com CAR-T para muito mais pacientes com tumores sólidos e reduzir a probabilidade de recaídas por perda de antígeno, oferecendo uma nova e potente forma de ajudar o sistema imune a concluir o que começa.
Citação: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Palavras-chave: terapia com células CAR-T, tumores sólidos, microambiente tumoral, vesículas de membrana externa bacterianas, imunoterapia contra o câncer