Clear Sky Science · zh
一种双重染色自动流式细胞术方法用于连续生物反应器中细菌的实时监测
实时观察微生物的工作状态
现代生物技术依赖大量细菌培养来生产从药物到作物保护剂的各种产物。然而,在那些气泡翻腾的大罐内,要在任一时刻准确了解微生物的生理状态却并不容易。本研究介绍了一种类似自动显微观察的系统,能够每小时观察单个细菌细胞,不仅揭示细胞数量,还能判断它们是否在活跃生长和复制DNA。这样的实时洞见有可能使工业发酵更高效、更可靠且更易于控制。

为什么只数细胞还不够
在工业发酵罐中,细胞密度有助于决定何时补料、何时收获以及工艺的生产力。传统工具——如光密度读数、干重测定或电学传感器——测量的是培养物的整体浑浊度或质量。这些方法有用但粗糙:它们无法区分活细胞与不活跃细胞,忽视尺寸和形态差异,也无法判断细胞是否正在准备分裂。因此,操作人员常常在部分盲区调整工艺,依赖的是滞后或间接的信号。
一种新的自动化细菌生命窗口
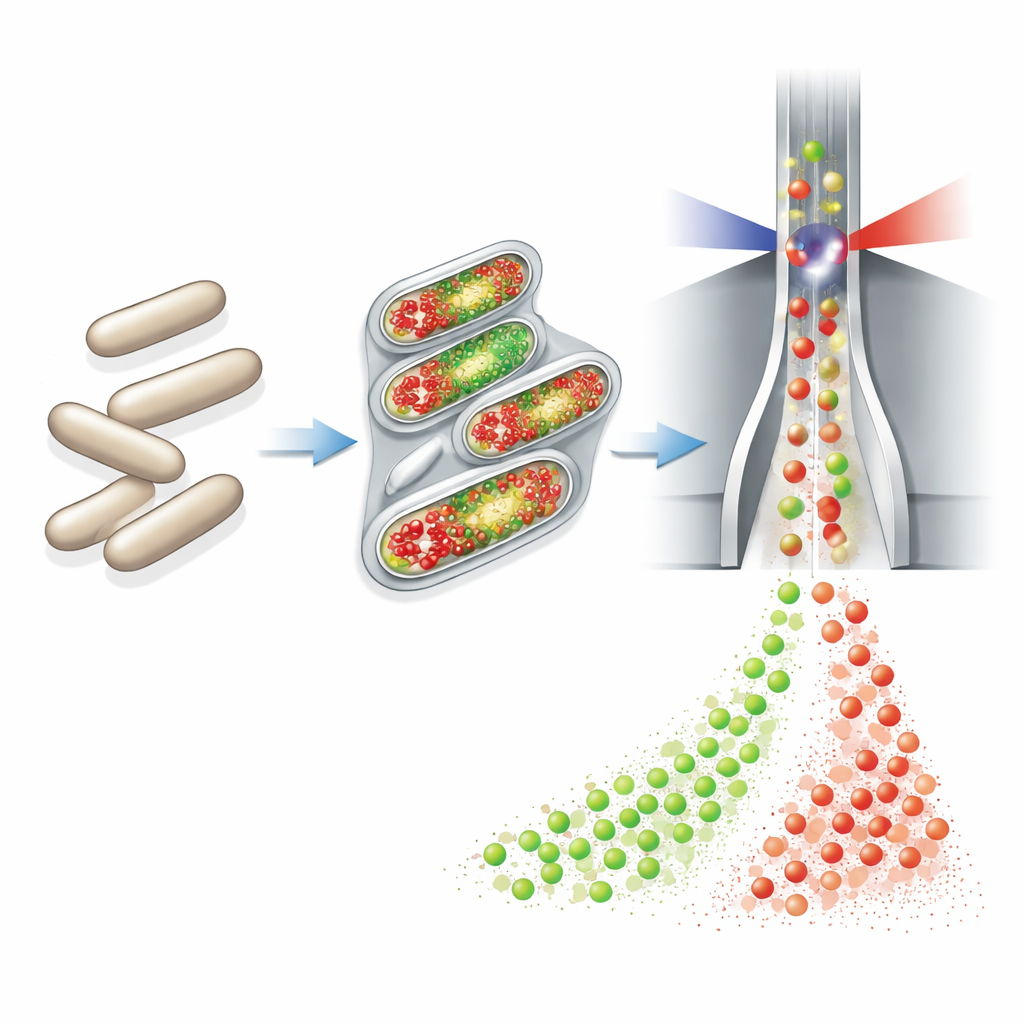
作者基于流式细胞术这一技术——该技术可以在细胞通过激光束时快速测量成千上万个单细胞的性质——进行了扩展。他们将一个全自动取样与染色装置连接到小型连续生物反应器。该装置每小时抽取极少量培养物,对细胞进行化学固定和透化,加入两种荧光染料,稀释样品后直接送入细胞仪。第一种染料(DAPI)的荧光强度与每个细胞所含DNA量成比例,是细胞生长与染色体拷贝数的敏感指示。第二种染料通过“click”反应连接到一种名为EdU的DNA合成前体,特异性标记正在复制DNA的细胞——也就是即将分裂的细胞。
逐个细胞追踪细菌生长
研究团队在三种无致病性革兰氏阴性细菌上测试了该系统:一种土壤分布的布拉氏根瘤菌(Bradyrhizobium)菌株、模式种大肠杆菌(Escherichia coli)和与植物有关的Stenotrophomonas rhizophila。在连续培养中,他们改变新鲜培养基流过反应器的速度(稀释率),并让自动系统持续运行。细胞仪报告了细胞计数和每个细胞的平均DAPI信号,后者反映DNA含量。在各种条件下,DAPI信号的上升稳定地出现在细胞数明显增加或氧耗变化之前。这个早期预警显示,细胞在传统指标发出警示之前就已经开始加速DNA复制和生长,从而原则上可以更早地调整补料或操作条件。该方法还能捕捉每个物种在不同流速下进入并维持稳态生长的方式,以及在非常高稀释率下,培养稀释但富集了生长更快、DNA含量更高的细胞的现象。
成功之处与局限
在封闭的批培养实验(瓶或孔板)中,基于EdU的染料成功标记出DNA复制的高峰,接种后不久达到最高值,随后随着培养减缓而下降。它能追踪具有多拷贝染色体的细胞亚群的出现与消失,证实其对活跃复制细胞的可靠标记能力。然而,当在小型反应器的培养基中连续供应EdU时,往往会减慢或干扰生长。对S. rhizophila而言,EdU几乎使培养停止;对布拉氏根瘤菌则显著降低了细胞数;即便是大肠杆菌,生长也变慢且复制信号仅出现在最初数小时内。增加荧光染料用量并不能解决该问题。作者得出结论:在持续暴露条件下,EdU对生长抑制性过强且技术上过于挑剔,不适合作为工业监测中的常规复制标记物。
对更智能生物反应器的启示
尽管存在EdU的限制,双重染色工作流程证明了自动在线流式细胞术可以提供丰富的、时间分辨的细菌生理学图景。计数细胞并跟踪其DAPI信号,提供了对生物量的稳健直接测量以及不同稀释率下生长变化的早期指示。集成的取样—染色—细胞仪链条每小时运行且几乎不需人工干预,表明此类系统可以嵌入未来的生产线中。虽然本文测试的特定复制染料尚不适合作为日常控制细菌工厂的工具,但相同的自动化框架可以与其他荧光标记物配合使用。从长远看,这类实时、单细胞监测有助于将生物反应器维持在最佳“甜点”区,从而提高产量、稳定性和各类微生物工艺的产品质量。
引用: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
关键词: 自动化流式细胞术, 细菌生物反应器, 实时生物工艺监测, 细胞周期与DNA复制, 工业生物技术