Clear Sky Science · sv
En tvåfärgsautomatisk flödescytometri-metod för realtidsövervakning av bakterier i kontinuerliga bioreaktorer
Att iaktta mikrober i realtid
Modern bioteknik förlitar sig på stora bakteriekulturer för att tillverka allt från läkemedel till växtskyddsmedel. Ändå är det förvånansvärt svårt att veta vad mikroberna gör vid varje givet ögonblick inne i de skummande tankarna. Denna studie introducerar ett automatiserat, mikroskopliknande system som kan följa enskilda bakterieceller varje timme och avslöja inte bara hur många som finns utan också om de aktivt växer och kopierar sitt DNA. Sådan realtidsinsikt kan göra industriell jäsning mer effektiv, pålitlig och lättare att styra.

Varför cellräkning inte räcker
I industriella fermentorer hjälper celltäthet att avgöra när mer näring ska tillföras, när skörd ska ske och hur produktiv en process kan vara. Traditionella verktyg — som optisk densitet, torrviktsmätningar eller elektriska sensorer — mäter kulturens övergripande grumlighet eller massa. De är användbara men grova: de kan inte skilja levande från inaktiva celler, förbiser skillnader i storlek och form och säger inget om huruvida celler förbereder sig för delning. Som en följd arbetar operatörer ofta delvis i blindo och justerar processer utifrån fördröjda eller indirekta signaler.
En ny automatiserad fönster mot bakterielivet
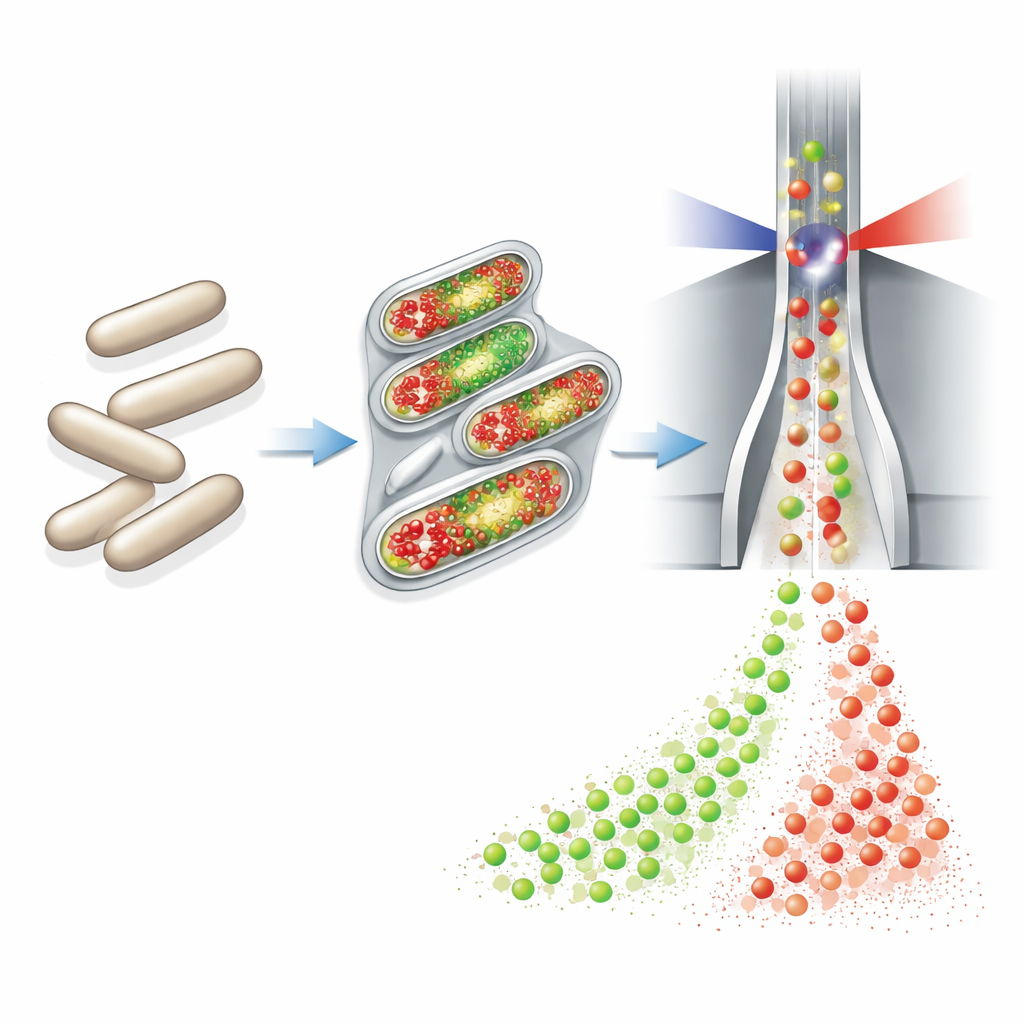
Författarna byggde vidare på en teknik kallad flödescytometri, som snabbt mäter egenskaper hos tusentals enskilda celler när de passerar en laserstråle. De kopplade en helt automatiserad provtagar- och färgningsenhet till små kontinuerliga bioreaktorer. Varje timme drog enheten en mycket liten volym kultur, fixade och permeabiliserade cellerna kemiskt, tillsatte två fluorescerande färgämnen, spädde provet och skickade det direkt till en cytometer. Ett färgämne (DAPI) lyser i proportion till hur mycket DNA varje cell innehåller och fungerar som en känslig indikator på celltillväxt och kromosomantal. Det andra färgämnet, bundet genom en ”click”-reaktion till en DNA-byggsten som kallas EdU, markerar specifikt celler som håller på att kopiera sitt DNA — de som är på väg att dela sig.
Att följa bakterietillväxt, en cell i taget
Teamet testade denna uppsättning på tre icke-patogena Gram-negativa bakterier: en jordlevande Bradyrhizobium-stam, modellarten Escherichia coli och den växtassocierade Stenotrophomonas rhizophila. I kontinuerliga kulturer varierade de hur snabbt färskt medium flödade genom reaktorerna (spädningshastigheten) och lät det automatiska systemet köra. Cytometern rapporterade både cellantal och genomsnittlig DAPI-signal per cell, vilket speglar DNA-innehåll. Över förhållandena visade en ökning i DAPI-signal pålitligt före synliga ökningar i cellantal eller förändringar i syreförbrukning. Denna tidiga varning visade att cellerna ökade DNA-replikation och tillväxt långt innan traditionella indikatorer skulle signalera en förändring, vilket i princip möjliggör tidigare justeringar av näringstillförsel eller driftsparametrar. Metoden fångade också hur varje art gick in i och bibehöll jämn tillväxt vid olika flödeshastigheter, och hur kulturer vid mycket hög spädning tunnades ut men berikades av snabbare växande celler med högre DNA-innehåll.
Vad som fungerade — och vad som inte gjorde det
I batchexperiment (slutna kolvar eller plattor) markerade EdU-baserat färgämne framgångsrikt perioder av DNA-replikation, med toppar strax efter inokulationen och därefter minskning när kulturerna saktade ner. Det följde framträdandet och försvinnandet av undergrupper med många kromosomkopior och bekräftade att det pålitligt markerar aktivt replikerande celler. När EdU däremot kontinuerligt tillsattes i mediet i de små reaktorerna, hämmande det ofta eller störde tillväxten. För S. rhizophila stoppade det nästan kulturen; för Bradyrhizobium minskade det kraftigt cellantalet; och även E. coli växte långsammare och visade replikeringssignaler endast under de första timmarna. Ökad mängd fluorescerande färgämne löste inte problemet. Författarna drar slutsatsen att EdU vid kontinuerlig exponering är för tillväxthämmande och tekniskt kinkig för att fungera som en rutinmässig replikationsmarkör i industriell övervakning.
Konsekvenser för smartare bioreaktorer
Trots begränsningarna med EdU visade dubbelmärkningsarbetsflödet att automatiserad online-flödescytometri kan leverera rika, tidsupplösta bilder av bakteriefysiologi. Att räkna celler och följa deras DAPI-signal gav ett robust, direkt mått på biomassa och en tidig indikation på tillväxtförändringar vid olika spädningshastigheter. Den integrerade kedjan av provtagare–färgare–cytometer körde timvis med minimal mänsklig inblandning, vilket visar att sådana system kan vävas in i framtida produktionslinjer. Medan den specifika replikeringsfärg som testats här ännu inte är redo för daglig styrning av bakteriefabriker, kan samma automatiserade ramverk paras med andra fluorescerande markörer. På sikt kan denna typ av realtidsövervakning på enklallsnivå hjälpa till att hålla bioreaktorer i deras optimala ”sweet spot”, förbättra utbyten, stabilitet och produktkvalitet för en mängd mikrobiella processer.
Citering: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Nyckelord: automatisk flödescytometri, bakteriella bioreaktorer, realtidsövervakning av bioprocesser, cellcykel och DNA-replikation, industriell bioteknik