Clear Sky Science · pl
Metoda z podwójnym znakowaniem w zautomatyzowanej cytometrii przepływowej do monitorowania bakterii w czasie rzeczywistym w ciągłych bioreaktorach
Obserwowanie pracy mikrobów w czasie rzeczywistym
Nowoczesna biotechnologia opiera się na masowych hodowlach bakterii produkujących wszystko, od leków po środki ochrony roślin. Jednak w tych pieniących się zbiornikach zaskakująco trudno jest w danej chwili wiedzieć, co robią mikroby. W pracy tej przedstawiono zautomatyzowany system przypominający mikroskop, który może obserwować pojedyncze komórki bakteryjne co godzinę, ujawniając nie tylko ich liczbę, lecz także to, czy aktywnie rosną i kopiują swoje DNA. Taka wiedza w czasie rzeczywistym może uczynić fermentację przemysłową bardziej wydajną, niezawodną i łatwiejszą do kontrolowania.

Dlaczego liczenie komórek to za mało
W fermentorach przemysłowych gęstość komórek pomaga określić, kiedy dodać pożywki, kiedy zebrać produkt i jak wydajny może być proces. Tradycyjne narzędzia — takie jak pomiary gęstości optycznej, suchej masy czy czujniki elektryczne — mierzą ogólne zmętnienie lub masę hodowli. Są użyteczne, lecz prymitywne: nie rozróżniają komórek żywych od nieaktywnych, pomijają różnice w rozmiarze i kształcie oraz nie informują o tym, czy komórki przygotowują się do podziału. W efekcie operatorzy często działają częściowo „na ślepo”, dostosowując procesy na podstawie opóźnionych lub pośrednich sygnałów.
Nowe, zautomatyzowane okno na życie bakterii
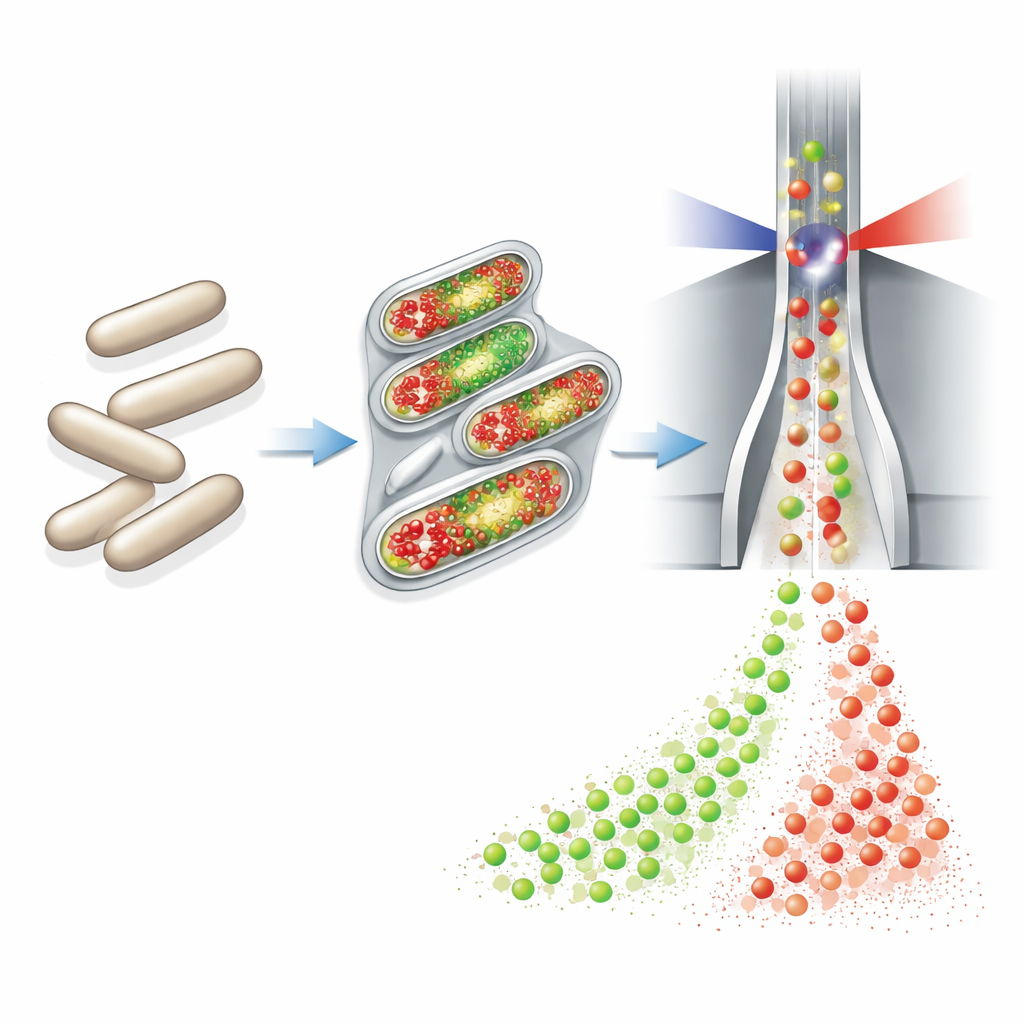
Autorzy oparli się na technologii zwanej cytometrią przepływową, która szybko mierzy właściwości tysięcy pojedynczych komórek przechodzących przez wiązkę lasera. Podłączyli w pełni zautomatyzowane urządzenie do pobierania próbek i znakowania barwnikami do małych ciągłych bioreaktorów. Co godzinę urządzenie pobierało niewielką objętość hodowli, chemicznie utrwalało i permeabilizowało komórki, dodawało dwa barwniki fluorescencyjne, rozcieńczało próbkę i wysyłało ją bezpośrednio do cytometru. Jeden barwnik (DAPI) świeci proporcjonalnie do ilości DNA w każdej komórce, służąc jako czuły wskaźnik wzrostu i liczby kopii chromosomów. Drugi barwnik, przyłączany poprzez reakcję „click” do cegiełki DNA zwanej EdU, specyficznie oznacza komórki będące w trakcie kopiowania DNA — te przygotowujące się do podziału.
Śledzenie wzrostu bakterii, komórka po komórce
Zespół przetestował to rozwiązanie na trzech niepatogennych bakteriach Gram-ujemnych: glebowym szczepie Bradyrhizobium, modelowym Escherichia coli oraz związanej z roślinami Stenotrophomonas rhizophila. W hodowlach ciągłych zmieniano szybkość przepływu świeżego medium przez reaktory (wskaźnik rozcieńczenia) i uruchamiano zautomatyzowany system. Cytometr raportował zarówno liczby komórek, jak i średni sygnał DAPI na komórkę, odzwierciedlający zawartość DNA. We wszystkich warunkach wzrost sygnału DAPI pojawiał się pewnie przed widocznymi wzrostami liczby komórek lub zmianami w zużyciu tlenu. To wczesne ostrzeżenie pokazywało, że komórki zwiększają replikację DNA i wzrost znacznie wcześniej niż sygnalizowałyby tradycyjne wskaźniki, co w praktyce umożliwia wcześniejsze dostosowanie dokarmiania lub parametrów pracy. Metoda uchwyciła też, jak każdy gatunek wchodził i utrzymywał stabilny wzrost przy różnych przepływach oraz jak przy bardzo wysokim rozcieńczeniu kultury rzedły, lecz były wzbogacone w szybciej rosnące komórki o wyższej zawartości DNA.
Co zadziałało — a co nie
W eksperymentach wsadowych (zamknięte kolby lub płytki) barwnik oparty na EdU skutecznie uwidaczniał fale replikacji DNA, osiągając maksimum wkrótce po inokulacji, a następnie spadając w miarę zwalniania wzrostu kultur. Śledził pojawianie się i znikanie podgrup komórek z wieloma kopiami chromosomów, potwierdzając, że wiarygodnie oznacza aktywnie replikujące komórki. Jednak gdy EdU było ciągle dostarczane w medium małych reaktorów, często spowalniało lub zaburzało wzrost. Dla S. rhizophila niemal zatrzymywało hodowlę; dla Bradyrhizobium silnie zmniejszało liczbę komórek; a nawet E. coli rosło wolniej i wykazywało sygnały replikacji tylko w pierwszych godzinach. Zwiększenie ilości barwnika fluorescencyjnego nie rozwiązało problemu. Autorzy wnioskują, że przy ciągłej ekspozycji EdU jest zbyt hamujące dla wzrostu i technicznie kapryśne, by służyć jako rutynowy znacznik replikacji w monitoringu przemysłowym.
Implikacje dla inteligentniejszych bioreaktorów
Mimo ograniczeń związanych z EdU, schemat podwójnego znakowania dowiódł, że zautomatyzowana cytometria przepływowa online może dostarczać bogate, czasowo rozdzielcze obrazy fizjologii bakterii. Liczenie komórek i śledzenie ich sygnału DAPI dawało solidny, bezpośredni pomiar biomasy oraz wczesny wskaźnik zmian wzrostu przy różnych wskaźnikach rozcieńczenia. Zintegrowany łańcuch: pobieracz–znakowacz–cytometr działał co godzinę przy minimalnej interwencji człowieka, pokazując, że takie systemy można włączyć do przyszłych linii produkcyjnych. Chociaż testowany tutaj konkretny barwnik replikacyjny nie jest jeszcze gotowy do codziennej kontroli „fabryk” bakteryjnych, ta sama zautomatyzowana platforma może być sparowana z innymi markerami fluorescencyjnymi. W dłuższej perspektywie tego typu monitorowanie pojedynczych komórek w czasie rzeczywistym może pomóc utrzymać bioreaktory w optymalnym „punkcie”, poprawiając plony, stabilność i jakość produktu w szerokim spektrum procesów mikrobiologicznych.
Cytowanie: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Słowa kluczowe: zautomatyzowana cytometria przepływowa, bioreaktory bakteryjne, monitorowanie bioprocesów w czasie rzeczywistym, cykl komórkowy i replikacja DNA, biotechnologia przemysłowa