Clear Sky Science · de
Eine doppelfärbende automatisierte Durchflusszytometrie-Methode zur Echtzeit-Überwachung von Bakterien in kontinuierlichen Bioreaktoren
Mikroben bei der Arbeit in Echtzeit beobachten
Die moderne Biotechnologie baut auf riesigen Bakterienkulturen auf, die alles von Arzneimitteln bis zu Pflanzenschutzmitteln herstellen. Doch in diesen schäumenden Tanks ist es überraschend schwierig zu wissen, was die Mikroben in einem bestimmten Moment tun. Diese Studie stellt ein automatisiertes, mikroskopieähnliches System vor, das einzelne Bakterienzellen stündlich beobachtet und nicht nur zeigt, wie viele vorhanden sind, sondern auch, ob sie aktiv wachsen und ihre DNA replizieren. Solche Echtzeit-Einblicke könnten industrielle Fermentationen effizienter, zuverlässiger und leichter steuerbar machen.

Warum Zellzählungen allein nicht ausreichen
In industriellen Fermentern hilft die Zelldichte bei Entscheidungen, wann mehr Nährstoffe zugegeben, wann geerntet werden soll und wie produktiv ein Prozess ist. Traditionelle Werkzeuge – wie optische Dichtebestimmungen, Trockenmasse-Messungen oder elektrische Sensoren – messen die makroskopische Trübung oder Masse einer Kultur. Sie sind nützlich, aber grob: Sie können lebende von inaktiven Zellen nicht unterscheiden, übersehen Unterschiede in Größe und Form und sagen nichts darüber aus, ob Zellen sich auf die Teilung vorbereiten. Deshalb arbeiten Betreiber oft teilweise im Blindflug und passen Prozesse auf Basis verzögerter oder indirekter Signale an.
Ein neues automatisiertes Fenster in das bakterielle Leben
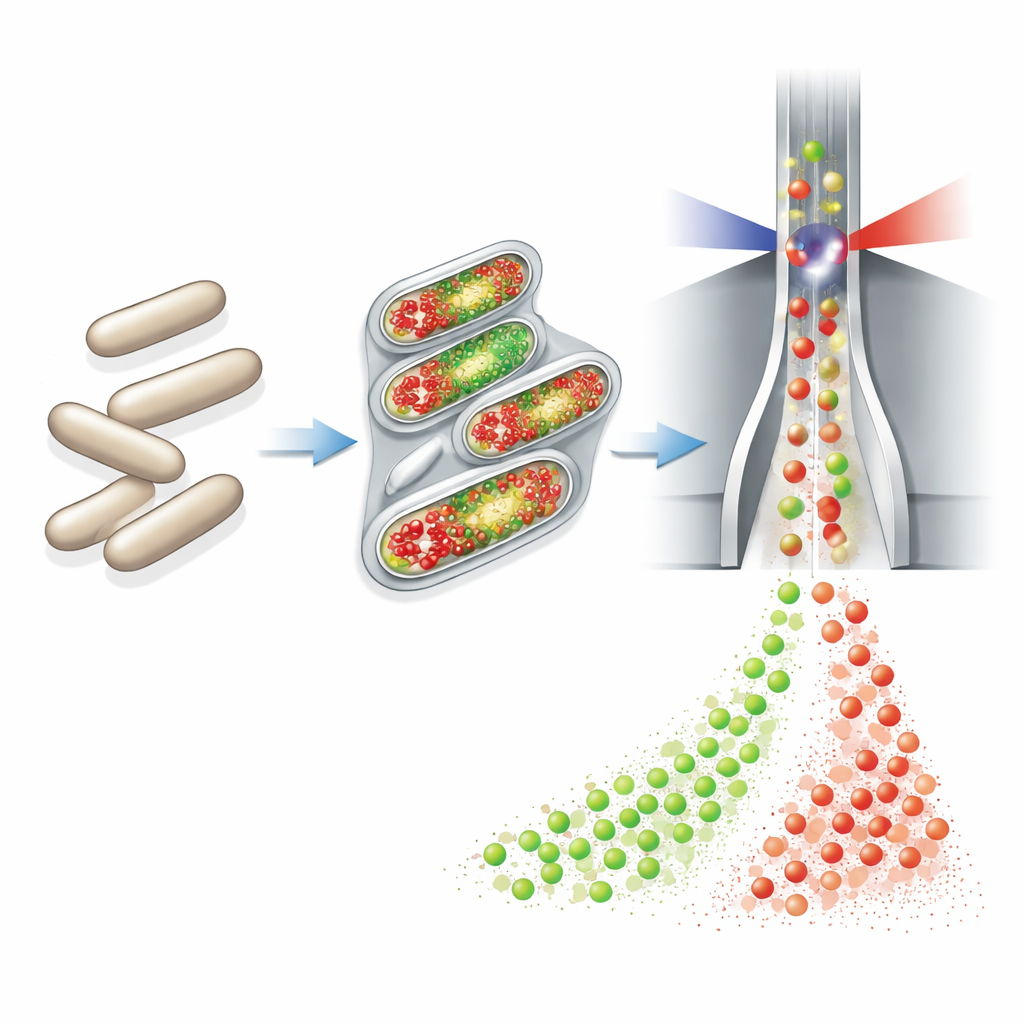
Die Autoren bauten auf einer Technologie namens Durchflusszytometrie auf, die Eigenschaften von Tausenden einzelnen Zellen schnell misst, während sie einen Laser passieren. Sie schlossen ein vollständig automatisiertes Probenahme- und Färbesystem an kleine kontinuierliche Bioreaktoren an. Stündlich entnahm dieses Gerät ein winziges Kulturvolumen, fixierte und permeabilisierte chemisch die Zellen, fügte zwei fluoreszierende Farbstoffe hinzu, verdünnte die Probe und leitete sie direkt an einen Zyto¬meter weiter. Ein Farbstoff (DAPI) fluoresziert proportional zur DNA-Menge jeder Zelle und dient als empfindlicher Indikator für Zellwachstum und Chromosomenkopienzahl. Der zweite Farbstoff, über eine „Click“-Reaktion an einen DNA-Baustein namens EdU gebunden, markiert spezifisch Zellen, die gerade ihre DNA kopieren – also Zellen kurz vor der Teilung.
Bakterielles Wachstum verfolgen, Zelle für Zelle
Das Team testete dieses Setup an drei nicht-pathogenen, gramnegativen Bakterien: einem bodenbewohnenden Bradyrhizobium-Stamm, dem Modellorganismus Escherichia coli und dem pflanzenassoziierten Stenotrophomonas rhizophila. In kontinuierlichen Kulturen variierten sie die Geschwindigkeit, mit der frisches Medium durch die Reaktoren floss (die Verdünnungsrate), und ließen das automatisierte System laufen. Der Zytometer berichtete sowohl Zellzahlen als auch das durchschnittliche DAPI-Signal pro Zelle, das den DNA-Gehalt widerspiegelt. Unter den untersuchten Bedingungen trat ein Anstieg des DAPI-Signals zuverlässig vor sichtbaren Zunahmen der Zellzahl oder Änderungen im Sauerstoffverbrauch auf. Diese Frühwarnung zeigte, dass die Zellen die DNA-Replikation und das Wachstum hochfuhren, lange bevor traditionelle Indikatoren eine Verschiebung melden würden, und würde prinzipiell frühere Anpassungen der Nährstoffzufuhr oder Betriebsbedingungen erlauben. Die Methode erfasste außerdem, wie jede Spezies bei verschiedenen Durchflussraten in einen stabilen Wachstumszustand eintrat und diesen hielt, und wie bei sehr hoher Verdünnung die Kulturen ausdünnten, aber in schnellwüchsige Zellen mit höherem DNA-Gehalt angereichert waren.
Was funktionierte — und was nicht
In Batch-Experimenten (geschlossene Kolben oder Platten) hob der EdU-basierte Farbstoff erfolgreich DNA-Replikationsausbrüche hervor, die kurz nach der Inokulation ihren Höhepunkt erreichten und dann abnahmen, als die Kulturen langsamer wurden. Er verfolgte das Erscheinen und Verschwinden von Untergruppen mit vielen Chromosomenkopien und bestätigte damit, dass er aktiv replizierende Zellen zuverlässig markiert. Als EdU jedoch kontinuierlich im Medium der kleinen Reaktoren zugeführt wurde, beeinträchtigte es oft das Wachstum oder störte es. Bei S. rhizophila stoppte es die Kultur nahezu; bei Bradyrhizobium reduzierte es die Zellzahlen stark; und selbst E. coli wuchs langsamer und zeigte Replikationssignale nur in den frühen Stunden. Eine Erhöhung der Farbstoffmenge behob dieses Problem nicht. Die Autoren schlussfolgern, dass EdU bei kontinuierlicher Exposition zu wachstumshemmend und technisch problematisch ist, um als routinemäßiger Replikationsmarker in der industriellen Überwachung zu dienen.
Folgen für intelligentere Bioreaktoren
Trotz der EdU-Beschränkungen zeigte der doppelfärbende Workflow, dass automatisierte Online-Durchflusszytometrie reichhaltige, zeitaufgelöste Einblicke in die bakterielle Physiologie liefern kann. Zellzählungen und das Verfolgen des DAPI-Signals lieferten eine robuste, direkte Messung der Biomasse und einen frühen Indikator für Wachstumsänderungen bei unterschiedlichen Verdünnungsraten. Die integrierte Probennehmer–Färber–Zytometer-Kette arbeitete stündlich mit minimalem menschlichem Eingriff und zeigte, dass solche Systeme in zukünftige Produktionslinien eingebunden werden können. Während der hier getestete Replikationsfarbstoff noch nicht für die tägliche Steuerung bakterieller Fabriken geeignet ist, kann derselbe automatisierte Rahmen mit anderen fluoreszenten Markern kombiniert werden. Langfristig könnte diese Art der Echtzeit-Einzelzellüberwachung helfen, Bioreaktoren in ihrem optimalen „Sweet Spot“ zu halten und so Ausbeuten, Stabilität und Produktqualität für eine breite Palette mikrobieller Prozesse zu verbessern.
Zitation: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Schlüsselwörter: automatisierte Durchflusszytometrie, bakterielle Bioreaktoren, Echtzeit-Bioprozessüberwachung, Zellzyklus und DNA-Replikation, industrielle Biotechnologie