Clear Sky Science · fr
Méthode automatisée de cytométrie en flux à double marquage pour la surveillance en temps réel des bactéries dans des bioréacteurs continus
Observer les microbes en action, en temps réel
La biotechnologie moderne repose sur d’immenses cultures bactériennes pour produire tout, des médicaments aux agents de protection des cultures. Pourtant, à l’intérieur de ces cuves écumantes, il reste étonnamment difficile de savoir ce que font les microbes à un instant donné. Cette étude présente un système automatisé, proche d’un microscope, capable d’observer des cellules bactériennes individuelles chaque heure, révélant non seulement leur nombre mais aussi si elles sont en croissance active et en train de copier leur ADN. Ce type d’informations en temps réel pourrait rendre la fermentation industrielle plus efficace, fiable et plus facile à contrôler.

Pourquoi compter les cellules ne suffit pas
Dans les fermenteurs industriels, la densité cellulaire aide à décider quand apporter des nutriments, quand récolter et quelle productivité attendre. Les outils traditionnels — lectures de densité optique, mesures de matière sèche ou capteurs électriques — mesurent la turbidité ou la masse globale d’une culture. Ils sont utiles mais grossiers : ils ne permettent pas de distinguer les cellules vivantes des inactives, négligent les différences de taille et de forme, et n’indiquent rien sur le fait que les cellules se préparent à se diviser. En conséquence, les opérateurs travaillent souvent en partie à l’aveugle, ajustant les procédés sur la base de signaux retardés ou indirects.
Une nouvelle fenêtre automatisée sur la vie bactérienne
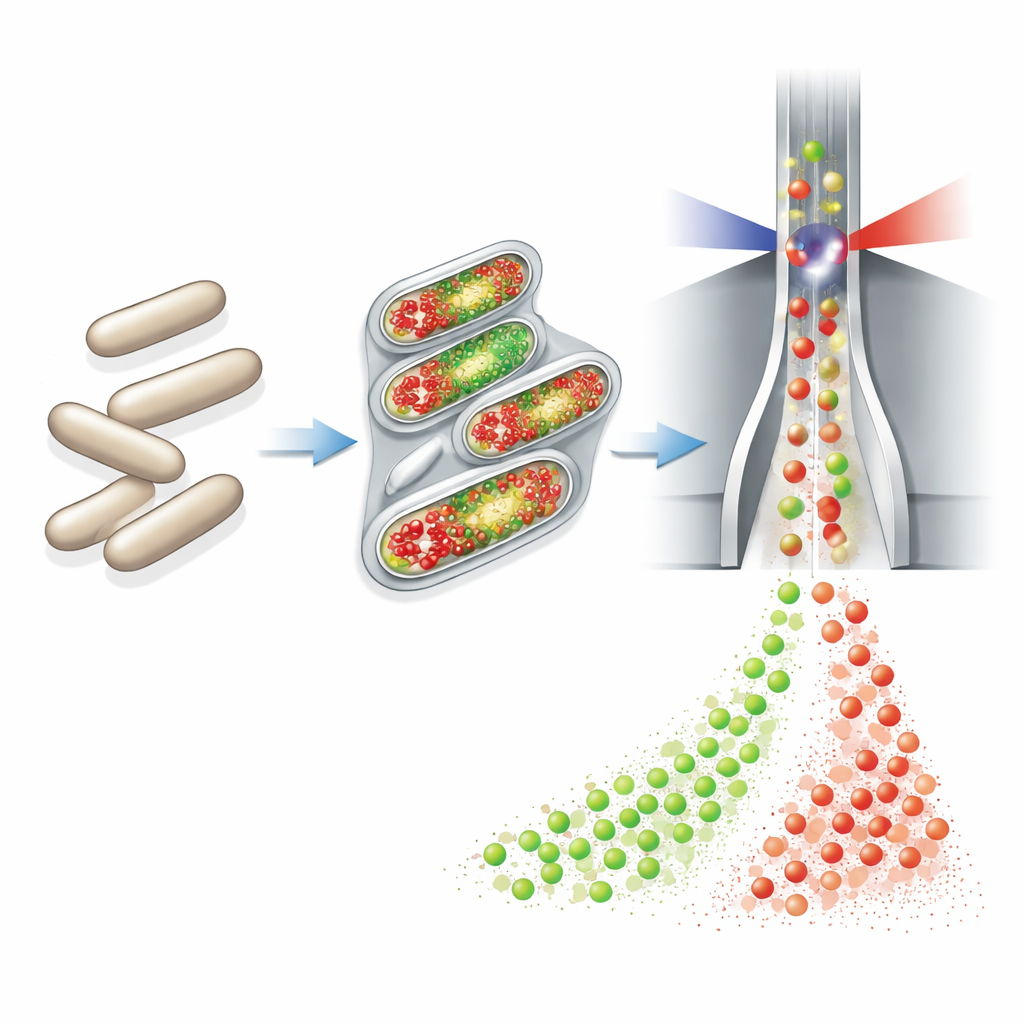
Les auteurs se sont appuyés sur une technique appelée cytométrie en flux, qui mesure rapidement les propriétés de milliers de cellules individuelles lorsqu’elles traversent un faisceau laser. Ils ont connecté un dispositif entièrement automatisé d’échantillonnage et de marquage à de petits bioréacteurs continus. Toutes les heures, l’appareil prélevait un volume minime de culture, fixait et perméabilisait chimiquement les cellules, ajoutait deux colorants fluorescents, diluait l’échantillon puis l’envoyait directement au cytomètre. Un colorant (DAPI) s’illumine en proportion de la quantité d’ADN contenue dans chaque cellule, servant d’indicateur sensible de la croissance cellulaire et du nombre de copies chromosomiques. Le second colorant, lié via une réaction « click » à un précurseur d’ADN appelé EdU, marque spécifiquement les cellules en train de répliquer leur ADN — celles qui sont sur le point de se diviser.
Suivre la croissance bactérienne, cellule par cellule
L’équipe a testé ce dispositif sur trois bactéries Gram négatives non pathogènes : une souche de Bradyrhizobium du sol, l’espèce modèle Escherichia coli, et la plante associée Stenotrophomonas rhizophila. Dans des cultures continues, ils ont fait varier la vitesse d’alimentation en milieu frais (le taux de dilution) et laissé le système automatisé fonctionner. Le cytomètre a rendu compte à la fois des nombres de cellules et du signal DAPI moyen par cellule, qui reflète la teneur en ADN. Dans toutes les conditions, une hausse du signal DAPI est apparue de façon fiable avant les augmentations visibles du nombre de cellules ou les changements d’utilisation d’oxygène. Cet avertissement précoce montrait que les cellules augmentaient leur réplication d’ADN et leur croissance bien avant que les indicateurs traditionnels ne signalent un changement, permettant en principe des ajustements plus rapides de l’alimentation ou des conditions d’exploitation. La méthode a aussi capté la façon dont chaque espèce entrait en croissance stable à différents débits, et comment, à des dilutions très élevées, les cultures s’éclaircissaient mais s’enrichissaient en cellules à croissance plus rapide et à plus forte teneur en ADN.
Ce qui a fonctionné — et ce qui n’a pas marché
Dans les expériences en batch (flacons ou plaques fermés), le colorant à base d’EdU a mis en évidence avec succès des pics de réplication de l’ADN, culminant peu après l’inoculation puis décroissant à mesure que la culture ralentissait. Il a suivi l’apparition et la disparition de sous-groupes de cellules possédant de nombreuses copies chromosomiques, confirmant qu’il marque de façon fiable les cellules en réplication active. Cependant, lorsque l’EdU était fourni en continu dans le milieu des petits réacteurs, il ralentissait souvent la croissance ou la perturbait. Pour S. rhizophila, il a presque arrêté la culture ; pour Bradyrhizobium, il a fortement réduit le nombre de cellules ; et même E. coli a présenté une croissance plus lente et des signaux de réplication seulement pendant les premières heures. Augmenter la quantité de colorant fluorescent n’a pas résolu ce problème. Les auteurs concluent que, en exposition continue, l’EdU est trop inhibiteur de la croissance et trop délicat techniquement pour servir de marqueur de réplication de routine dans la surveillance industrielle.
Conséquences pour des bioréacteurs plus intelligents
Malgré les limites de l’EdU, le protocole à double marquage a démontré que la cytométrie en flux en ligne et automatisée peut fournir des images riches et résolues dans le temps de la physiologie bactérienne. Le comptage des cellules et le suivi de leur signal DAPI ont fourni une mesure directe et robuste de la biomasse et un indicateur précoce des changements de croissance à différents taux de dilution. La chaîne intégrée échantillonneur–marqueur–cytomètre a fonctionné à l’heure avec une intervention humaine minimale, montrant que de tels systèmes peuvent être intégrés aux futures lignes de production. Si le colorant de réplication testé ici n’est pas encore prêt pour le contrôle quotidien des « usines » bactériennes, le même cadre automatisé peut être associé à d’autres marqueurs fluorescents. À long terme, ce type de surveillance en temps réel et au niveau de la cellule unique pourrait aider à maintenir les bioréacteurs dans leur « zone optimale », améliorant les rendements, la stabilité et la qualité des produits pour une large gamme de procédés microbiens.
Citation: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Mots-clés: cytométrie en flux automatisée, bioréacteurs bactériens, surveillance des bioprocédés en temps réel, cycle cellulaire et réplication de l’ADN, biotechnologie industrielle