Clear Sky Science · nl
Een geautomatiseerde flowcytometrie-methode met dubbele kleuring voor realtime monitoring van bacteriën in continue bioreactoren
Microben in real time observeren
Moderne biotechnologie steunt op enorme bacteriecultures om alles te produceren, van geneesmiddelen tot gewasbeschermingsmiddelen. Toch is het in die schuimende tanks verrassend moeilijk om op elk moment te weten wat de microben aan het doen zijn. Deze studie introduceert een geautomatiseerd, microscoopachtig systeem dat individuele bacteriële cellen elk uur kan volgen en niet alleen laat zien hoeveel cellen aanwezig zijn, maar ook of ze actief groeien en hun DNA kopiëren. Dergelijke realtime-inzichten zouden industriële fermentatie efficiënter, betrouwbaarder en beter regelbaar kunnen maken.

Waarom cellentelling niet genoeg is
In industriële fermentoren helpt de celdichtheid bij het bepalen wanneer er meer voedingsstoffen moeten worden toegevoegd, wanneer geoogst moet worden en hoe productief een proces kan zijn. Traditionele instrumenten — zoals optische dichtheidsmetingen, droge-massa-bepalingen of elektrische sensoren — meten de bulkvertroebeling of massa van een cultuur. Ze zijn nuttig maar grof: ze kunnen levende niet onderscheiden van inactieve cellen, zien geen verschillen in grootte en vorm en zeggen niets over of cellen zich voorbereiden op deling. Daardoor werken bedieners vaak deels in het donker en passen ze processen aan op basis van vertraagde of indirecte signalen.
Een nieuw geautomatiseerd venster op bacterieel leven
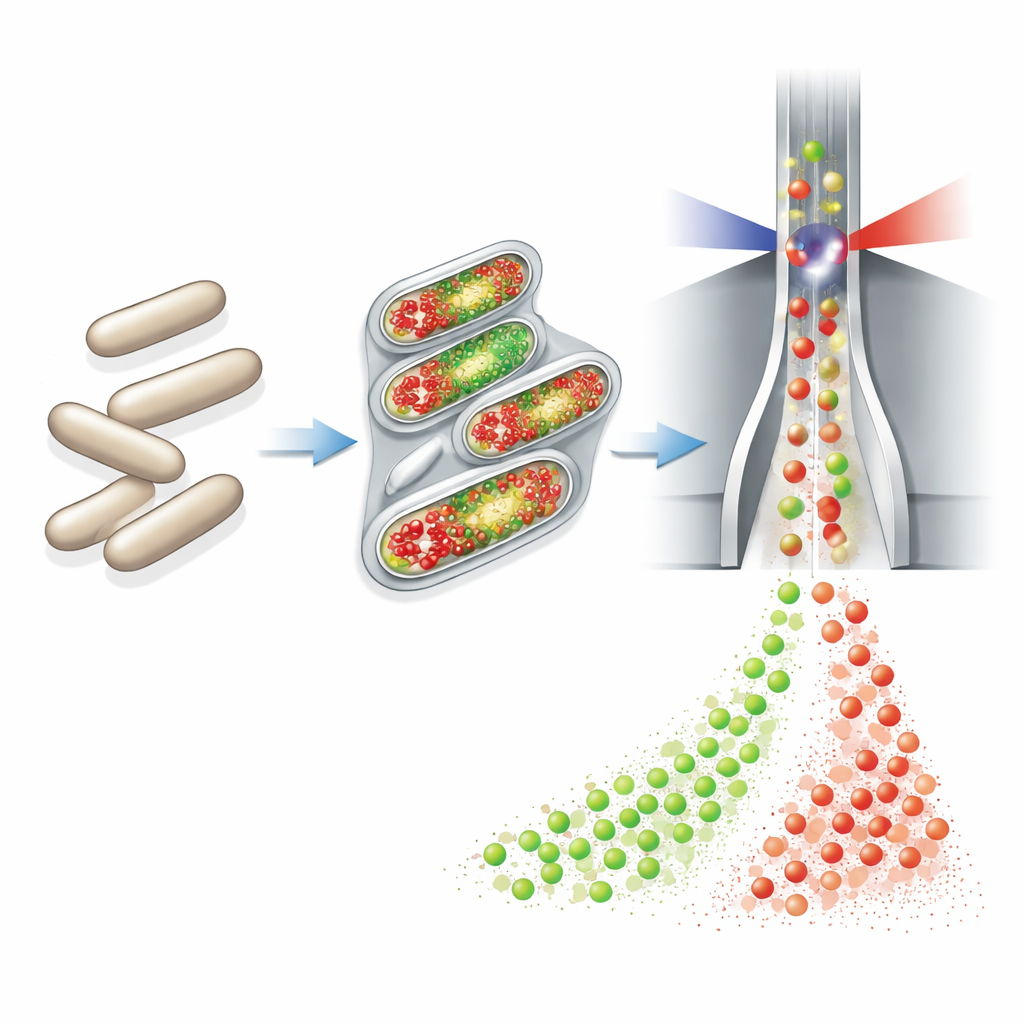
De auteurs bouwden voort op een technologie genaamd flowcytometrie, die snel eigenschappen van duizenden afzonderlijke cellen meet terwijl ze een laserstraal passeren. Ze sloten een volledig geautomatiseerd monstername- en kleuringsapparaat aan op kleine continue bioreactoren. Elk uur nam dit apparaat een kleine hoeveelheid cultuur, fixeerde en permeabiliseerde chemisch de cellen, voegde twee fluorescerende kleurstoffen toe, verdunde het monster en stuurde het direct naar een cytometer. Eén kleurstof (DAPI) fluoresceert evenredig met de hoeveelheid DNA die elke cel bevat en fungeert als een gevoelig teken van celgroei en aantal chromosoomkopieën. De tweede kleurstof, aangebracht via een "click"-reactie op een DNA-bouwsteen genaamd EdU, markeert specifiek cellen die bezig zijn hun DNA te kopiëren — cellen die op het punt staan te delen.
Bacteriële groei volgen, cel voor cel
Het team testte deze opstelling op drie niet-pathogene, Gram-negatieve bacteriën: een in de bodem levende Bradyrhizobium-stam, de modelsoort Escherichia coli en de plantgeassocieerde Stenotrophomonas rhizophila. In continue culturen varieerden ze de snelheid waarmee vers medium door de reactoren stroomde (de verdunningssnelheid) en lieten het geautomatiseerde systeem draaien. De cytometer rapporteerde zowel celaantallen als het gemiddelde DAPI-signaal per cel, dat de DNA-inhoud weerspiegelt. In alle condities verscheen een stijging van het DAPI-signaal betrouwbaar vóór zichtbare toename in celaantal of veranderingen in zuurstofverbruik. Deze vroege waarschuwing toonde aan dat cellen hun DNA-replicatie en groei opvoerden lang voordat traditionele indicatoren een verschuiving zouden signaleren, waardoor in principe eerder aanpassingen in voeding of bedrijfscondities mogelijk zouden zijn. De methode legde ook vast hoe elke soort steady-state-groei bereikte en handhaafde bij verschillende stromingssnelheden en hoe culturen bij zeer hoge verdunning uitdunden maar verrijkt raakten met sneller groeiende cellen met hogere DNA-inhoud.
Wat werkte — en wat niet
In batchexperimenten (gesloten kolven of platen) benadrukte de EdU-gebaseerde kleurstof met succes pieken van DNA-replicatie, die kort na inoculatie piekten en vervolgens afnamen toen de culturen vertraagden. Het volgde het verschijnen en verdwijnen van subgroepen cellen met veel chromosoomkopieën, wat bevestigde dat het betrouwbaar actief replicerende cellen markeert. Echter, wanneer EdU continu in het medium van de kleine reactoren werd toegediend, vertraagde of verstoorde het vaak de groei. Bij S. rhizophila stopte de cultuur bijna; bij Bradyrhizobium verminderde het sterk het celaantal; en zelfs E. coli groeide langzamer en toonde replicatiesignalen alleen in de vroege uren. Het verhogen van de hoeveelheid fluorescerende kleurstof loste dit probleem niet op. De auteurs concluderen dat EdU bij continue blootstelling te groeiremmend en technisch te lastig is om als routine-replicatiemarker in industriële monitoring te dienen.
Gevolgen voor slimere bioreactoren
Ondanks de beperkingen van EdU bewees de dubbele-kleuringsworkflow dat geautomatiseerde online flowcytometrie rijke, tijdsopgeloste beelden van bacteriële fysiologie kan leveren. Cellen tellen en het DAPI-signaal volgen gaf een robuuste, directe maat voor biomassa en een vroege indicator van groeiveranderingen bij verschillende verdunningssnelheden. De geïntegreerde monsternemer–kleurer–cytometerketen werkte elk uur met minimale menselijke tussenkomst, en toonde aan dat dergelijke systemen in toekomstige productielijnen kunnen worden ingebed. Hoewel de specifieke replicatiekleurstof die hier getest is nog niet gereed is voor dagelijkse aansturing van bacteriefabrieken, kan hetzelfde geautomatiseerde raamwerk worden gecombineerd met andere fluorescerende markers. Op de lange termijn kan dit soort realtime, enkel-celmonitoring helpen om bioreactoren in hun optimale "sweet spot" te houden, waardoor opbrengst, stabiliteit en productkwaliteit voor een breed scala aan microbiële processen verbeteren.
Bronvermelding: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Trefwoorden: geautomatiseerde flowcytometrie, bacteriële bioreactoren, realtime bioprocesmonitoring, celcyclus en DNA-replicatie, industriële biotechnologie