Clear Sky Science · es
Un método automatizado de citometría de flujo con doble tinción para el seguimiento en tiempo real de bacterias en biorreactores continuos
Observar a los microbios en acción, en tiempo real
La biotecnología moderna depende de enormes cultivos bacterianos para producir desde fármacos hasta protectores de cultivos. Sin embargo, dentro de esos tanques espumosos resulta sorprendentemente difícil saber qué hacen los microbios en un momento dado. Este estudio presenta un sistema automatizado similar a un microscopio que puede observar células bacterianas individuales cada hora, revelando no solo cuántas hay, sino si están creciendo activamente y copiando su ADN. Esta visión en tiempo real podría hacer que la fermentación industrial sea más eficiente, fiable y fácil de controlar.

Por qué contar células no basta
En los fermentadores industriales, la densidad celular ayuda a decidir cuándo aportar más nutrientes, cuándo cosechar y cuál puede ser la productividad del proceso. Las herramientas tradicionales—como las lecturas de densidad óptica, las mediciones de peso seco o los sensores eléctricos—miden la turbidez o la masa global de un cultivo. Son útiles pero burdas: no distinguen células vivas de inactivas, pasan por alto diferencias de tamaño y forma, y no indican si las células se están preparando para dividirse. Como resultado, los responsables a menudo operan con información parcial, ajustando procesos en función de señales indirectas o retrasadas.
Una nueva ventana automatizada a la vida bacteriana
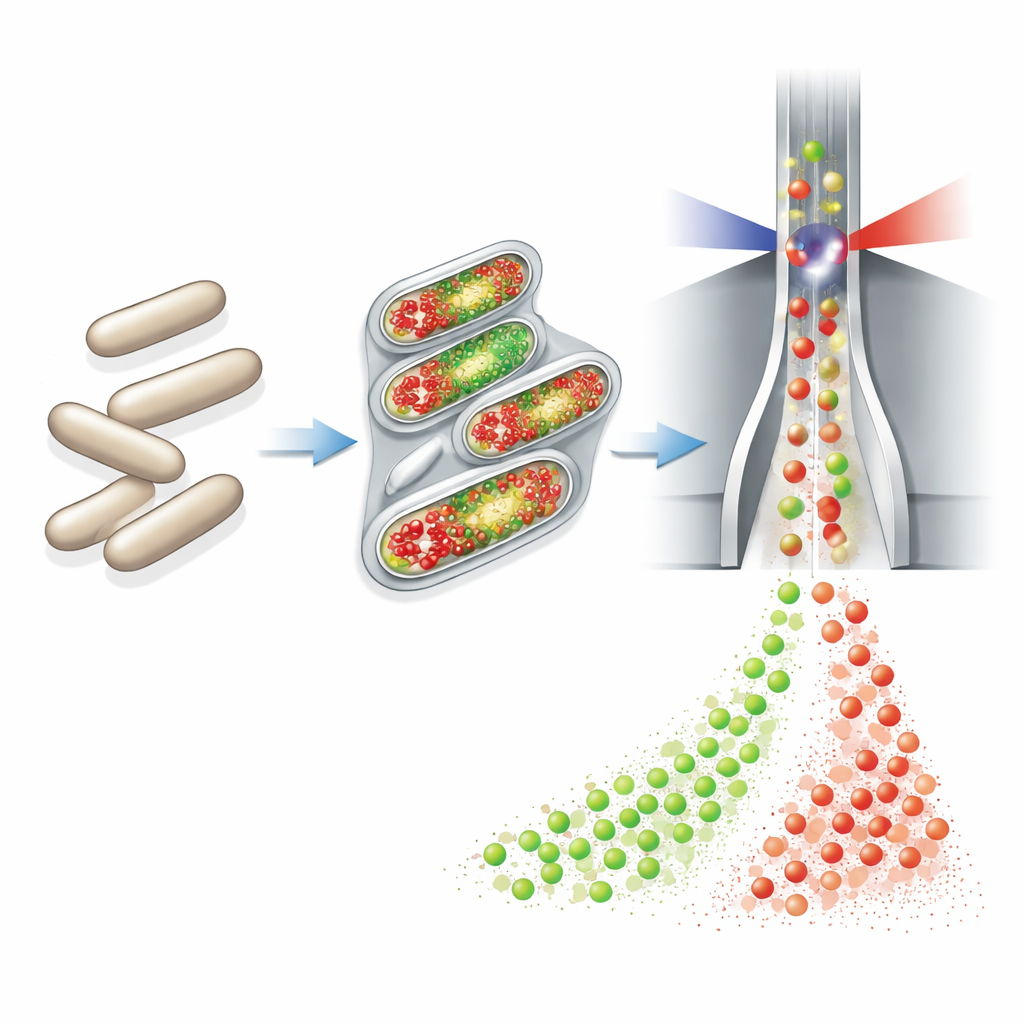
Los autores partieron de una tecnología llamada citometría de flujo, que mide rápidamente propiedades de miles de células individuales a medida que atraviesan un haz láser. Conectaron un dispositivo totalmente automatizado de muestreo y tinción a pequeños biorreactores continuos. Cada hora, este dispositivo tomaba un volumen mínimo de cultivo, fijaba y permeabilizaba químicamente las células, añadía dos tintes fluorescentes, diluía la muestra y la enviaba directamente al citómetro. Un tinte (DAPI) fluoresce en proporción a la cantidad de ADN de cada célula, funcionando como un indicador sensible del crecimiento celular y del número de copias del cromosoma. El segundo tinte, unido mediante una reacción "click" a un bloque de construcción del ADN llamado EdU, marca específicamente las células que están copiando su ADN: las que están a punto de dividirse.
Seguir el crecimiento bacteriano, célula a célula
El equipo probó este sistema con tres bacterias Gram negativas no patógenas: una cepa de Bradyrhizobium de suelo, la especie modelo Escherichia coli y la asociada a plantas Stenotrophomonas rhizophila. En cultivos continuos, variaron la velocidad de flujo del medio fresco a través de los reactores (la tasa de dilución) y dejaron funcionar el sistema automatizado. El citómetro informó tanto recuentos celulares como la señal media de DAPI por célula, que refleja el contenido de ADN. En distintas condiciones, un aumento en la señal de DAPI apareció de forma fiable antes de los incrementos visibles en el número de células o cambios en el consumo de oxígeno. Esta alerta temprana mostró que las células aumentaban la replicación del ADN y el crecimiento mucho antes de que los indicadores tradicionales detectaran un cambio, permitiendo, en principio, ajustes anticipados en la alimentación o en las condiciones de operación. El método también capturó cómo cada especie entraba y mantenía un crecimiento estable a distintas tasas de dilución y cómo, a diluciones muy altas, los cultivos se afinaban pero se enriquecían en células de crecimiento más rápido con mayor contenido de ADN.
Lo que funcionó—y lo que no
En experimentos por lotes (matrices cerradas en frascos o placas), el tinte basado en EdU resaltó con éxito pulsos de replicación del ADN, alcanzando un pico poco después de la inoculación y luego disminuyendo conforme los cultivos se desaceleraban. Permitió seguir la aparición y desaparición de subgrupos de células con muchas copias cromosómicas, confirmando que marca de forma fiable a las células que replican activamente. Sin embargo, cuando el EdU se suministró de forma continua en el medio de los pequeños reactores, con frecuencia ralentizó o perturbó el crecimiento. En S. rhizophila casi detuvo el cultivo; en Bradyrhizobium redujo drásticamente el número de células; e incluso E. coli creció más despacio y mostró señales de replicación solo en las primeras horas. Aumentar la cantidad de tinte fluorescente no solucionó el problema. Los autores concluyen que, bajo exposición continua, el EdU inhibe demasiado el crecimiento y resulta técnicamente problemático para servir como marcador de replicación de uso rutinario en el monitoreo industrial.
Implicaciones para biorreactores más inteligentes
A pesar de las limitaciones del EdU, el flujo de trabajo de doble tinción demostró que la citometría de flujo en línea y automatizada puede ofrecer imágenes ricas y temporales de la fisiología bacteriana. Contar células y seguir su señal de DAPI proporcionó una medida directa y robusta de la biomasa y un indicador temprano de cambios de crecimiento a distintas tasas de dilución. La cadena integrada muestreador–tinción–citómetro funcionó cada hora con mínima intervención humana, mostrando que estos sistemas pueden integrarse en futuras líneas de producción. Si bien el tinte de replicación concreto probado aquí aún no está listo para el control cotidiano de las fábricas bacterianas, el mismo marco automatizado puede emparejarse con otros marcadores fluorescentes. A largo plazo, este tipo de monitorización en tiempo real a nivel de célula única podría ayudar a mantener los biorreactores en su "punto óptimo", mejorando rendimientos, estabilidad y calidad del producto en una amplia gama de procesos microbianos.
Cita: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Palabras clave: citometría de flujo automatizada, biorreactores bacterianos, monitoreo de bioprocesos en tiempo real, ciclo celular y replicación del ADN, biotecnología industrial