Clear Sky Science · pt
Um método automatizado de citometria de fluxo com dupla coloração para monitoramento em tempo real de bactérias em biorreatores contínuos
Observando microrganismos trabalhando em tempo real
A biotecnologia moderna depende de grandes culturas de bactérias para produzir desde medicamentos até agentes de proteção de culturas. Ainda assim, dentro daqueles tanques efervescentes, é surpreendentemente difícil saber o que os microrganismos estão fazendo em um dado momento. Este estudo apresenta um sistema automatizado semelhante a um microscópio que pode observar células bacterianas individuais a cada hora, revelando não apenas quantas estão presentes, mas se elas estão ativamente crescendo e copiando seu DNA. Essa percepção em tempo real pode tornar a fermentação industrial mais eficiente, confiável e fácil de controlar.

Por que contar células não é suficiente
Em fermentadores industriais, a densidade celular ajuda a determinar quando fornecer mais nutrientes, quando colher e quão produtivo um processo pode ser. Ferramentas tradicionais — como leituras de densidade óptica, medidas de peso seco ou sensores elétricos — medem a turbidez ou a massa bruta da cultura. Elas são úteis, mas grosseiras: não distinguem células vivas de inativas, ignoram diferenças de tamanho e forma e não informam se as células estão se preparando para se dividir. Como resultado, os operadores frequentemente trabalham parcialmente às cegas, ajustando processos com base em sinais indiretos ou defasados.
Uma nova janela automatizada para a vida bacteriana
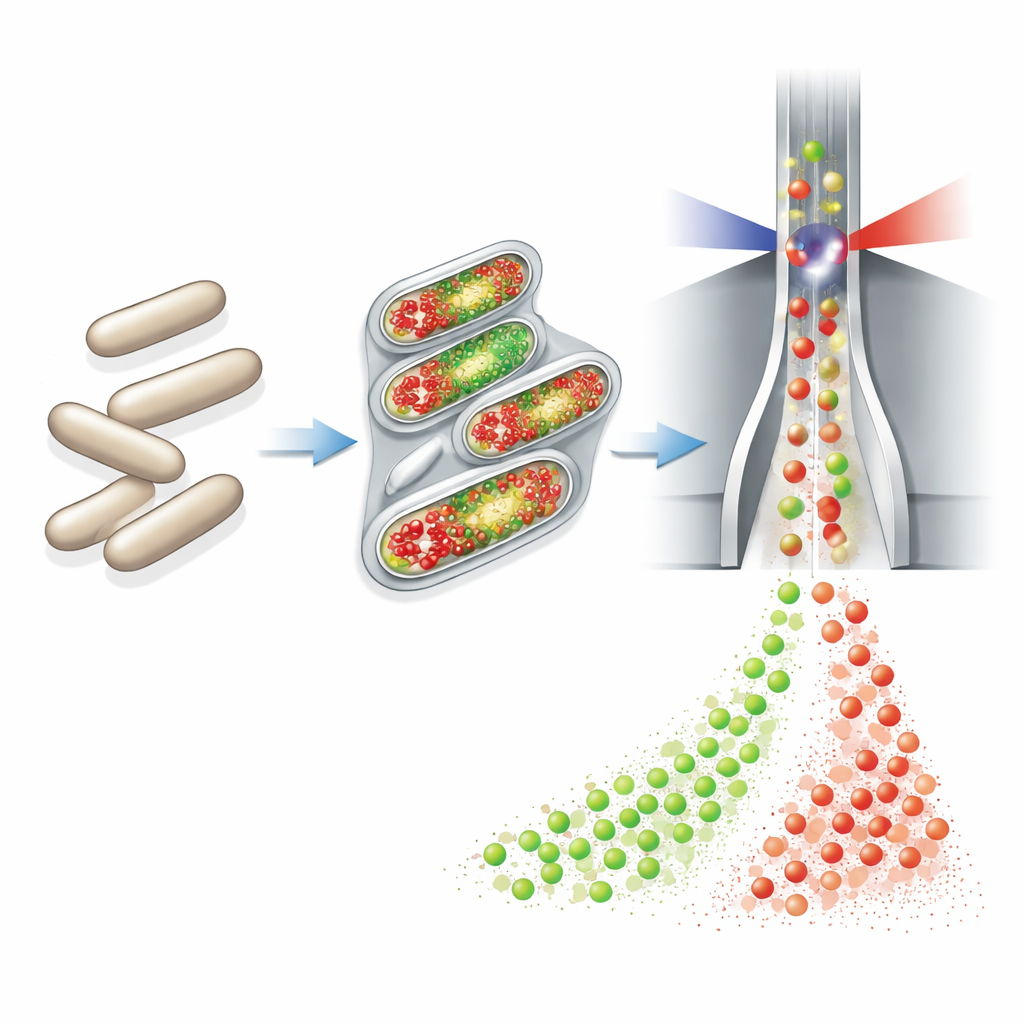
Os autores se apoiaram em uma tecnologia chamada citometria de fluxo, que mede rapidamente propriedades de milhares de células individuais à medida que passam por um feixe de laser. Eles conectaram um dispositivo totalmente automatizado de amostragem e coloração a pequenos biorreatores contínuos. A cada hora, esse dispositivo retirava um pequeno volume de cultura, fixava e permeabilizava quimicamente as células, adicionava dois corantes fluorescentes, diluía a amostra e a enviava diretamente ao citômetro. Um corante (DAPI) fluoresce em proporção à quantidade de DNA que cada célula contém, servindo como um indicador sensível de crescimento celular e número de cromossomos. O segundo corante, ligado por meio de uma reação “click” a um bloco de construção do DNA chamado EdU, marca especificamente as células que estão no ato de copiar seu DNA — aquelas prestes a se dividir.
Acompanhando o crescimento bacteriano, célula a célula
A equipe testou esse arranjo em três bactérias Gram-negativas não patogênicas: uma estirpe de Bradyrhizobium oriunda do solo, a espécie-modelo Escherichia coli e a associada a plantas Stenotrophomonas rhizophila. Em culturas contínuas, eles variaram a velocidade com que o meio fresco fluía pelos reatores (a taxa de diluição) e deixaram o sistema automatizado rodar. O citômetro reportou tanto contagens de células quanto o sinal médio de DAPI por célula, que reflete o conteúdo de DNA. Em diferentes condições, um aumento no sinal de DAPI surgiu de forma confiável antes de aumentos visíveis no número de células ou mudanças no consumo de oxigênio. Esse alerta precoce mostrou que as células estavam acelerando a replicação do DNA e o crescimento muito antes de indicadores tradicionais sinalizarem uma mudança, permitindo, em princípio, ajustes antecipados de alimentação ou das condições operacionais. O método também capturou como cada espécie entrou e manteve crescimento estável em diferentes taxas de fluxo e como, em diluição muito alta, as culturas se afinaram, mas ficaram enriquecidas em células de crescimento mais rápido com maior conteúdo de DNA.
O que funcionou — e o que não funcionou
Em experimentos em batelada (frascos ou placas fechadas), o corante à base de EdU destacou com sucesso picos de replicação do DNA, atingindo o máximo logo após a inoculação e depois diminuindo à medida que as culturas desaceleravam. Ele acompanhou o surgimento e o desaparecimento de subgrupos de células com muitas cópias de cromossomos, confirmando que marca de forma confiável células em replicação ativa. Porém, quando o EdU foi fornecido continuamente no meio dos pequenos reatores, frequentemente retardou ou perturbou o crescimento. Para S. rhizophila, quase paralisou a cultura; para Bradyrhizobium, reduziu fortemente o número de células; e mesmo E. coli cresceu mais lentamente e mostrou sinais de replicação apenas nas primeiras horas. Aumentar a quantidade do corante fluorescente não resolveu o problema. Os autores concluem que, sob exposição contínua, o EdU é excessivamente inibitório ao crescimento e tecnicamente exigente para servir como marcador rotineiro de replicação no monitoramento industrial.
Implicações para biorreatores mais inteligentes
Apesar das limitações do EdU, o fluxo de trabalho de dupla coloração demonstrou que a citometria de fluxo online automatizada pode fornecer retratos ricos e com resolução temporal da fisiologia bacteriana. Contar células e rastrear seu sinal de DAPI forneceu uma medida robusta e direta de biomassa e um indicador precoce de mudanças de crescimento em diferentes taxas de diluição. A cadeia integrada amostrador–coloridor–citômetro operou a cada hora com intervenção humana mínima, mostrando que esses sistemas podem ser integrados às linhas de produção futuras. Embora o corante de replicação específico testado aqui ainda não esteja pronto para o controle diário de fábricas bacterianas, a mesma estrutura automatizada pode ser combinada com outros marcadores fluorescentes. A longo prazo, esse tipo de monitoramento em tempo real e em nível de célula única pode ajudar a manter biorreatores em sua “zona ótima”, melhorando rendimentos, estabilidade e qualidade do produto para uma ampla gama de processos microbianos.
Citação: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Palavras-chave: citometria de fluxo automatizada, biorreatores bacterianos, monitoramento de bioprocessos em tempo real, ciclo celular e replicação do DNA, biotecnologia industrial