Clear Sky Science · it
Un metodo di citometria a flusso automatizzato a doppia colorazione per il monitoraggio in tempo reale dei batteri in bioreattori continui
Osservare i microbi al lavoro in tempo reale
La biotecnologia moderna si basa su grandi colture di batteri per produrre di tutto, dai farmaci agli agenti di protezione delle colture. Eppure, all’interno di quei serbatoi schiumosi, è sorprendentemente difficile sapere cosa stiano facendo i microrganismi in ogni singolo momento. Questo studio introduce un sistema automatizzato, simile a un microscopio, in grado di osservare singole cellule batteriche ogni ora, rivelando non solo quante ce ne sono, ma anche se stanno attivamente crescendo e replicando il loro DNA. Un simile accesso in tempo reale potrebbe rendere la fermentazione industriale più efficiente, affidabile e più semplice da controllare.

Perché contare le cellule non basta
Nei fermentatori industriali la densità cellulare aiuta a decidere quando integrare nutrienti, quando raccogliere il prodotto e quale sia la produttività del processo. Gli strumenti tradizionali—come le letture della densità ottica, le misure del peso secco o i sensori elettrici—misurano il torbido o la massa complessiva di una coltura. Sono utili ma grezzi: non distinguono le cellule vive da quelle inattive, trascurano differenze di dimensione e forma e non informano se le cellule si stanno preparando a dividersi. Di conseguenza, gli operatori spesso lavorano in parte alla cieca, regolando i processi sulla base di segnali ritardati o indiretti.
Una nuova finestra automatizzata sulla vita batterica
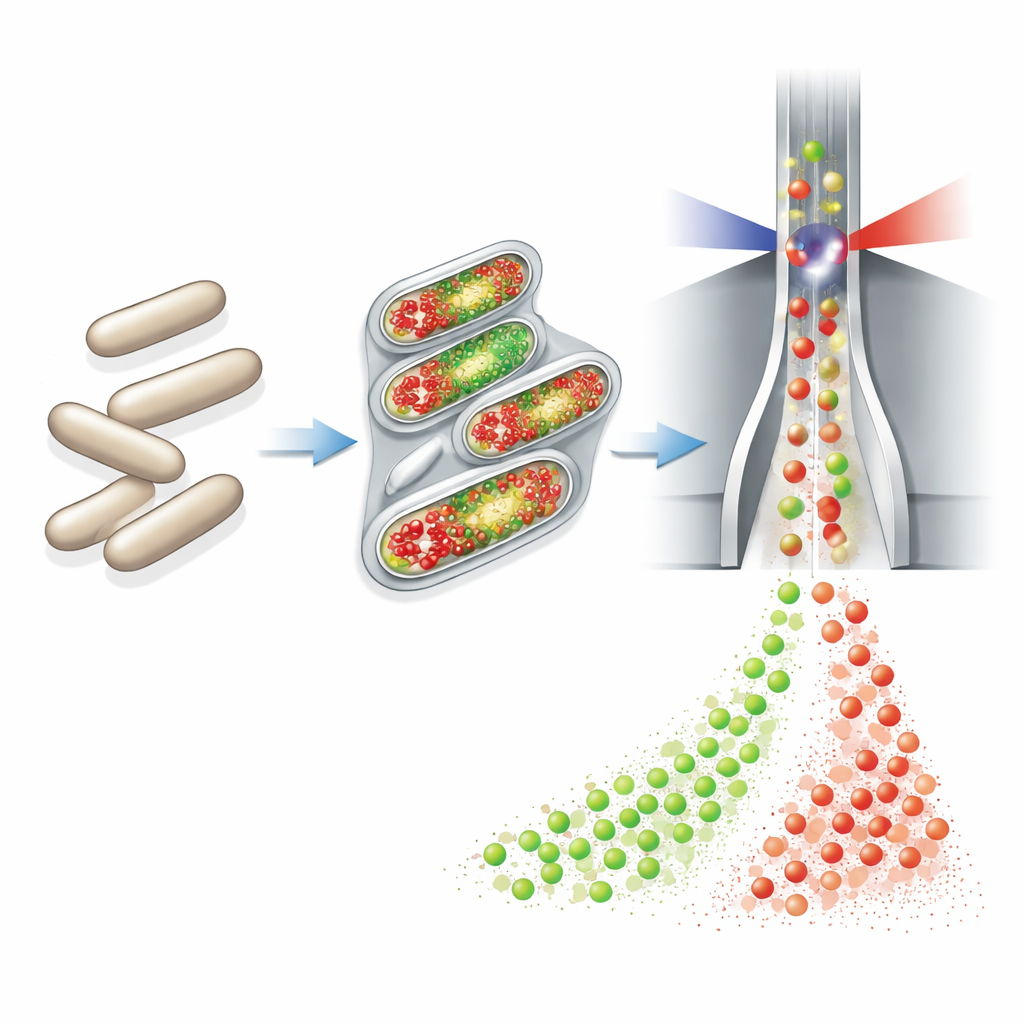
Gli autori hanno sfruttato una tecnologia chiamata citometria a flusso, che misura rapidamente le proprietà di migliaia di cellule individuali mentre passano davanti a un fascio laser. Hanno collegato un dispositivo completamente automatizzato di campionamento e colorazione a piccoli bioreattori continui. Ogni ora questo dispositivo prelevava un volume minuscolo di coltura, fissava e permeabilizzava chimicamente le cellule, aggiungeva due coloranti fluorescenti, diluiva il campione e lo inviava direttamente al citometro. Un colorante (DAPI) emette fluorescenza in proporzione alla quantità di DNA presente in ciascuna cellula, fungendo da indicatore sensibile della crescita cellulare e del numero di cromosomi. Il secondo colorante, legato tramite una reazione “click” a un mattoncino del DNA chiamato EdU, marca specificamente le cellule che stanno copiando il DNA—quindi quelle prossime alla divisione.
Seguire la crescita batterica, cellula per cellula
Il gruppo ha testato questa configurazione su tre batteri Gram-negativi non patogeni: un ceppo di Bradyrhizobium presente nel suolo, la specie modello Escherichia coli e lo Stenotrophomonas rhizophila associato alle piante. In colture continue hanno variato la velocità di rinnovo del mezzo (tasso di diluizione) e lasciato operare il sistema automatizzato. Il citometro ha riportato sia il numero di cellule sia il segnale medio di DAPI per cellula, che riflette il contenuto di DNA. In tutte le condizioni, un aumento del segnale DAPI è apparso in modo affidabile prima degli incrementi visibili nel conteggio cellulare o dei cambiamenti nel consumo di ossigeno. Questo allarme precoce ha mostrato che le cellule stavano intensificando la replicazione del DNA e la crescita molto prima che gli indicatori tradizionali segnalassero una variazione, permettendo, in linea di principio, aggiustamenti anticipati dell’alimentazione o delle condizioni operative. Il metodo ha anche catturato come ciascuna specie entrava e manteneva una crescita stabile a diversi tassi di diluizione e come, a diluizioni molto elevate, le colture si assottigliassero ma fossero arricchite in cellule a crescita più rapida con contenuto di DNA superiore.
Cosa ha funzionato—e cosa no
Negli esperimenti in batch (flaconi o piastre chiuse), il colorante basato su EdU ha evidenziato con successo picchi di replicazione del DNA, raggiungendo il massimo poco dopo l’inoculo e poi diminuendo con il rallentamento delle colture. Ha seguito l’apparizione e la scomparsa di sottogruppi di cellule con molte copie cromosomiche, confermando che marca in modo affidabile le cellule in replicazione attiva. Tuttavia, quando EdU è stato fornito continuamente nel mezzo dei piccoli reattori, spesso ha rallentato o perturbato la crescita. Per S. rhizophila ha quasi arrestato la coltura; per Bradyrhizobium ha ridotto fortemente il numero di cellule; e persino E. coli è cresciuto più lentamente mostrando segnali di replicazione solo nelle prime ore. Aumentare la quantità di colorante fluorescente non ha risolto il problema. Gli autori concludono che, sotto esposizione continua, l’EdU è troppo inibente per la crescita e tecnicamente problematico per essere utilizzato come marcatore di replicazione di routine nel monitoraggio industriale.
Implicazioni per bioreattori più intelligenti
Nonostante i limiti dell’EdU, il flusso di lavoro a doppia colorazione ha dimostrato che la citometria a flusso online automatizzata può fornire immagini ricche e risolte nel tempo della fisiologia batterica. Contare le cellule e monitorare il loro segnale DAPI ha dato una misura diretta e robusta della biomassa e un indicatore precoce di cambiamenti di crescita a diversi tassi di diluizione. La catena integrata campionatore–coloratore–citometro ha operato a cadenza oraria con intervento umano minimo, mostrando che tali sistemi possono essere integrati nelle linee di produzione future. Pur non essendo ancora pronto per il controllo quotidiano delle “fabbriche” batteriche il colorante di replicazione testato qui, lo stesso quadro automatizzato può essere abbinato ad altri marcatori fluorescenti. A lungo termine, questo tipo di monitoraggio in tempo reale a livello di singola cellula potrebbe aiutare a mantenere i bioreattori nel loro “punto dolce” ottimale, migliorando rese, stabilità e qualità del prodotto per un’ampia gamma di processi microbici.
Citazione: López-Gálvez, J., Schönfelder, E., Mayer, H. et al. A double-staining automated flow cytometry method for real-time monitoring of bacteria in continuous bioreactors. npj Syst Biol Appl 12, 47 (2026). https://doi.org/10.1038/s41540-026-00694-3
Parole chiave: citometria a flusso automatizzata, bioreattori batterici, monitoraggio in tempo reale dei bioprocessi, <keyword>biotecnologia industriale