Clear Sky Science · zh
使用神经网络的情境感知合成启动子设计实现了真核转录网络的重新接线
教会细胞新把戏
现代生物技术常常围绕一个简单问题:我们能否精确告诉细胞何时开启或关闭某个基因?这篇论文探讨了一种在面包酵母中实现该目标的新方法,利用人工智能重新设计被称为启动子的微小DNA开关。通过学习这些天然开关的布线方式,作者展示了计算机可以提出精确的编辑建议,使科学家能够将新的控制旋钮接入细胞的基因电路。
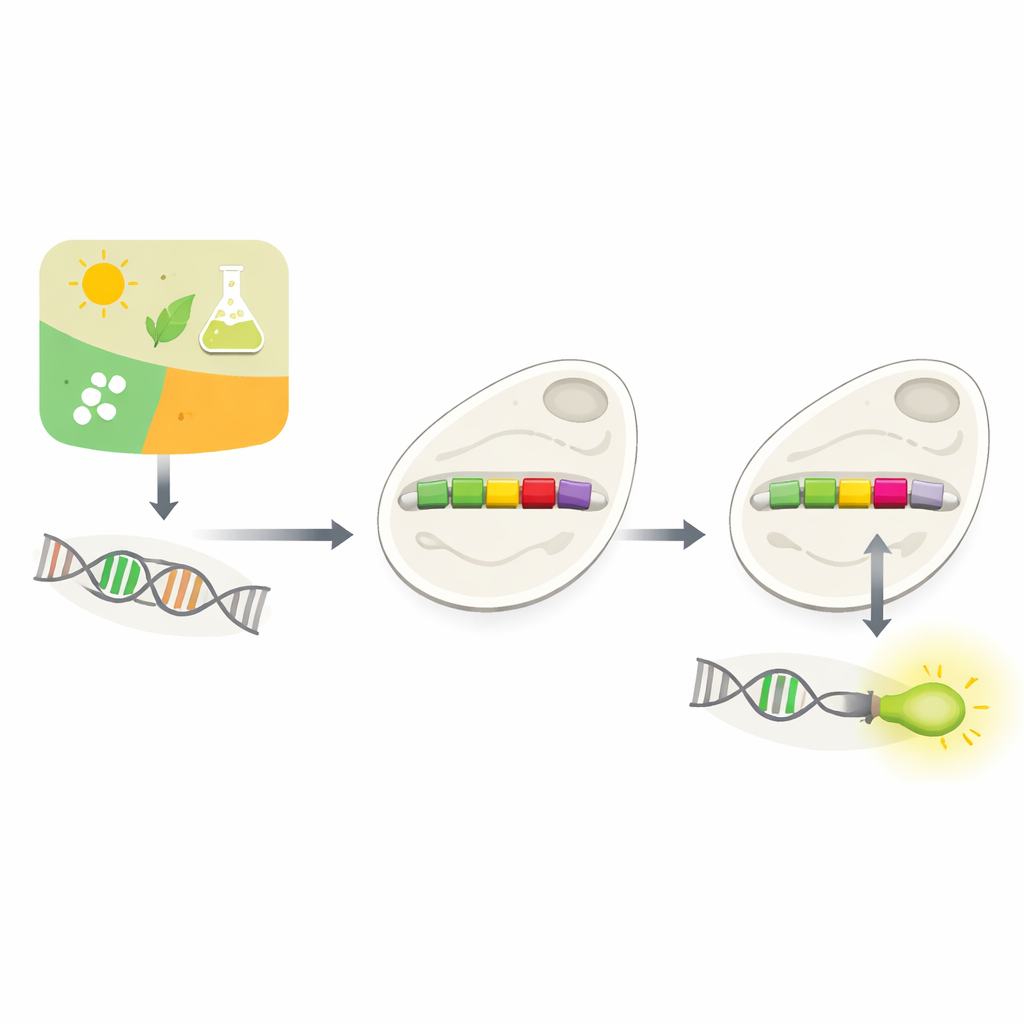
细胞如何决定使用哪些基因
每个细胞都必须不断决定使用哪些基因以及何时使用。其中很大一部分决策发生在启动子上——位于基因之前的短DNA片段。启动子像调光开关一样,响应来自环境或细胞内部的信号。生物学家长期以来一直试图构建定制启动子,以便随心控制基因——例如让酵母合成有价值的化学物质或感测毒素。但天然启动子结构复杂、依赖上下文,简单地在其中插入新的调控元件往往会破坏其功能。对大量可能设计进行实验验证既缓慢又昂贵。
让神经网络“读懂”DNA逻辑
作者构建了一个两步神经网络系统,从DNA中直接学习启动子的“语法”。首先,他们收集了来自100,000多个酵母亲缘物种的启动子序列,并训练了一个名为Place-Back的模型,使其在序列被打乱并部分替换后识别短DNA片段最初来自何处。由于模型必须仅靠上下文恢复正确位置,它学会了关于启动子哪些区域可以改变而不破坏核心功能的微妙模式。第二个模型Determiner则参考Place-Back的预测,决定新的调控元件应放置在何处以及应重写多大范围的DNA。
在计算机中设计可切换的启动子
有了这个系统,团队提出了一个实用问题:他们可以把已知的TetR抑制蛋白结合位点插入到真实酵母启动子的什么位置,使基因可以按需关闭?他们在计算上测试了酵母基因组中所有6,011个启动子,并生成了一个数千候选位点的排名列表,指出哪些位置可以“适配”新元件而不会破坏关键特征,例如转录起始的核心区域。模型经常偏好靠近这些核心区域但又避免直接损伤的位置,这表明它们学到了具有生物学意义的约束。
将AI设计的开关付诸实验
为验证计算机建议在活细胞中是否有效,研究者选择了四个原生酵母启动子,强弱各异,并按建议精确编辑每一个,在预测位置插入TetR结合位点。他们将这些启动子连接到亮光素酶报告基因,并在另一段DNA上引入TetR,以便新系统不会干扰酵母自身的调控。在存在TetR的条件下,四个设计中有三个表现出强烈抑制,其中一个实现了近乎完全的关闭——约98%的活性下降——且无需额外调试。模型未建议的替代插入位点经常使启动子失效或丧失响应能力,这强调了位置的重要性,以及神经网络确实找到了特定的“甜点位”。
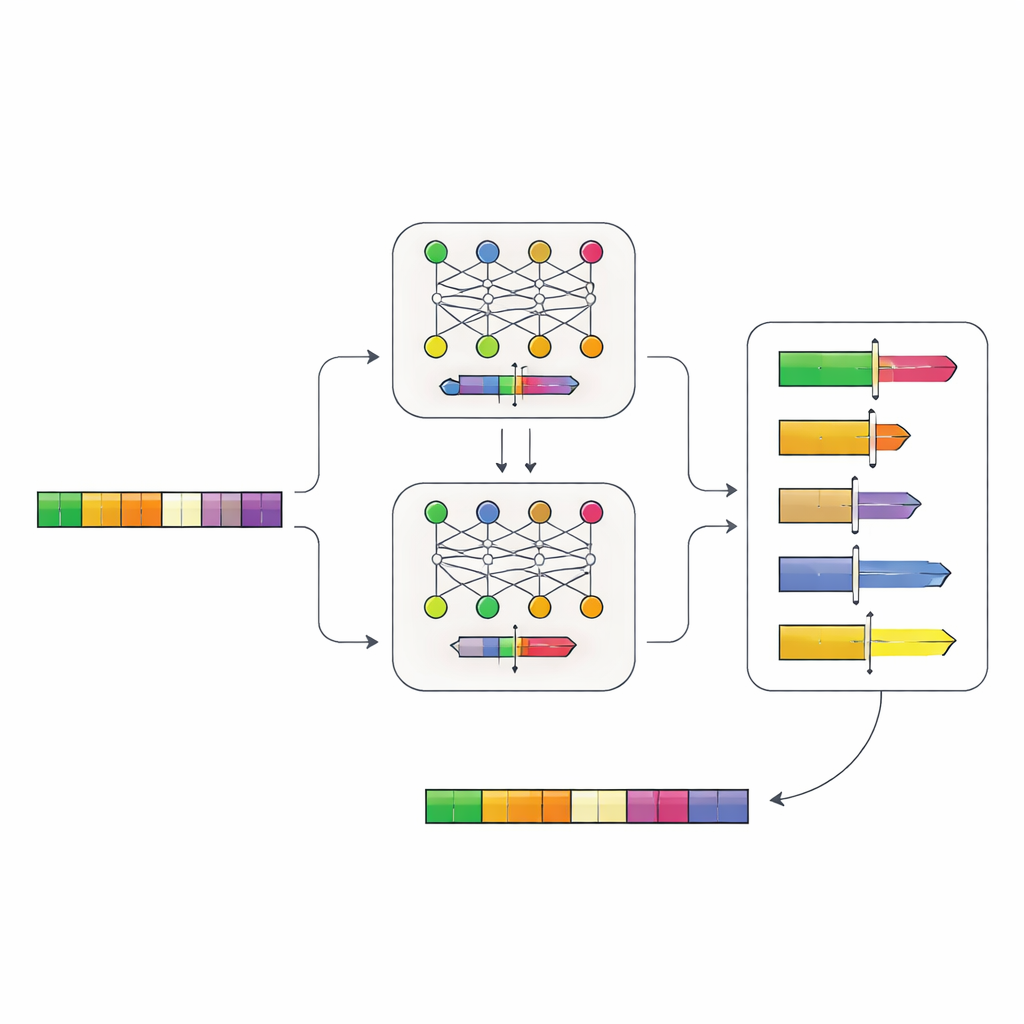
重新布线酵母的原生决策网络
随后,团队用同样的方法改造了酵母自身的调控网络,而不是添加一个人工附加系统。他们编辑了PCF11基因的启动子——该基因对生存至关重要——在其中插入了Mig1的结合位点,Mig1是遇到葡萄糖时会激活的天然抑制子。在测试实验中,重新设计的启动子表现如预期:在有葡萄糖时,PCF11活性下降超过一半;在无葡萄糖时,活性略高于正常水平。将该合成启动子换入酵母基因组后,细胞在低糖环境下生长几乎正常,但在高糖环境下达到的最大密度较低,表明该必需基因现在受新连接的条件性约束。
这对未来基因设计意味着什么
简而言之,这项工作表明神经网络可以学到足够多的基因调控“语言”,以提出智能、情境感知的DNA开关编辑建议。模型无需实验测量作为训练标签,就能指出可以安全插入新控制元件的位置,使基因对所选信号产生响应。包括成功改造必需基因控制在内的酵母实验证明了在许多生物中实现可扩展、可预测的调控DNA设计的路径。这可能加速为医学、农业和工业生物技术定制遗传程序的创建,同时揭示细胞如何自然组织其决策电路的新规则。
引用: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
关键词: 合成生物学, 基因调控, 神经网络, 启动子工程, 酵母