Clear Sky Science · ru
Проектирование контекстно-зависимых синтетических промоторов с помощью нейронных сетей позволяет перенастраивать транскрипционные сети эукариот
Обучая клетки новым трюкам
Современная биотехнология часто сводится к простому вопросу: можем ли мы точно указать клетке, когда включать или выключать ген? В этой работе исследуют новый способ сделать это в пекарских дрожжах, используя искусственный интеллект для переработки крошечных ДНК‑переключателей, называемых промоторами. Изучая, как устроены эти природные переключатели, авторы показывают, что компьютеры могут предлагать точные правки, позволяющие учёным встраивать новые органы управления в генетическую схему клетки.
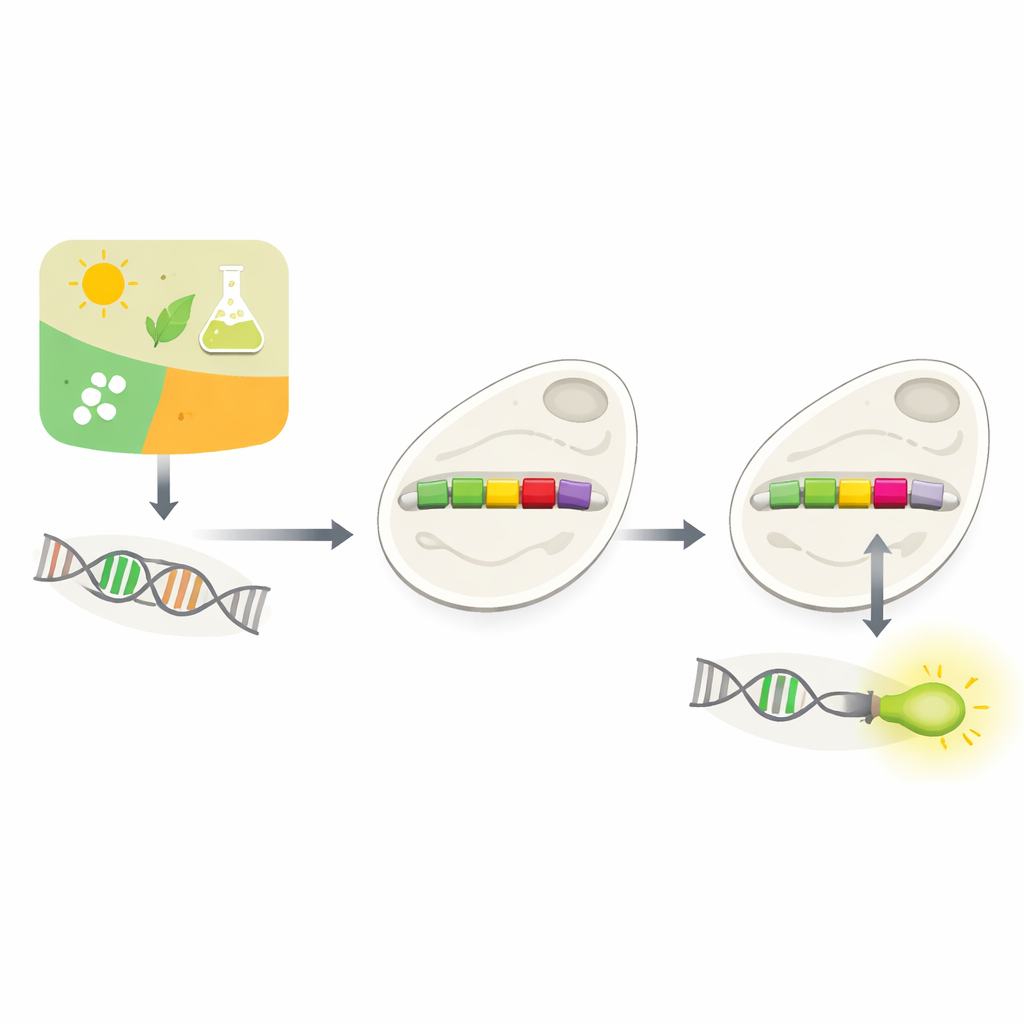
Как клетки решают, какие гены использовать
Каждая клетка постоянно решает, какие гены включать и когда. Большая часть этого принятия решений происходит на промоторах — коротких участках ДНК, расположенных прямо перед генами. Промоторы работают как регуляторы яркости, реагируя на сигналы из окружающей среды или внутри клетки. Биологи уже давно пытаются проектировать кастомные промоторы, чтобы управлять генами по желанию — например, чтобы заставить дрожжи синтезировать ценные химикаты или обнаруживать токсины. Но природные промоторы сложны и зависят от контекста, и простая вставка новых регуляторных элементов часто нарушает их функцию. Экспериментальная проверка множества возможных вариантов медленна и дорога.
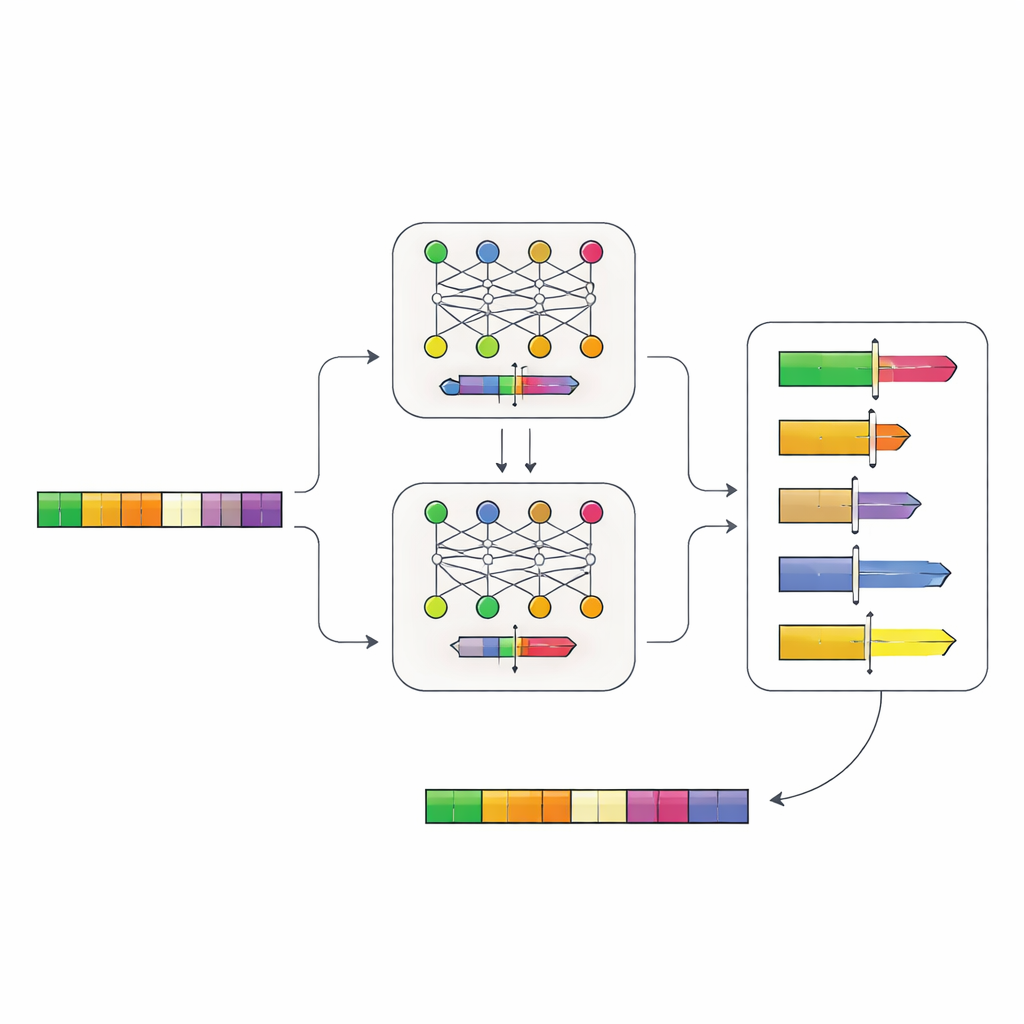
Позволив нейросетям читать логику ДНК
Авторы создали двухэтапную систему на основе нейронных сетей, которая изучает «грамматику» промоторов прямо из последовательностей ДНК. Сначала они собрали последовательности промоторов более чем 100 000 генов у родственников дрожжей и обучили модель под названием Place-Back определять, откуда исходно произошёл короткий фрагмент ДНК после того, как его перемешали и частично заменили. Поскольку модели приходилось восстанавливать правильное место, опираясь только на контекст, она выучила тонкие закономерности о том, какие области промотора можно менять, не нарушая его основной функции. Вторая модель, Determiner, затем анализировала предсказания Place-Back и решала, где следует разместить новый регуляторный элемент и какого размера участок ДНК нужно переписать.
Проектирование переключаемых промоторов в компьютере
Вооружённые этой системой, исследователи задали практический вопрос: куда можно вставить хорошо известную сайт связывания репрессора TetR в реальные промоторы дрожжей, чтобы гены можно было отключать по команде? Они виртуально проверили все 6 011 промоторов в геноме дрожжей и составили ранжированный список тысяч кандидатов, где новый элемент должен «вписаться», не нарушая ключевых особенностей, таких как ядро начала транскрипции. Модели часто отдавали предпочтение участкам, близким к этим ключевым регионам, но при этом избегали прямого повреждения, что говорит о том, что они выучили биологически значимые ограничения.
Проверка переключателей, спроектированных ИИ
Чтобы выяснить, сработают ли предложения компьютера в живых клетках, исследователи выбрали четыре нативных промотора дрожжей с разной силой и отредактировали каждый точно так, как рекомендовала модель, вставив сайт связывания TetR в предсказанную позицию. Они присоединили эти промоторы к яркому люциферазному репортеру и ввели TetR на отдельном фрагменте ДНК, чтобы новая система не мешала собственной регуляции дрожжей. В присутствии TetR три из четырёх конструкций показали сильную репрессию, а одна достигла почти полного выключения — примерно 98% снижения активности — без дополнительной настройки. Альтернативные места вставки, не предложенные моделью, часто нарушали работу промотора или уничтожали его способность отвечать, подчёркивая, что расположение имеет значение и что нейронная сеть выявляла конкретные «сладкие точки».
Перенастройка родной системы принятия решений у дрожжей
Затем команда использовала тот же подход для изменения собственной регуляторной сети дрожжей, а не искусственной надстройки. Они отредактировали промотор PCF11, гена, необходимого для выживания, вставив сайт связывания Mig1 — естественного репрессора, активного в присутствии глюкозы. В тестовых анализах переработанный промотор вел себя как задумано: при наличии глюкозы активность PCF11 падала более чем вдвое; при отсутствии глюкозы активность была немного выше нормы. После замены этого синтетического промотора в геноме дрожжей клетки росли почти нормально при низком содержании сахара, но достигали меньшей максимальной плотности при высоком содержании, показав, что теперь жизненно важный ген условно ограничен новой связью.
Что это значит для будущего проектирования генетики
Проще говоря, эта работа демонстрирует, что нейронные сети могут выучить достаточно о «языке» генетического контроля, чтобы предлагать умные, контекстно‑зависимые правки ДНК‑переключателей. Не требуя экспериментальных измерений в качестве обучающих меток, модели указывают места, где новые регуляторные элементы можно безопасно вставлять, чтобы гены стали отзывчивыми на выбранные сигналы. Успешные тесты на дрожжах, включая перенастройку контроля над жизненно важным геномом, открывают путь к масштабируемому, предсказуемому проектированию регуляторной ДНК во множестве организмов. Это может ускорить создание индивидуальных генетических программ для медицины, сельского хозяйства и промышленной биотехнологии, а также раскрыть новые правила о том, как клетки организуют собственные схемы принятия решений.
Цитирование: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Ключевые слова: синтетическая биология, регуляция генов, нейронные сети, инжиниринг промоторов, дрожжи