Clear Sky Science · de
Kontextbewusste Gestaltung synthetischer Promotoren mittels neuronaler Netze ermöglicht das Umlernen eukaryotischer Transkriptionsnetzwerke
Zellen neue Fähigkeiten beibringen
Moderne Biotechnologie dreht sich oft um eine einfache Frage: Können wir einer Zelle genau sagen, wann ein Gen ein- oder ausgeschaltet werden soll? Diese Arbeit untersucht einen neuen Weg, dies in Bäckerhefe zu erreichen, indem künstliche Intelligenz winzige DNA-Schalter, sogenannte Promotoren, neu gestaltet. Indem die Autoren lernen lassen, wie diese natürlichen Schalter verdrahtet sind, zeigen sie, dass Computer präzise Änderungen vorschlagen können, mit denen Wissenschaftler neue Steuerknöpfe in die genetische Schaltung der Zelle einbauen können.
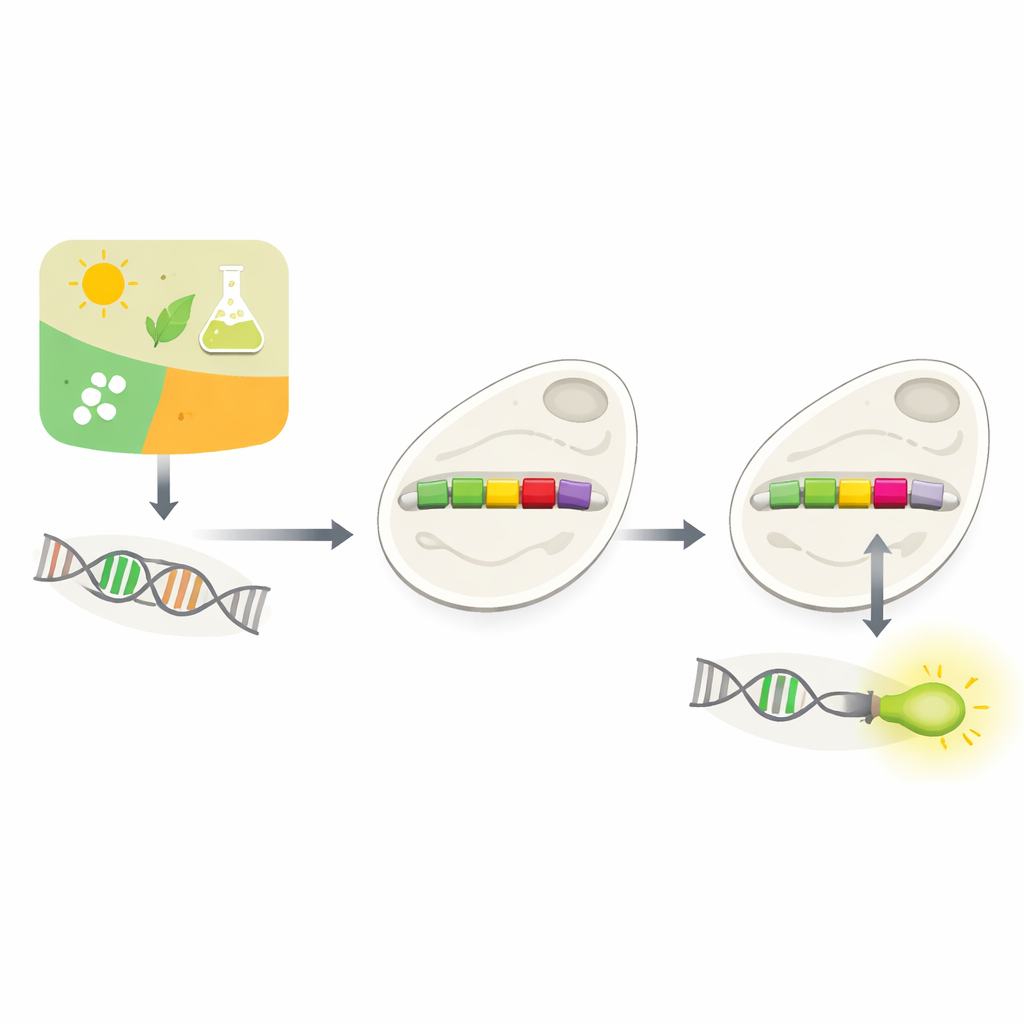
Wie Zellen entscheiden, welche Gene sie nutzen
Jede Zelle muss ständig entscheiden, welche Gene sie nutzt und wann. Ein Großteil dieser Entscheidungsfindung findet an Promotoren statt, kurzen DNA-Abschnitten unmittelbar vor Genen. Promotoren wirken wie Dimmer-Schalter und reagieren auf Signale aus der Umwelt oder dem Inneren der Zelle. Biologen versuchen seit langem, maßgeschneiderte Promotoren zu bauen, um Gene willkürlich steuern zu können — zum Beispiel um Hefen wertvolle Chemikalien produzieren zu lassen oder um Gifte zu detektieren. Natürliche Promotoren sind jedoch komplex und kontextabhängig, und das einfache Einfügen neuer Kontrollelemente zerstört oft ihre Funktion. Experimentelle Tests vieler möglicher Designs sind langsam und teuer.
Neuronale Netze die DNA-Logik lesen lassen
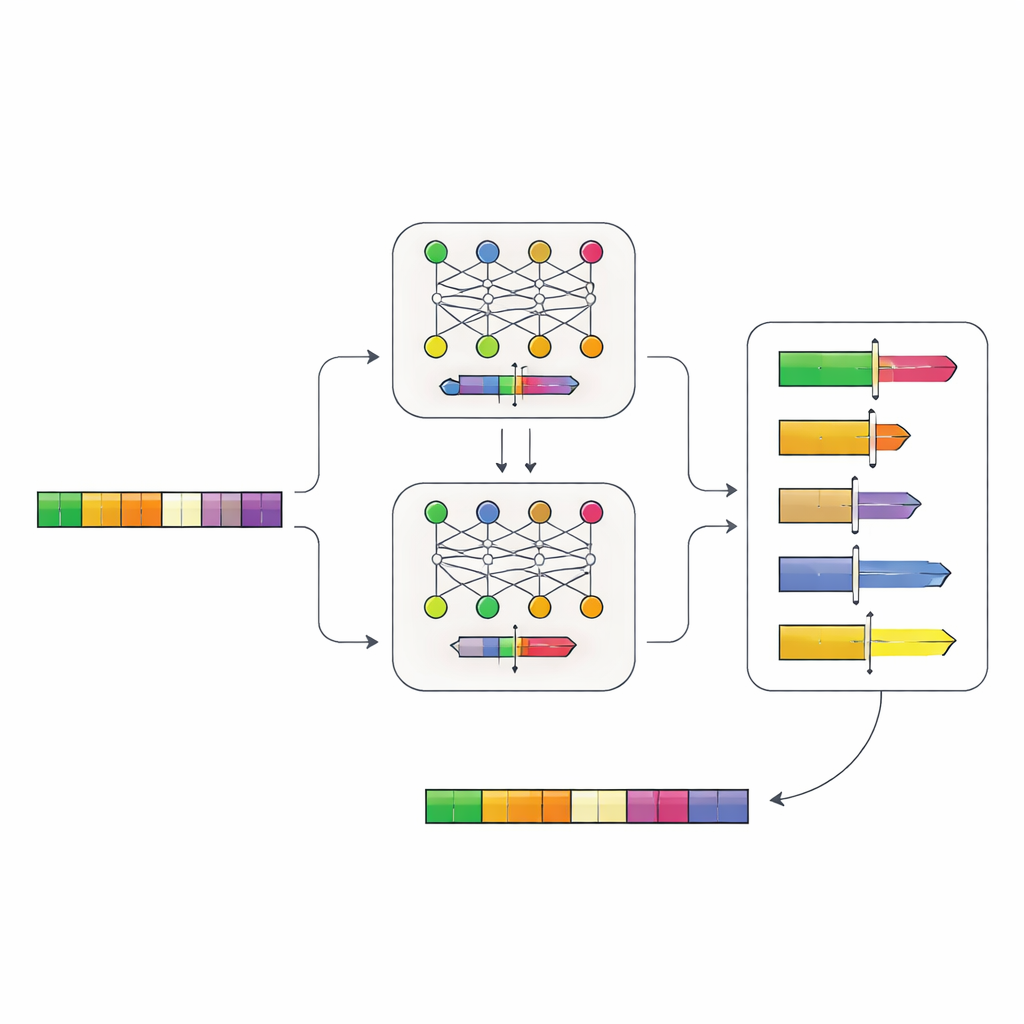
Die Autoren entwickelten ein zweistufiges System aus neuronalen Netzen, das die „Grammatik“ von Promotoren direkt aus der DNA erlernt. Zunächst sammelten sie Promotorsequenzen von mehr als 100.000 Genen aus Hefeverwandten und trainierten ein Modell namens Place-Back darauf, zu erkennen, wo ein kurzer DNA-Abschnitt ursprünglich herstammte, nachdem er verwürfelt und teilweise ersetzt worden war. Weil das Modell die richtige Stelle allein aus dem Kontext rekonstruieren musste, lernte es subtile Muster darüber, welche Regionen eines Promotors verändert werden können, ohne seine Kernfunktion zu stören. Ein zweites Modell, der Determiner, betrachtete dann Place-Backs Vorhersagen und entschied sowohl, wo ein neues Kontrollelement platziert werden sollte, als auch wie groß der umzuschreibende DNA-Bereich sein sollte.
Schaltbare Promotoren in silico entwerfen
Mit diesem System stellte das Team eine praktische Frage: Wo könnten sie eine bekannte Bindungsstelle für das Repressorprotein TetR in echte Hefepromotoren einfügen, sodass Gene auf Befehl abgeschaltet werden können? Sie testeten virtuell alle 6.011 Promotoren des Hefegenoms und erzeugten eine Rangliste von Tausenden Kandidaten, an denen das neue Element „passen“ sollte, ohne essentielle Merkmale wie den Kernstartbereich, an dem die Transkription beginnt, zu stören. Die Modelle bevorzugten oft Stellen nahe diesen Kernregionen, vermieden dabei aber direkte Schäden — ein Hinweis darauf, dass sie biologisch sinnvolle Beschränkungen gelernt hatten.
KI-entworfene Schalter in der Praxis testen
Um zu prüfen, ob die Vorschläge des Computers in lebenden Zellen funktionieren, wählten die Forscher vier native Hefepromotoren mit unterschiedlichen Stärken aus und bearbeiteten jeden exakt wie empfohlen, indem sie die TetR-Bindungsstelle an der vorhergesagten Position einfügten. Sie koppelten diese Promotoren an einen hellen Luciferase-Reporter und brachten TetR auf einem separaten DNA-Fragment ein, damit das neue System die eigene Regulation der Hefe nicht stört. In Gegenwart von TetR zeigten drei der vier Designs starke Repression, und eines erreichte nahezu vollständige Abschaltung — etwa 98 % Reduktion der Aktivität — ohne weitere Feinabstimmung. Alternative Einfügestellen, die nicht vom Modell vorgeschlagen wurden, beeinträchtigten den Promotor häufig oder zerstörten seine Reaktionsfähigkeit, was unterstreicht, dass die Platzierung entscheidend ist und das neuronale Netz spezifische „Sweet Spots“ identifizierte.
Die native Entscheidungsfindung der Hefe umlenken
Das Team nutzte denselben Ansatz anschließend, um das eigene Regulationsnetzwerk der Hefe zu verändern, statt ein künstliches Zusatzsystem einzubauen. Sie bearbeiteten den Promotor von PCF11, einem für das Überleben essentiellen Gen, und fügten eine Bindungsstelle für Mig1 ein, einen natürlichen Repressor, der in Gegenwart von Glukose aktiv wird. In Tests verhielt sich der neu gestaltete Promotor wie beabsichtigt: Bei Glukosezufuhr sank die PCF11-Aktivität um mehr als die Hälfte; bei fehlender Glukose war die Aktivität leicht erhöht gegenüber dem Normalzustand. Nachdem dieser synthetische Promotor ins Hefegenom eingebaut wurde, wuchsen die Zellen bei niedrigem Zucker fast normal, erreichten aber bei hohem Zucker eine geringere maximale Dichte, was zeigt, dass das essentielle Gen nun konditional durch die neue Verbindung eingeschränkt ist.
Was das für zukünftiges genetisches Design bedeutet
Vereinfacht zeigt diese Arbeit, dass neuronale Netze genug über die „Sprache“ der Genkontrolle lernen können, um intelligente, kontextbewusste Änderungen an DNA-Schaltern vorzuschlagen. Ohne experimentelle Messungen als Trainingslabels weisen die Modelle auf Stellen hin, an denen neue Kontrollelemente sicher eingefügt werden können, damit Gene auf gewählte Signale reagieren. Die erfolgreichen Tests in Hefe, einschließlich der Umverdrahtung der Kontrolle eines essentiellen Gens, deuten auf einen Weg zu skalierbarer, vorhersagbarer Gestaltung regulatorischer DNA in vielen Organismen hin. Das könnte die Entwicklung maßgeschneiderter genetischer Programme für Medizin, Landwirtschaft und industrielle Biotechnologie beschleunigen und gleichzeitig neue Regeln darüber offenlegen, wie Zellen ihre eigenen Entscheidungsnetzwerke organisieren.
Zitation: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Schlüsselwörter: synthetische Biologie, Genregulation, neuronale Netze, Promotor-Engineering, Hefe