Clear Sky Science · pt
Design de promotores sintéticos dependentes de contexto usando redes neurais possibilita a reconfiguração de redes de transcrição eucarióticas
Ensinando Novas Habilidades às Células
A biotecnologia moderna frequentemente se apoia numa pergunta simples: podemos dizer a uma célula exatamente quando ligar ou desligar um gene? Este artigo explora uma nova forma de fazer isso na levedura comum (Saccharomyces cerevisiae), usando inteligência artificial para redesenhar pequenos interruptores de DNA chamados promotores. Ao aprender como esses interruptores naturais são estruturados, os autores mostram que computadores podem propor edições precisas que permitem aos cientistas conectar novos controles à circuitaria genética da célula.
Como as Células Decidem Quais Genes Usar
Cada célula precisa constantemente decidir quais genes usar, e quando. Grande parte dessa tomada de decisão ocorre nos promotores, trechos curtos de DNA que ficam imediatamente antes dos genes. Promotores agem como reguladores de intensidade, respondendo a sinais do ambiente ou do próprio interior da célula. Biólogos há muito tentam construir promotores personalizados para controlar genes à vontade — por exemplo, para fazer leveduras produzirem compostos valiosos ou detectarem toxinas. Mas promotores naturais são complexos e dependentes do contexto, e simplesmente inserir novos elementos de controle frequentemente prejudica sua função. Testar experimentalmente muitos designs possíveis é lento e caro.
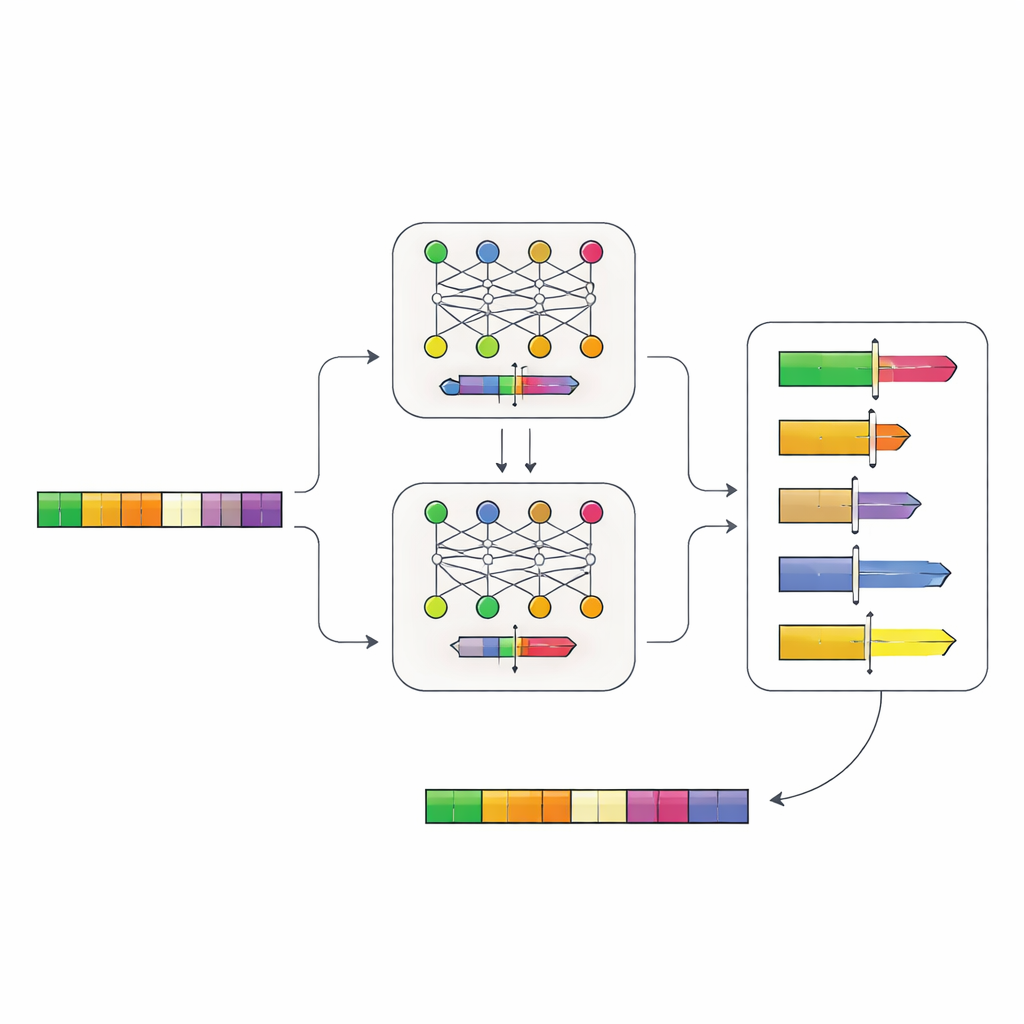
Deixando Redes Neurais Lerem a Lógica do DNA
Os autores construíram um sistema de redes neurais em duas etapas que aprende a “gramática” dos promotores diretamente a partir do DNA. Primeiro, coletaram sequências de promotores de mais de 100.000 genes em parentes das leveduras e treinaram um modelo, chamado Place-Back, para reconhecer de onde um pequeno segmento de DNA originalmente vinha depois de ele ter sido embaralhado e parcialmente substituído. Como o modelo precisava recuperar o local correto apenas a partir do contexto, ele aprendeu padrões sutis sobre quais regiões de um promotor podem ser alteradas sem perturbar sua função central. Um segundo modelo, o Determiner, então examinou as previsões do Place-Back e decidiu onde um novo elemento regulatório deveria ir e qual extensão de DNA deveria ser reescrita.
Projetando Promotores com Comutação In Silico
Com esse sistema, a equipe fez uma pergunta prática: onde poderiam inserir um sítio de ligação bem conhecido para a proteína represora TetR em promotores reais de levedura, de modo que genes pudessem ser desligados sob comando? Eles testaram virtualmente todos os 6.011 promotores do genoma de levedura e produziram uma lista ranqueada de milhares de candidatos onde o novo elemento deveria “encaixar” sem perturbar características essenciais, como a região central de início onde a transcrição começa. Os modelos frequentemente favoreceram sítios próximos a essas regiões centrais, ao mesmo tempo evitando danos diretos, sugerindo que haviam aprendido restrições biologicamente significativas.
Testando Interruptores Projetados por IA
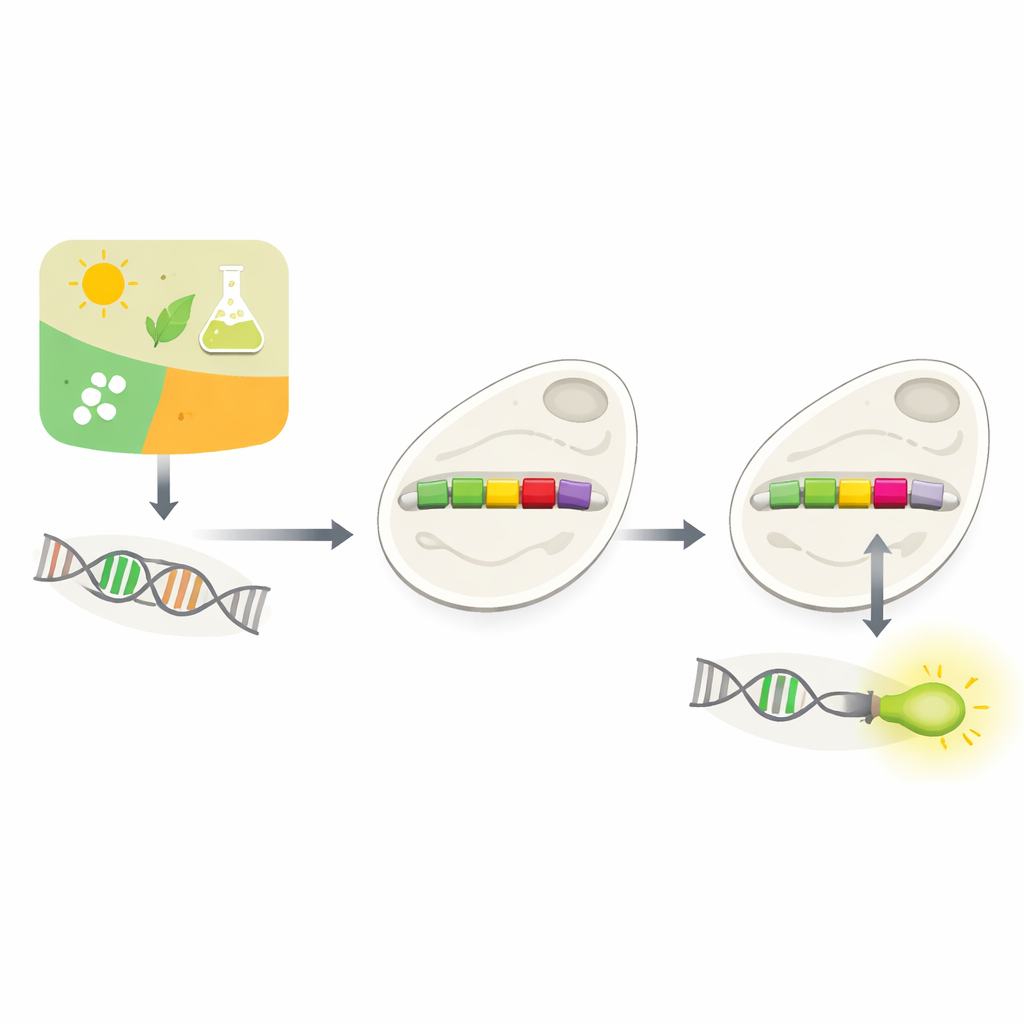
Para verificar se as sugestões do computador funcionavam em células vivas, os pesquisadores escolheram quatro promotores nativos de levedura com diferentes forças e editaram cada um exatamente como recomendado, inserindo o sítio de ligação TetR na localização prevista. Eles conectaram esses promotores a um reportador brilhante de luciferase e introduziram TetR em um fragmento de DNA separado, para que o novo sistema não interferisse na regulação própria da levedura. Na presença de TetR, três dos quatro designs mostraram forte repressão, e um alcançou quase desligamento completo — cerca de 98% de redução na atividade — sem qualquer ajuste adicional. Locais de inserção alternativos não sugeridos pelo modelo frequentemente prejudicaram o promotor ou destruíram sua capacidade de responder, ressaltando que a posição importa e que a rede neural estava identificando “pontos ideais” específicos.
Reconfigurando a Tomada de Decisão Nativa da Levedura
A equipe então usou a mesma abordagem para alterar a própria rede regulatória da levedura, em vez de um sistema artificial adicional. Eles editaram o promotor de PCF11, um gene essencial para a sobrevivência, para inserir um sítio de ligação para Mig1, um represso natural que se torna ativo na presença de glicose. Em ensaios de teste, o promotor redesenhado se comportou como previsto: quando glicose estava presente, a atividade de PCF11 caiu em mais da metade; quando a glicose estava ausente, a atividade ficou ligeiramente acima do normal. Após substituir esse promotor sintético no genoma da levedura, as células cresceram quase normalmente em baixa concentração de açúcar, mas atingiram uma densidade máxima menor em alto açúcar, mostrando que o gene essencial agora ficou condicionalmente restringido pela nova conexão.
O Que Isso Significa Para o Futuro do Projeto Genético
Em termos simples, este trabalho mostra que redes neurais podem aprender o suficiente sobre a “linguagem” do controle gênico para sugerir edições inteligentes e conscientes do contexto em interruptores de DNA. Sem precisar de medições experimentais como rótulos de treino, os modelos indicam pontos onde novos elementos de controle podem ser inseridos com segurança para que genes passem a responder a sinais escolhidos. Os testes bem-sucedidos em levedura, incluindo a reconfiguração do controle de um gene essencial, apontam para um caminho em direção ao projeto escalável e preditivo de DNA regulatório em muitos organismos. Isso pode acelerar a criação de programas genéticos sob medida para medicina, agricultura e biotecnologia industrial, ao mesmo tempo em que revela novas regras sobre como as células organizam naturalmente seus próprios circuitos de tomada de decisão.
Citação: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Palavras-chave: biologia sintética, regulação gênica, redes neurais, engenharia de promotores, levedura