Clear Sky Science · nl
Contextbewuste ontwerp van synthetische promotors met neurale netwerken maakt het herbedraden van eukaryotische transcriptienetwerken mogelijk
Cellen nieuwe trucs leren
Moderne biotechnologie draait vaak om een eenvoudige vraag: kunnen we de cel precies vertellen wanneer een gen aan of uit moet staan? Dit artikel onderzoekt een nieuwe manier om dat in bakkersgist te doen, waarbij kunstmatige intelligentie wordt gebruikt om kleine DNA-schakelaars, promotoren genoemd, te herontwerpen. Door te leren hoe deze natuurlijke schakelaars zijn bedraad, laten de auteurs zien dat computers precieze aanpassingen kunnen voorstellen waarmee wetenschappers nieuwe regelknoppen in de genetische schakeling van de cel kunnen plaatsen.
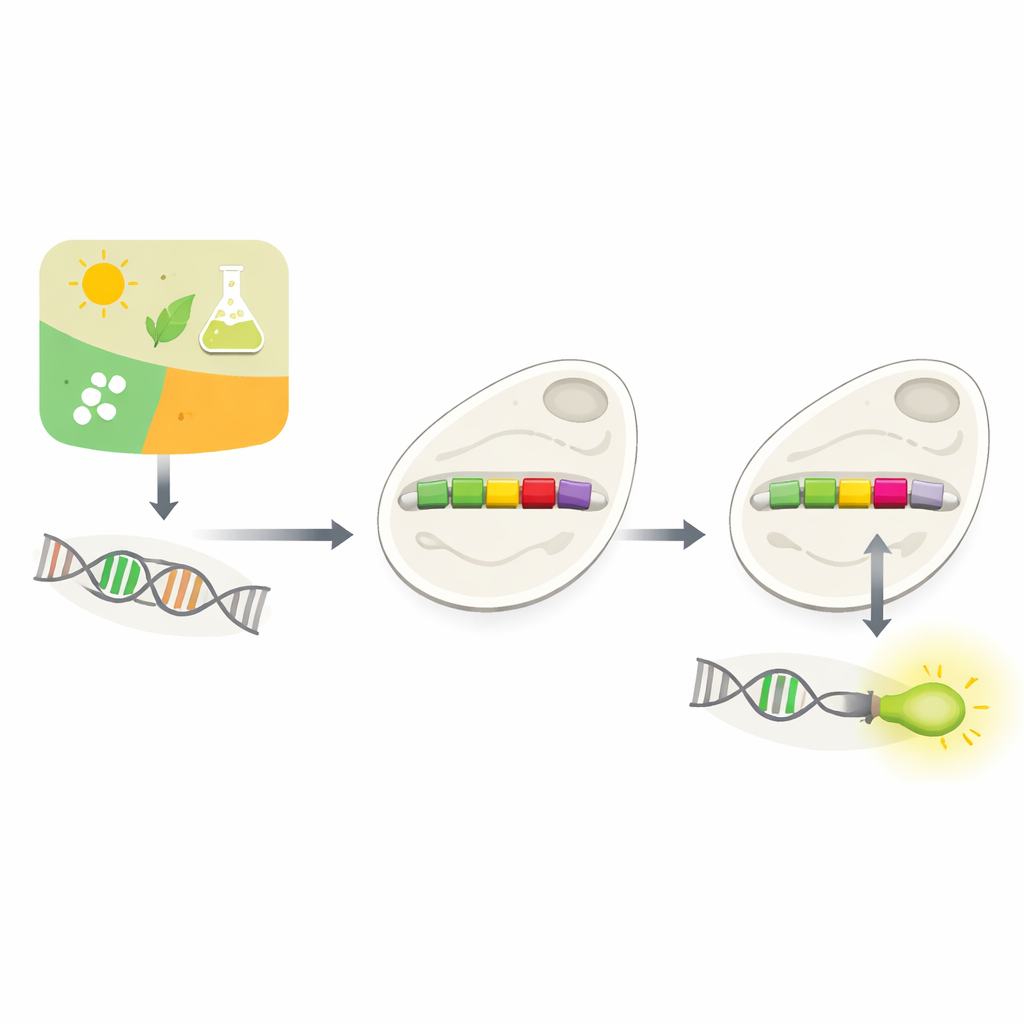
Hoe cellen beslissen welke genen ze gebruiken
Elke cel moet voortdurend beslissen welke genen te gebruiken en wanneer. Een groot deel van die besluitvorming vindt plaats bij promotoren, korte DNA-streken die direct voor genen liggen. Promotoren werken als dimmers en reageren op signalen uit de omgeving of uit de cel zelf. Biologen proberen al lange tijd op maat gemaakte promotoren te bouwen zodat ze genen naar believen kunnen aansturen—bijvoorbeeld om gist waardevolle chemicaliën te laten produceren of om toxines te detecteren. Maar natuurlijke promotoren zijn complex en contextafhankelijk, en het zomaar toevoegen van nieuwe controle-elementen breekt vaak hun functie. Experimenteel veel mogelijke ontwerpen testen is traag en duur.
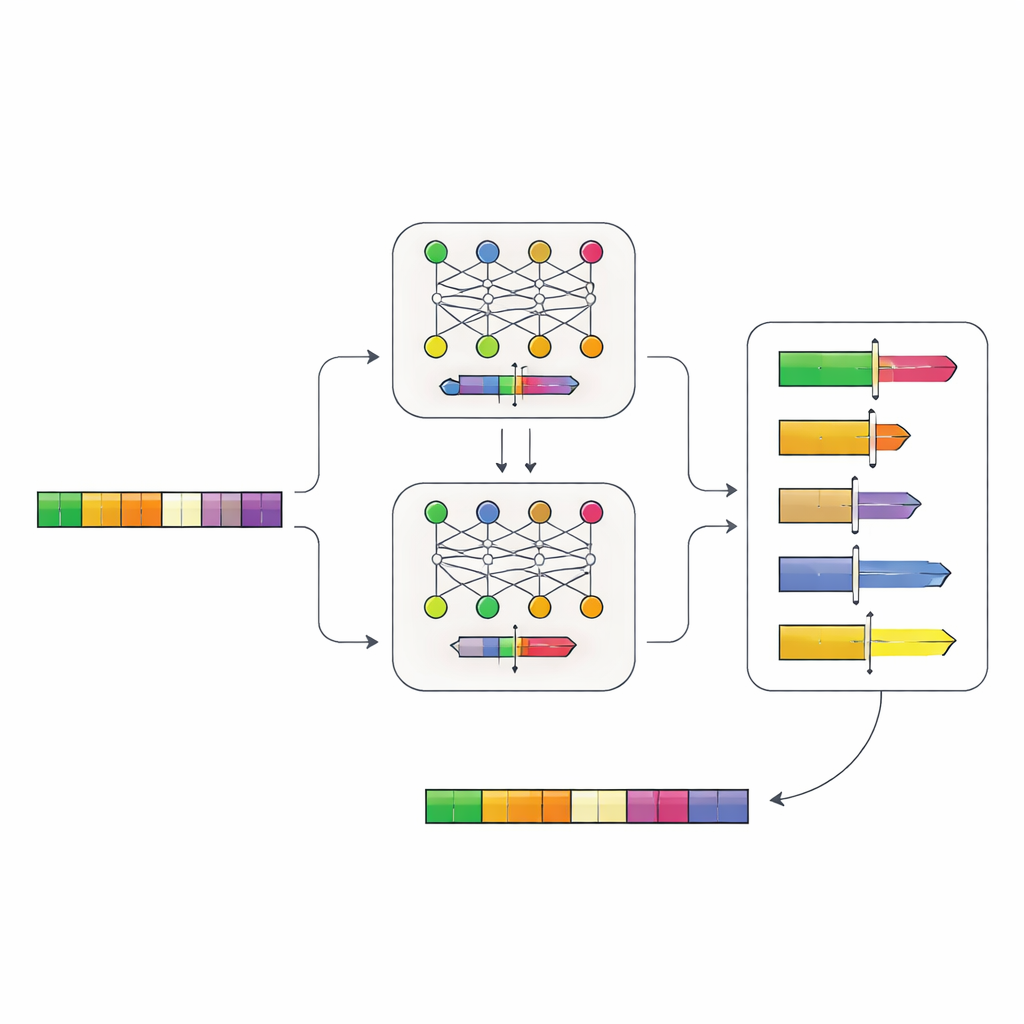
Neurale netwerken DNA-logica laten lezen
De auteurs bouwden een tweestapsysteem van neurale netwerken dat de “grammatica” van promotoren rechtstreeks uit DNA leert. Eerst verzamelden ze promotorsequenties van meer dan 100.000 genen uit gistverwanten en trainden ze een model, Place-Back genoemd, om te herkennen waar een kort DNA-fragment oorspronkelijk vandaan kwam nadat het was door elkaar gehaald en deels vervangen. Omdat het model de juiste plek alleen uit de context moest terugvinden, leerde het subtiele patronen over welke regio’s van een promotor gewijzigd kunnen worden zonder de kernfunctie te verstoren. Een tweede model, de Determiner, bekeek vervolgens Place-Backs voorspellingen en besliste zowel waar een nieuw regulatoir element moest komen als hoe groot een gebied van DNA herschreven moest worden.
Schakelbare promotoren in silico ontwerpen
Gewapend met dit systeem stelde het team een praktische vraag: waar konden ze een bekende bindingsplaats voor het TetR-repressoreiwit in echte gistpromotoren invoegen, zodat genen op commando uitgeschakeld konden worden? Ze testten virtueel alle 6.011 promotoren in het gistgenoom en produceerden een gerangschikte lijst van duizenden kandidaten waar het nieuwe element “paste” zonder essentiële kenmerken te verstoren, zoals het kernstartgebied waar transcriptie begint. De modellen gaven vaak de voorkeur aan locaties dicht bij deze kerngebieden, terwijl ze toch directe beschadiging meden, wat suggereert dat ze biologisch betekenisvolle beperkingen hadden geleerd.
AI-ontworpen schakelaars in de praktijk testen
Om te zien of de computersuggesties in levende cellen werkten, kozen de onderzoekers vier native gistpromotoren met verschillende sterktes en bewerkten elk precies zoals aanbevolen, waarbij ze de TetR-bindingsplaats op de voorspelde locatie invoegden. Ze koppelden deze promotoren aan een fel luciferasereporter en introduceerden TetR op een apart DNA-stuk, zodat het nieuwe systeem de eigen regulatie van gist niet zou verstoren. In aanwezigheid van TetR toonden drie van de vier ontwerpen sterke repressie, en één bereikte bijna volledige uitschakeling—ongeveer 98% reductie in activiteit—zonder verdere afstemming. Alternatieve invoegplaatsen die niet door het model werden voorgesteld, leidden vaak tot verlamde promotoren of vernietigden het responsvermogen, wat benadrukt dat de plaatsing ertoe doet en dat het neurale netwerk specifieke “sweet spots” identificeerde.
Het herbedraden van gist’ native besluitvorming
Het team gebruikte vervolgens dezelfde benadering om het eigen regulerende netwerk van gist aan te passen, in plaats van een kunstmatig toevoegingssysteem. Ze bewerkten de promotor van PCF11, een gen dat essentieel is voor overleving, om een bindingsplaats voor Mig1 in te voeren, een natuurlijke repressor die actief wordt in aanwezigheid van glucose. In testassays gedroeg de herontworpen promotor zich zoals bedoeld: wanneer glucose aanwezig was, daalde de PCF11-activiteit met meer dan de helft; wanneer glucose afwezig was, was de activiteit iets hoger dan normaal. Na het inwisselen van deze synthetische promotor in het gistgenoom groeiden cellen bijna normaal bij lage suikerconcentratie maar bereikten ze een lagere maximale dichtheid bij hoge suiker, wat laat zien dat het essentiële gen nu conditioneel werd beperkt door de nieuwe verbinding.
Wat dit betekent voor toekomstige genetische ontwerpen
Simpel gezegd laat dit werk zien dat neurale netwerken genoeg kunnen leren over de “taal” van genregulatie om slimme, contextbewuste wijzigingen aan DNA-schakelaars voor te stellen. Zonder experimentele metingen als trainingslabels wijzen de modellen plekken aan waar nieuwe controle-elementen veilig kunnen worden ingevoegd zodat genen reageren op gekozen signalen. De succesvolle tests in gist, inclusief het herbedraden van de controle over een essentieel gen, suggereren een pad naar schaalbaar, voorspelbaar ontwerp van regulatoir DNA in veel organismen. Dit kan het maken van op maat gemaakte genetische programma’s voor geneeskunde, landbouw en industriële biotechnologie versnellen, terwijl het ook nieuwe regels onthult over hoe cellen van nature hun eigen besluitvormingscircuits organiseren.
Bronvermelding: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Trefwoorden: synthetische biologie, genregulatie, neurale netwerken, promotorengineering, gist