Clear Sky Science · es
Diseño de promotores sintéticos con conciencia de contexto mediante redes neuronales permite reconfigurar redes de transcripción eucariotas
Enseñar nuevas habilidades a las células
La biotecnología moderna suele girar en torno a una pregunta simple: ¿podemos indicarle a una célula exactamente cuándo activar o desactivar un gen? Este artículo explora una nueva forma de hacerlo en la levadura de pan, usando inteligencia artificial para rediseñar pequeños interruptores de ADN llamados promotores. Al aprender cómo se conectan estos interruptores naturales, los autores muestran que los ordenadores pueden proponer ediciones precisas que permiten a los científicos enchufar nuevos controles al circuito genético de la célula.
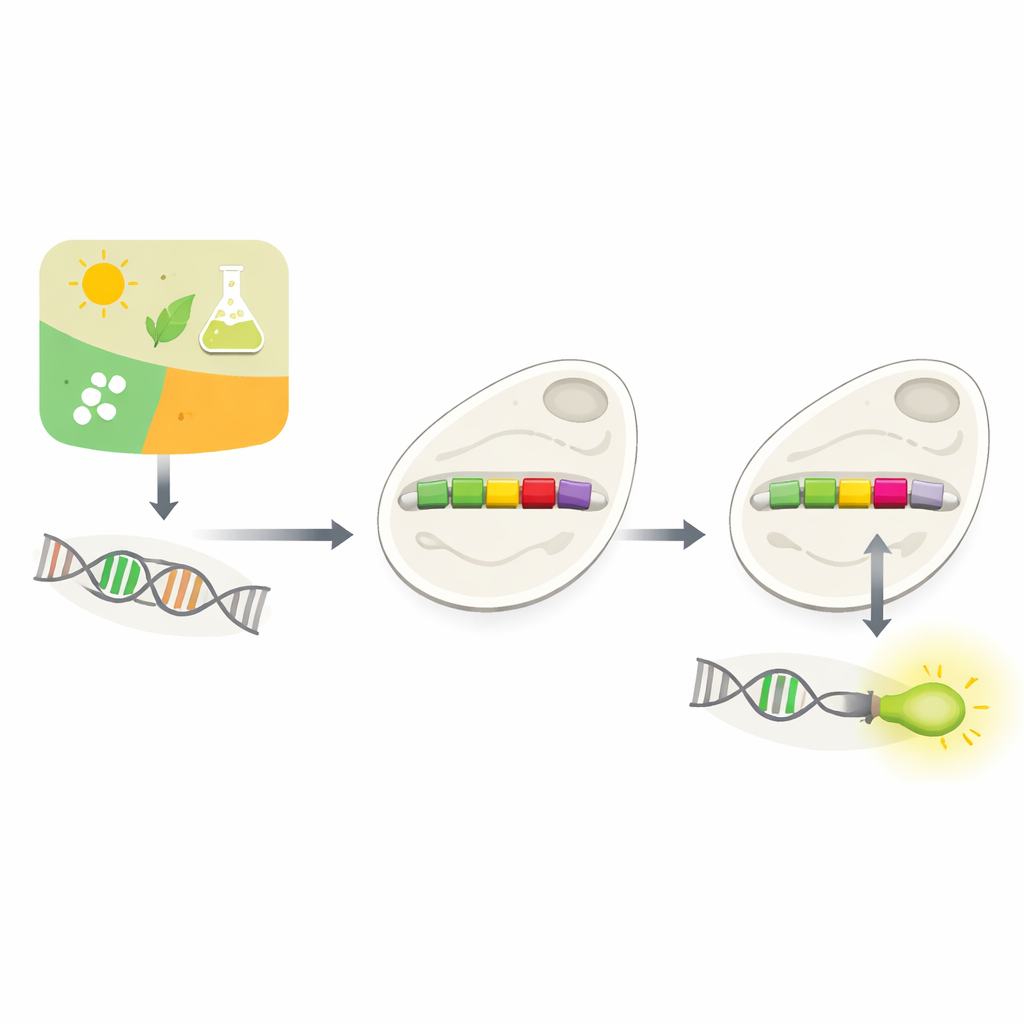
Cómo deciden las células qué genes usar
Cada célula debe decidir constantemente qué genes usar y cuándo. Gran parte de esta toma de decisiones ocurre en los promotores, tramos cortos de ADN que se sitúan justo antes de los genes. Los promotores actúan como reguladores de intensidad, respondiendo a señales del entorno o del interior de la célula. Los biólogos llevan tiempo intentando construir promotores a medida para controlar genes a voluntad—por ejemplo, para que la levadura produzca compuestos valiosos o para detectar toxinas. Pero los promotores naturales son complejos y dependientes del contexto, y simplemente introducir nuevos elementos de control en ellos suele romper su función. Probar muchas posibles variantes experimentalmente es lento y costoso.
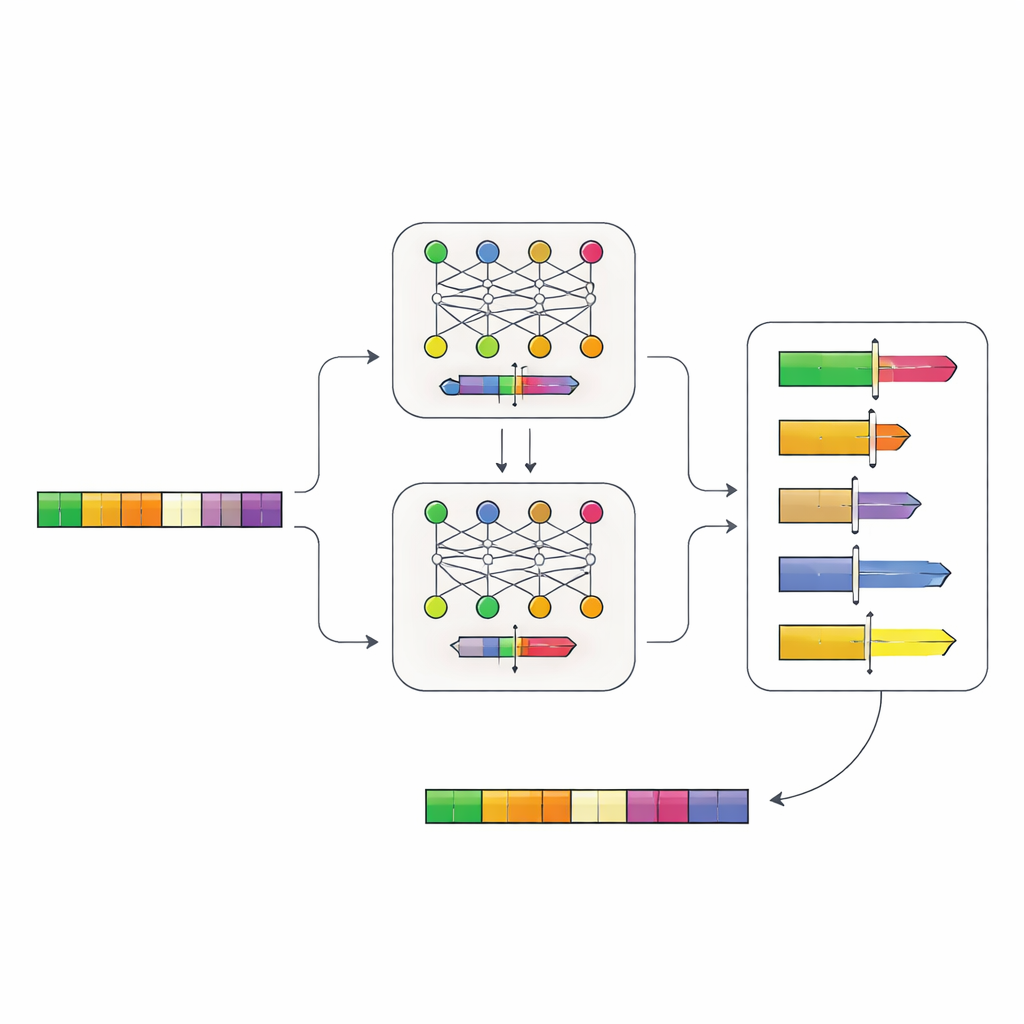
Dejar que las redes neuronales lean la lógica del ADN
Los autores construyeron un sistema de redes neuronales en dos etapas que aprende la “gramática” de los promotores directamente del ADN. Primero, recolectaron secuencias promotoras de más de 100.000 genes en parientes de la levadura y entrenaron un modelo, llamado Place-Back, para reconocer de dónde procedía originalmente un segmento corto de ADN después de haber sido reordenado y parcialmente reemplazado. Porque el modelo debía recuperar la posición correcta basándose solo en el contexto, aprendió patrones sutiles sobre qué regiones de un promotor pueden cambiarse sin perturbar su función central. Un segundo modelo, el Determiner, examinó entonces las predicciones de Place-Back y decidió tanto dónde debería ir un nuevo elemento regulador como qué tan amplia debía ser la región de ADN a reescribir.
Diseñar promotores conmutables in silico
Con este sistema, el equipo planteó una pregunta práctica: ¿dónde podrían insertar un sitio de unión bien conocido para la proteína represora TetR en promotores reales de levadura, de modo que los genes pudieran silenciarse bajo demanda? Probaron virtualmente los 6.011 promotores del genoma de la levadura y produjeron una lista ordenada de miles de candidatos donde el nuevo elemento debería “encajar” sin perturbar características esenciales, como la región central de inicio donde comienza la transcripción. Los modelos con frecuencia prefirieron sitios cercanos a estas regiones centrales evitando a la vez daños directos, lo que sugiere que aprendieron restricciones con sentido biológico.
Poner a prueba los interruptores diseñados por IA
Para comprobar si las sugerencias del ordenador funcionaban en células vivas, los investigadores escogieron cuatro promotores nativos de levadura de distintas intensidades y editaron cada uno exactamente como se recomendó, insertando el sitio de unión de TetR en la ubicación predicha. Ligaron estos promotores a un brillante reportero de luciferasa e introdujeron TetR en un fragmento de ADN separado, de modo que el sistema nuevo no interfiriera con la regulación propia de la levadura. En presencia de TetR, tres de los cuatro diseños mostraron una fuerte represión, y uno alcanzó un apagado casi completo—aproximadamente un 98% de reducción de la actividad—sin ajustes adicionales. Sitios de inserción alternativos no sugeridos por el modelo con frecuencia inutilizaban el promotor o destruían su capacidad de respuesta, subrayando que la colocación importa y que la red neuronal identificó puntos concretos “óptimos”.
Reconfigurar la toma de decisiones nativa de la levadura
El equipo usó luego el mismo enfoque para alterar la propia red reguladora de la levadura, en lugar de un sistema artificial añadido. Editaron el promotor de PCF11, un gen esencial para la supervivencia, para insertar un sitio de unión para Mig1, un represor natural que se activa en presencia de glucosa. En ensayos, el promotor rediseñado se comportó como se esperaba: cuando había glucosa, la actividad de PCF11 cayó a más de la mitad; cuando la glucosa estaba ausente, la actividad fue ligeramente superior a la normal. Tras reemplazar este promotor sintético en el genoma de la levadura, las células crecieron casi con normalidad en baja concentración de azúcar pero alcanzaron una densidad máxima menor en alta concentración, mostrando que el gen esencial quedó ahora condicionado por la nueva conexión.
Qué significa esto para el diseño genético futuro
En términos sencillos, este trabajo muestra que las redes neuronales pueden aprender lo suficiente sobre el “lenguaje” del control génico como para proponer ediciones inteligentes y conscientes del contexto en los interruptores de ADN. Sin necesitar mediciones experimentales como etiquetas de entrenamiento, los modelos señalan lugares donde pueden insertarse de forma segura nuevos elementos de control para que los genes respondan a señales elegidas. Las pruebas exitosas en levadura, incluida la reconfiguración del control de un gen esencial, sugieren un camino hacia un diseño escalable y predictivo del ADN regulador en muchos organismos. Esto podría acelerar la creación de programas genéticos a medida para la medicina, la agricultura y la biotecnología industrial, a la vez que revela nuevas reglas sobre cómo las células organizan naturalmente sus circuitos de toma de decisiones.
Cita: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Palabras clave: biología sintética, regulación génica, redes neuronales, ingeniería de promotores, levadura