Clear Sky Science · it
Progettazione di promotori sintetici consapevoli del contesto mediante reti neurali consente il ricollegamento delle reti trascrizionali eucariotiche
Insegnare nuove abilità alle cellule
La biotecnologia moderna spesso ruota attorno a una domanda semplice: possiamo dire a una cellula esattamente quando attivare o disattivare un gene? Questo articolo esplora un nuovo modo per farlo nel lievito di birra, usando l’intelligenza artificiale per riprogettare minuscoli interruttori di DNA chiamati promotori. Imparando come sono cablati questi interruttori naturali, gli autori dimostrano che i computer possono proporre modifiche precise che permettono agli scienziati di collegare nuovi manopole di controllo al circuito genetico della cellula.
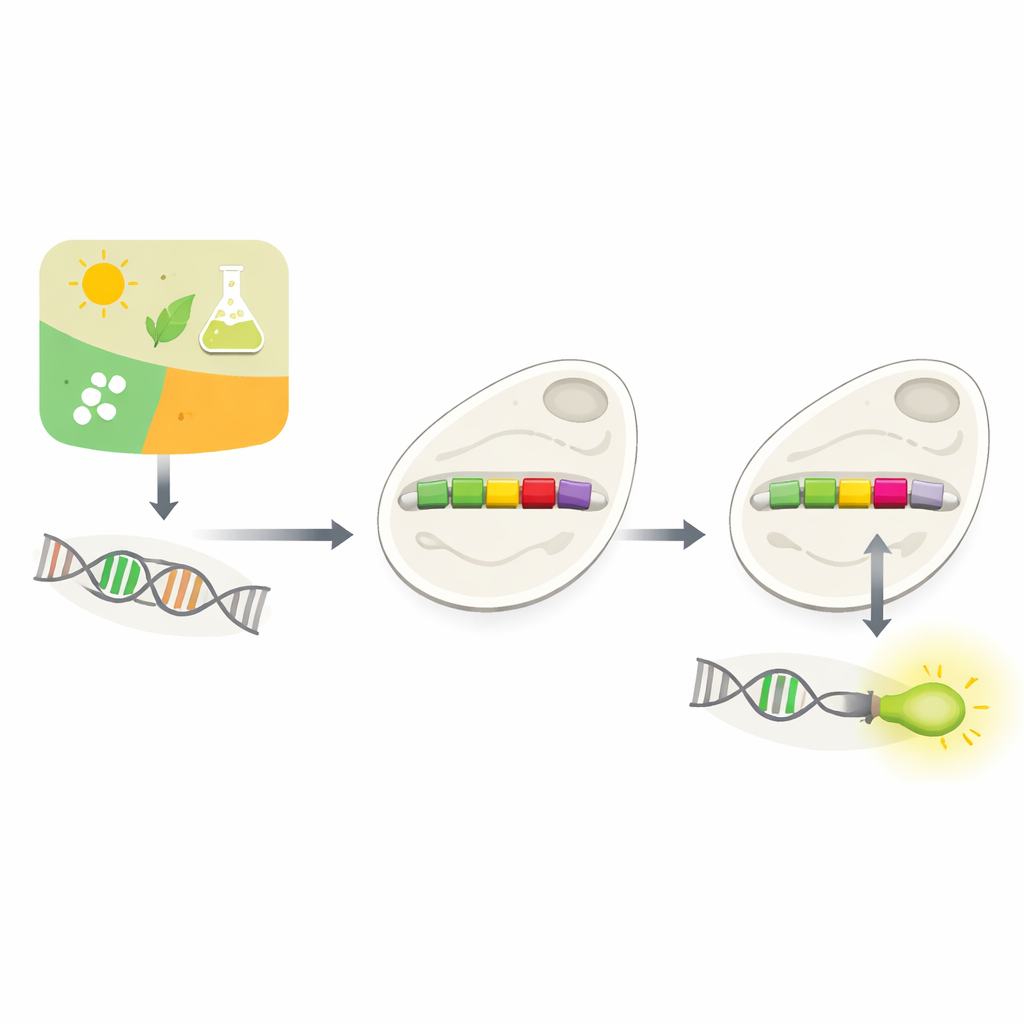
Come le cellule decidono quali geni usare
Ogni cellula deve decidere continuamente quali geni utilizzare e quando. Gran parte di questo processo decisionale avviene nei promotori, brevi tratti di DNA che si trovano immediatamente prima dei geni. I promotori agiscono come dimmer, rispondendo a segnali dall’ambiente o dall’interno della cellula. I biologi hanno a lungo provato a costruire promotori su misura per poter controllare i geni a piacimento—for example, per far produrre al lievito sostanze di valore o per rilevare tossine. Ma i promotori naturali sono complessi e dipendono dal contesto, e inserire semplicemente nuovi elementi di controllo spesso ne compromette la funzione. Testare sperimentalmente molte possibili soluzioni è lento e costoso.
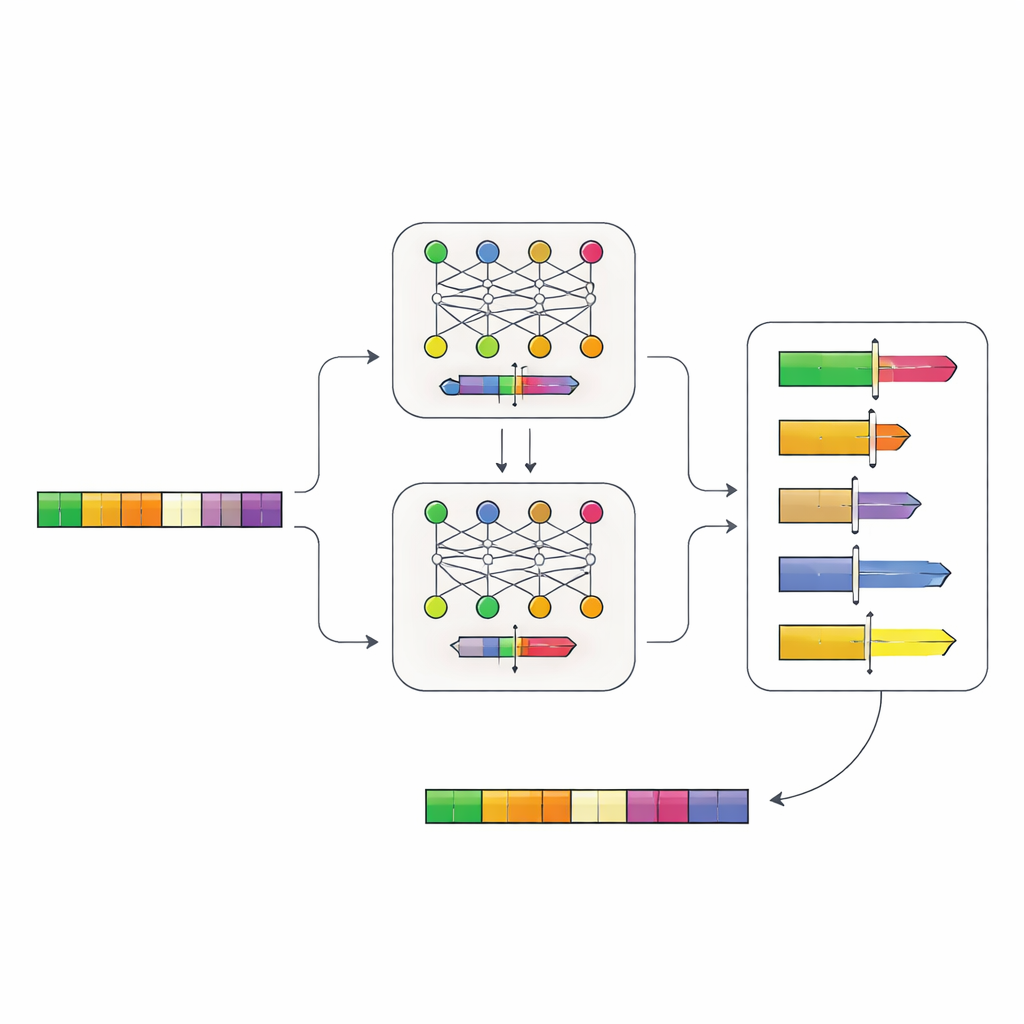
Lasciare che le reti neurali leggano la logica del DNA
Gli autori hanno costruito un sistema a due fasi basato su reti neurali che apprende direttamente la “grammatica” dei promotori dal DNA. Per prima cosa hanno raccolto sequenze di promotori da oltre 100.000 geni in parenti del lievito e hanno addestrato un modello, chiamato Place-Back, a riconoscere da dove proveniva originariamente un breve segmento di DNA dopo che era stato rimescolato e parzialmente sostituito. Poiché il modello doveva recuperare la posizione corretta basandosi solo sul contesto, ha appreso schemi sottili su quali regioni di un promotore possono essere modificate senza disturbare la sua funzione fondamentale. Un secondo modello, il Determiner, ha poi esaminato le predizioni di Place-Back e ha deciso sia dove inserire un nuovo elemento regolatorio sia quanto ampia dovesse essere la regione di DNA riscritta.
Progettare promotori commutabili in silico
Dotati di questo sistema, il team ha posto una domanda pratica: dove si potrebbe inserire un noto sito di legame per la proteina repressore TetR nei promotori reali del lievito, in modo che i geni possano essere spenti su comando? Hanno testato virtualmente tutti i 6.011 promotori nel genoma del lievito e prodotto una lista classificata di migliaia di candidati in cui il nuovo elemento dovrebbe “adattarsi” senza disturbare caratteristiche essenziali, come la regione di inizio core dove comincia la trascrizione. I modelli spesso privilegiavano siti vicini a queste regioni core evitando però danni diretti, suggerendo di aver imparato vincoli biologicamente rilevanti.
Mettere alla prova gli interruttori progettati dall’IA
Per verificare se i suggerimenti del computer funzionassero in cellule vive, i ricercatori hanno scelto quattro promotori nativi del lievito con diverse intensità e hanno modificato ciascuno esattamente come raccomandato, inserendo il sito di legame di TetR nella posizione prevista. Hanno collegato questi promotori a un forte reporter luciferasi e hanno introdotto TetR su un pezzo di DNA separato, in modo che il nuovo sistema non interferisse con la regolazione endogena del lievito. In presenza di TetR, tre dei quattro progetti hanno mostrato una forte repressione, e uno ha raggiunto quasi lo spegnimento completo—circa il 98% di riduzione dell’attività—senza ulteriori messa a punto. Siti di inserzione alternativi non suggeriti dal modello spesso hanno danneggiato il promotore o distrutto la sua capacità di rispondere, sottolineando che la posizione conta e che la rete neurale stava identificando specifici “punti ideali”.
Ricollegare il sistema decisionale nativo del lievito
Il team ha poi usato lo stesso approccio per alterare la rete regolatoria nativa del lievito, anziché un sistema aggiuntivo artificiale. Hanno modificato il promotore di PCF11, un gene essenziale per la sopravvivenza, per inserire un sito di legame per Mig1, un repressore naturale che diventa attivo in presenza di glucosio. Nei saggi di prova, il promotore riprogettato si è comportato come previsto: quando il glucosio era presente, l’attività di PCF11 è diminuita di oltre la metà; quando il glucosio era assente, l’attività era leggermente superiore al normale. Dopo aver sostituito questo promotore sintetico nel genoma del lievito, le cellule hanno cresciuto quasi normalmente a basso tenore di zucchero ma hanno raggiunto una densità massima inferiore ad alto zucchero, mostrando che il gene essenziale è ora vincolato condizionatamente dalla nuova connessione.
Cosa significa per il futuro della progettazione genetica
In termini semplici, questo lavoro mostra che le reti neurali possono apprendere abbastanza sul “linguaggio” del controllo genico da suggerire modifiche intelligenti e consapevoli del contesto ai commutatori del DNA. Senza richiedere misure sperimentali come etichette di addestramento, i modelli indicano punti in cui nuovi elementi di controllo possono essere inseriti in sicurezza affinché i geni diventino rispondenti a segnali scelti. I test riusciti nel lievito, incluso il ricollegamento del controllo di un gene essenziale, suggeriscono una via verso una progettazione predittiva e scalabile del DNA regolatorio in molti organismi. Questo potrebbe accelerare la creazione di programmi genetici su misura per la medicina, l’agricoltura e la biotecnologia industriale, rivelando al contempo nuove regole su come le cellule organizzano naturalmente i loro circuiti decisionali.
Citazione: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Parole chiave: biologia sintetica, regolazione genica, reti neurali, ingegneria dei promotori, lievito