Clear Sky Science · fr
Conception de promoteurs synthétiques sensibles au contexte via des réseaux neuronaux permettant le recâblage des réseaux transcriptionnels eucaryotes
Apprendre de Nouveaux Tours aux Cellules
La biotechnologie moderne repose souvent sur une question simple : peut-on indiquer à une cellule exactement quand activer ou désactiver un gène ? Cet article explore une nouvelle manière de le faire chez la levure de boulanger, en utilisant l’intelligence artificielle pour redesigner de petites bascules d’ADN appelées promoteurs. En apprenant comment ces interrupteurs naturels sont câblés, les auteurs montrent que des ordinateurs peuvent proposer des modifications précises permettant aux scientifiques d’intégrer de nouveaux boutons de contrôle dans le circuit génétique de la cellule.
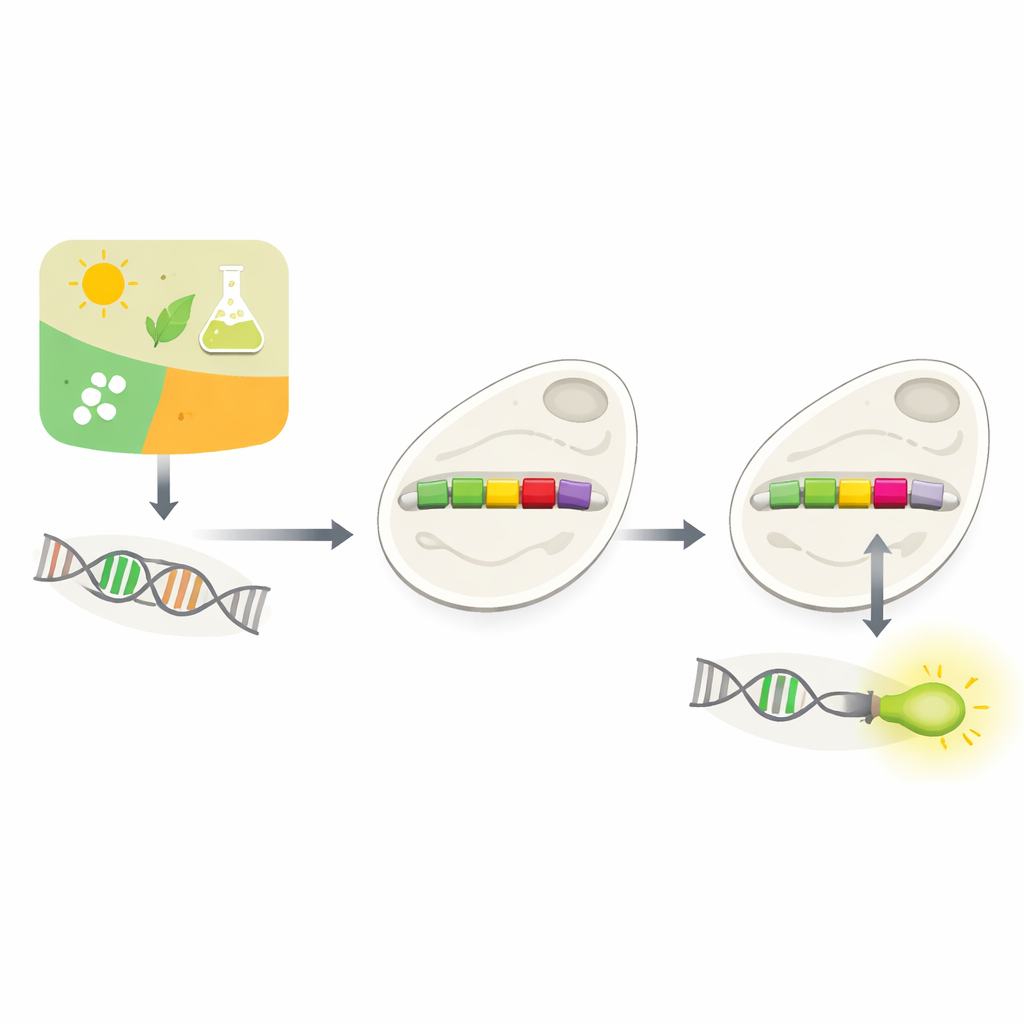
Comment les Cellules Décident Quels Gènes Utiliser
Chaque cellule doit constamment décider quels gènes utiliser, et quand. Une grande partie de cette prise de décision a lieu au niveau des promoteurs, de courts segments d’ADN situés juste en amont des gènes. Les promoteurs agissent comme des variateurs, répondant à des signaux venus de l’environnement ou de l’intérieur de la cellule. Les biologistes ont depuis longtemps tenté de concevoir des promoteurs sur mesure pour contrôler les gènes à volonté — par exemple pour faire produire à la levure des molécules de valeur ou détecter des toxines. Mais les promoteurs naturels sont complexes et dépendants du contexte, et insérer simplement de nouveaux éléments de régulation les casse souvent. Tester expérimentalement de nombreuses conceptions est lent et coûteux.
Laisser les Réseaux Neuronaux Lire la Logique de l’ADN
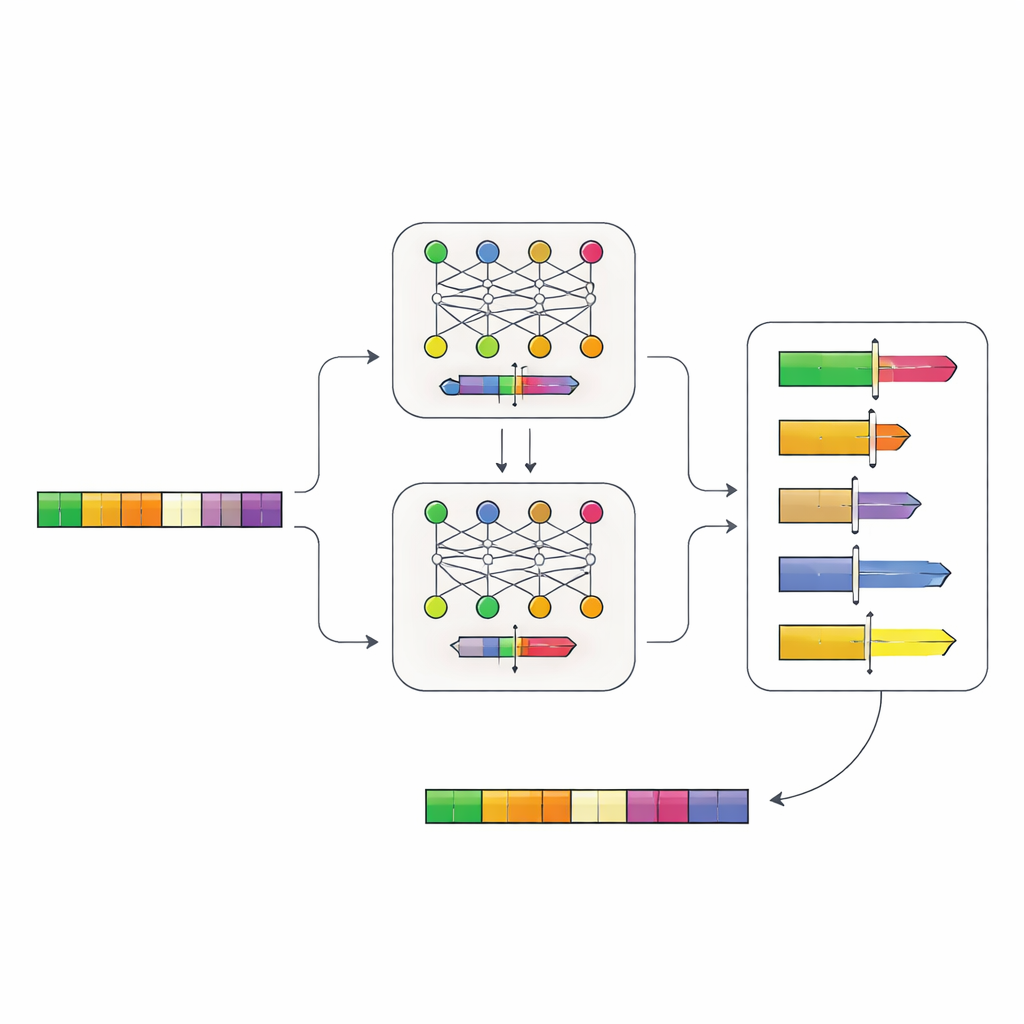
Les auteurs ont construit un système en deux étapes basé sur des réseaux neuronaux qui apprend la « grammaire » des promoteurs directement depuis l’ADN. D’abord, ils ont collecté des séquences de promoteurs provenant de plus de 100 000 gènes chez des proches de la levure et entraîné un modèle, appelé Place-Back, à reconnaître d’où provenait initialement un petit segment d’ADN après qu’il ait été mélangé et partiellement remplacé. Puisque le modèle devait retrouver la bonne position à partir du seul contexte, il a appris des motifs subtils sur les régions d’un promoteur qui peuvent être modifiées sans perturber sa fonction centrale. Un second modèle, le Determiner, a ensuite examiné les prédictions de Place-Back et décidé à la fois où insérer un nouvel élément régulateur et quelle étendue de la région d’ADN devait être réécrite.
Concevoir des Promoteurs Commutables In Silico
Armés de ce système, l’équipe s’est posé une question pratique : où pourraient-ils insérer un site de liaison bien connu pour la protéine répresseur TetR dans des promoteurs réels de levure, afin que des gènes puissent être éteints sur commande ? Ils ont testé virtuellement les 6 011 promoteurs du génome de la levure et produit une liste classée de milliers de candidats où le nouvel élément devrait « s’intégrer » sans perturber des caractéristiques essentielles, comme la région de démarrage centrale où commence la transcription. Les modèles privilégiaient souvent des sites proches de ces régions centrales tout en évitant les dommages directs, ce qui suggère qu’ils avaient appris des contraintes biologiquement significatives.
Mettre à l’Épreuve des Interrupteurs Conçus par IA
Pour vérifier si les suggestions de l’ordinateur fonctionnaient dans des cellules vivantes, les chercheurs ont choisi quatre promoteurs natifs de levure de forces différentes et ont modifié chacun exactement comme recommandé, en insérant le site de liaison TetR à l’emplacement prédit. Ils ont relié ces promoteurs à un rapporteur lumineux luciférase et introduit TetR sur un fragment d’ADN séparé, de sorte que le nouveau système n’interfère pas avec la régulation propre à la levure. En présence de TetR, trois des quatre conceptions ont montré une forte répression, et l’une a atteint une extinction presque complète — environ 98 % de réduction d’activité — sans réglage supplémentaire. Des sites d’insertion alternatifs non suggérés par le modèle ont souvent handicapé le promoteur ou détruit sa capacité à répondre, soulignant que le positionnement compte et que le réseau neuronal identifiait des « points sensibles » spécifiques.
Recâbler la Prise de Décision Native de la Levure
L’équipe a ensuite utilisé la même approche pour modifier le réseau de régulation propre à la levure, plutôt qu’un système additionnel artificiel. Ils ont édité le promoteur de PCF11, un gène essentiel à la survie, pour y insérer un site de liaison pour Mig1, un répresseur naturel qui s’active en présence de glucose. Dans des essais, le promoteur redesigné s’est comporté comme prévu : en présence de glucose, l’activité de PCF11 a chuté de plus de moitié ; en l’absence de glucose, l’activité était légèrement supérieure à la normale. Après avoir replacé ce promoteur synthétique dans le génome de la levure, les cellules ont grossièrement poussé normalement en faible teneur en sucre mais ont atteint une densité maximale plus faible en forte teneur en sucre, montrant que le gène essentiel était désormais conditionnellement contraint par la nouvelle connexion.
Ce que Cela Signifie pour la Conception Génétique Future
En termes simples, ce travail montre que des réseaux neuronaux peuvent apprendre suffisamment du « langage » du contrôle génétique pour proposer des modifications intelligentes et sensibles au contexte des interrupteurs d’ADN. Sans nécessiter de mesures expérimentales comme étiquettes d’entraînement, les modèles indiquent des emplacements où de nouveaux éléments de contrôle peuvent être insérés en toute sécurité afin que des gènes répondent à des signaux choisis. Les tests concluants chez la levure, incluant le recâblage du contrôle d’un gène essentiel, suggèrent une voie vers une conception prédictive et évolutive de l’ADN régulateur dans de nombreux organismes. Cela pourrait accélérer la création de programmes génétiques sur mesure pour la médecine, l’agriculture et la biotechnologie industrielle, tout en révélant de nouvelles règles sur la manière dont les cellules organisent naturellement leurs propres circuits décisionnels.
Citation: Kuhajda, L., Honzik, T., Svec, J. et al. Context-aware synthetic promoter design using neural networks enables rewiring of eukaryotic transcriptional networks. npj Syst Biol Appl 12, 65 (2026). https://doi.org/10.1038/s41540-026-00684-5
Mots-clés: biologie synthétique, régulation génique, réseaux neuronaux, ingénierie des promoteurs, levure