Clear Sky Science · zh
使用扩展序列库的高速多路复用 DNA-PAINT 成像揭示核结构
以新细节观察细胞核
在我们每个细胞内部,基因组以一种错综复杂的方式折叠和排列,帮助控制哪些基因被开启或关闭。直到最近,这些内部结构大多太小且过于拥挤,难以清晰可见。本文描述了一种更快、更强大的成像方法,使研究者能够以近分子精度同时绘制多种核成分的分布,揭示当基因活性被关闭时基因组及其周围结构如何重组。
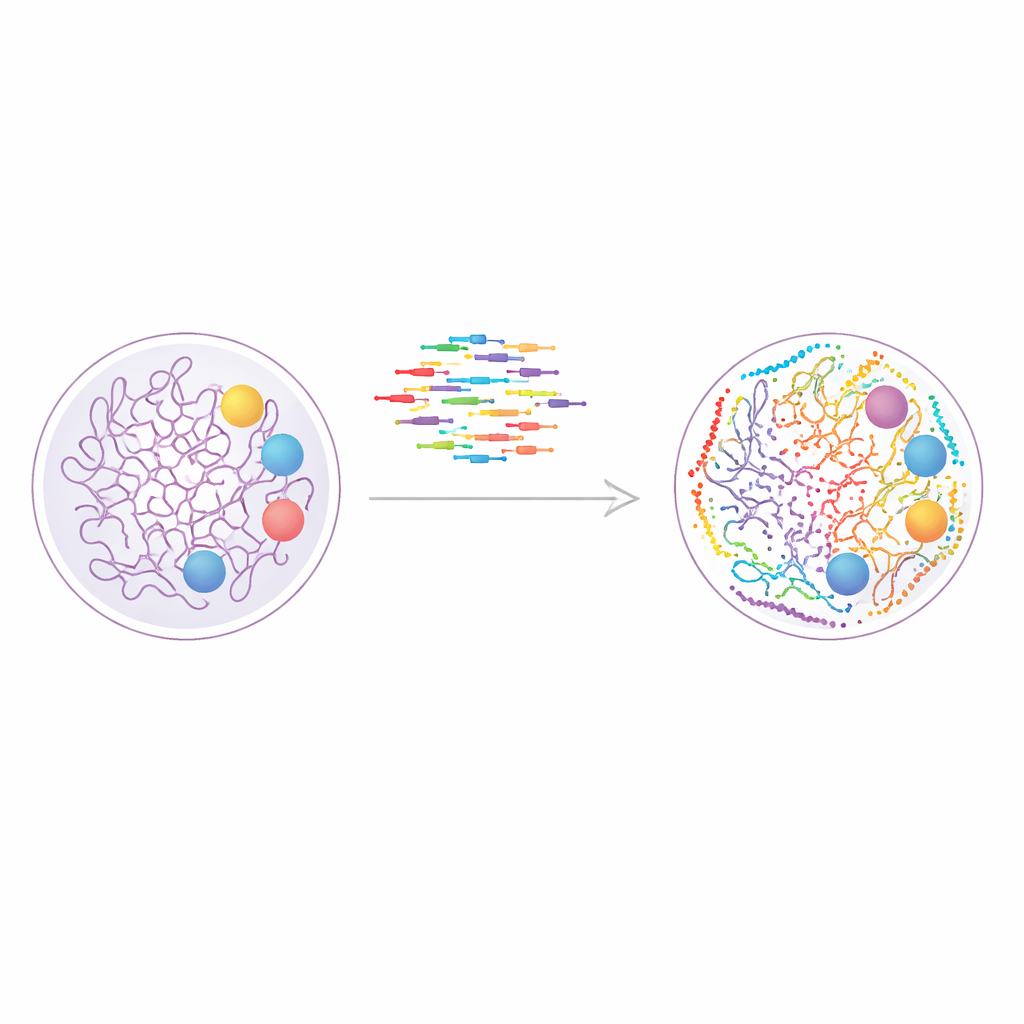
为基因组染上新颜色的方式
该研究建立在一种称为 DNA-PAINT 的技术之上,该技术使用短的荧光 DNA 链反复结合并解离到细胞结构上的匹配 DNA 标签。每次结合事件都会产生一次微小的光爆发,多个此类事件可以合成出远超普通显微镜极限的清晰图像。DNA-PAINT 天然适合在同一细胞中观察多个目标,因为每种蛋白或染色质标记都可以用不同的 DNA 序列进行标记。问题在于速度:传统的序列设计结合得太慢,使得每轮成像都需要数小时。
扩展颜色调色板
为了解决这一瓶颈,作者系统地设计了一组更宽的“速度优化”DNA 序列,这些序列能更频繁地结合,同时仍保持特异性。他们构建了设计化的 DNA 纳米结构(称为 DNA 折纸)来测试每个成像探针链识别其匹配停靠链的能力以及闪烁频率。通过组装携带停靠位点、以精确 4×3 网格排列且相距仅 20 纳米的折纸瓷砖,他们能够同时测量分辨率和不期望的串扰。这项工作总共产出了十二个快速序列,其中十个可以共同使用而互不干扰,从而在一次实验中直接成像多达十个目标。
更短时间内获得更清晰图像
并非所有快速序列的表现都相同。一部分序列表现出更长的结合事件,这被证明尤为有用。当团队在同一折纸网格上比较短结合与长结合序列时,长结合探针在相邻位点之间产生了更清晰的分离,即使在更低的激光功率下也能做到。较长的事件让相机能从每次结合中收集到更多光子,从而将定位精度提升到仅几纳米。这些探针对目标位点的采样也更高效,在更少的帧数中就能达到可靠覆盖。实际上,这意味着研究者可以在几分钟而非数小时内获取高质量的超分辨图像,并降低对样品造成损伤的风险。
绘制核内景观
凭借扩展的序列集合,研究人员从人造的 DNA 结构转向活细胞生物学。他们使用 DNA-PAINT 在人类细胞中成像了九种不同的核特征,包括活性与暂停态的 RNA 聚合酶 II、多种标志活跃或沉默染色质的组蛋白化学修饰、位于边缘的核纤层,以及富含剪接因子的类液滴状核斑。通过将常规抗体耦合到 DNA 停靠链并在九个连续轮次中成像这些靶点,他们组装出了一个超分辨、多路复用的核地图,其中每个点对应一个仅几纳米宽的分子微环境。
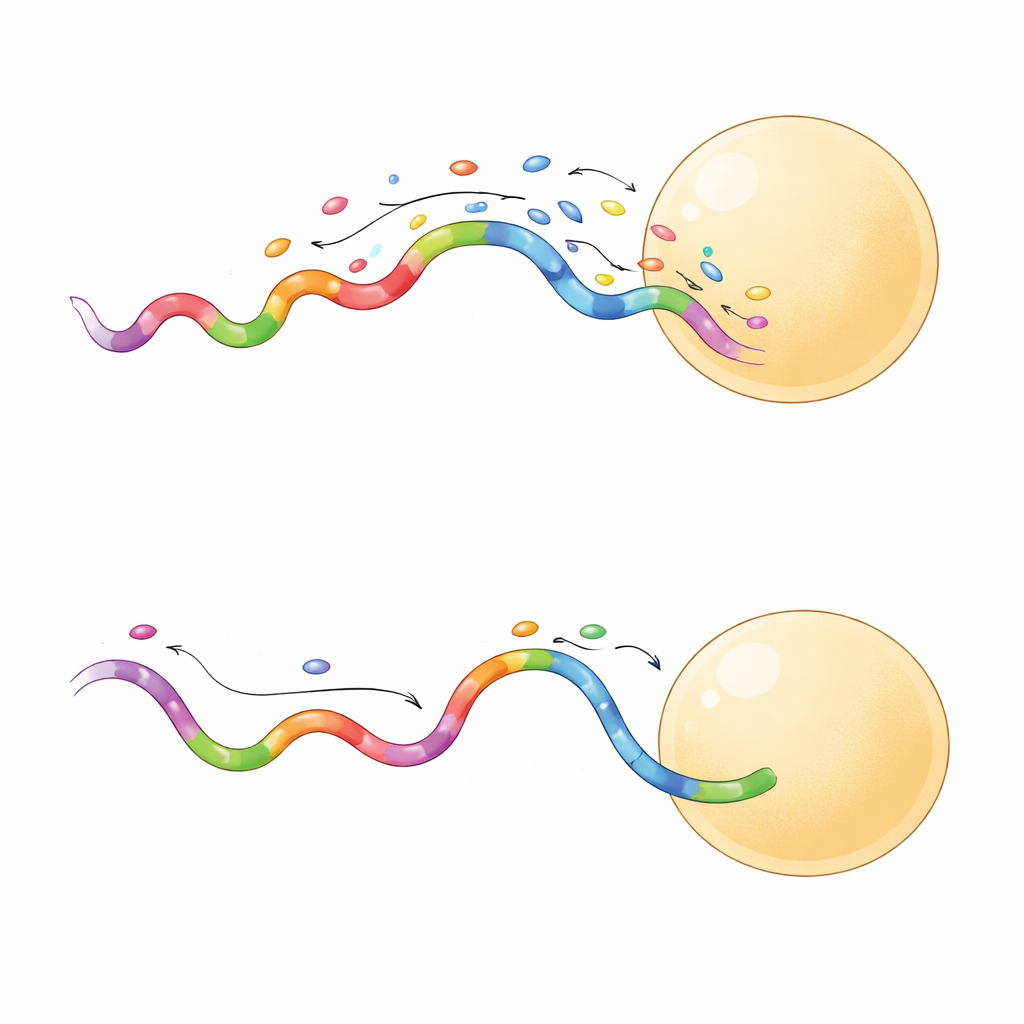
观察染色质对压力的反应
接着,团队探究当转录——即将 DNA 复制为 RNA 的过程——被阻断时,这一核地图如何变化。用药物放线菌素 D 处理细胞会使 RNA 聚合酶在 DNA 上停滞,这显著重塑了核内的空间关系。通常轮廓不规则并位于活性染色质中的核斑变得更为圆润,且它们与转录位点和活性组蛋白标记的紧密接触大多消失。与此同时,抑制性染色质标记与核纤层的关联增强,这与基因组更加致密、处于沉默状态一致。通过结合多层统计分析,作者能够将全局趋势与不同核成分之间局部富集或排斥的区域区分开来。
这对生物学为何重要
本质上,这项工作将 DNA-PAINT 转变为一种更快、更通用的工具,用于绘制细胞内部地理。借助更大的速度优化 DNA 序列库,科学家现在可以在实用时间范围内以纳米级分辨率在同一细胞中追踪众多核地标。作者展示了该方法足够灵敏,能够捕捉到在转录停止时染色质如何从核斑脱离并在边缘聚集。随着该方法扩展到更多蛋白和修饰,它有望绘制出健康与疾病状态下的详细“核组织图谱”,帮助揭示基因调控在三维空间中的布线方式。
引用: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
关键词: 超分辨成像, DNA-PAINT, 染色质组织, 核斑, 转录抑制