Clear Sky Science · pt
Imagem multiplexada de alta velocidade DNA-PAINT da organização nuclear usando um repertório de sequências ampliado
Vendo o núcleo celular com novos detalhes
Dentro de cada uma de nossas células, o genoma é dobrado e organizado de forma intrincada que ajuda a controlar quais genes são ativados ou silenciados. Até recentemente, grande parte dessa arquitetura interna era pequena e densa demais para ser vista com clareza. Este artigo descreve um método de imageamento mais rápido e mais potente que permite aos pesquisadores mapear muitos componentes nucleares ao mesmo tempo com precisão quase molecular, revelando como o genoma e suas estruturas circundantes se reorganizam quando a atividade gênica é interrompida.
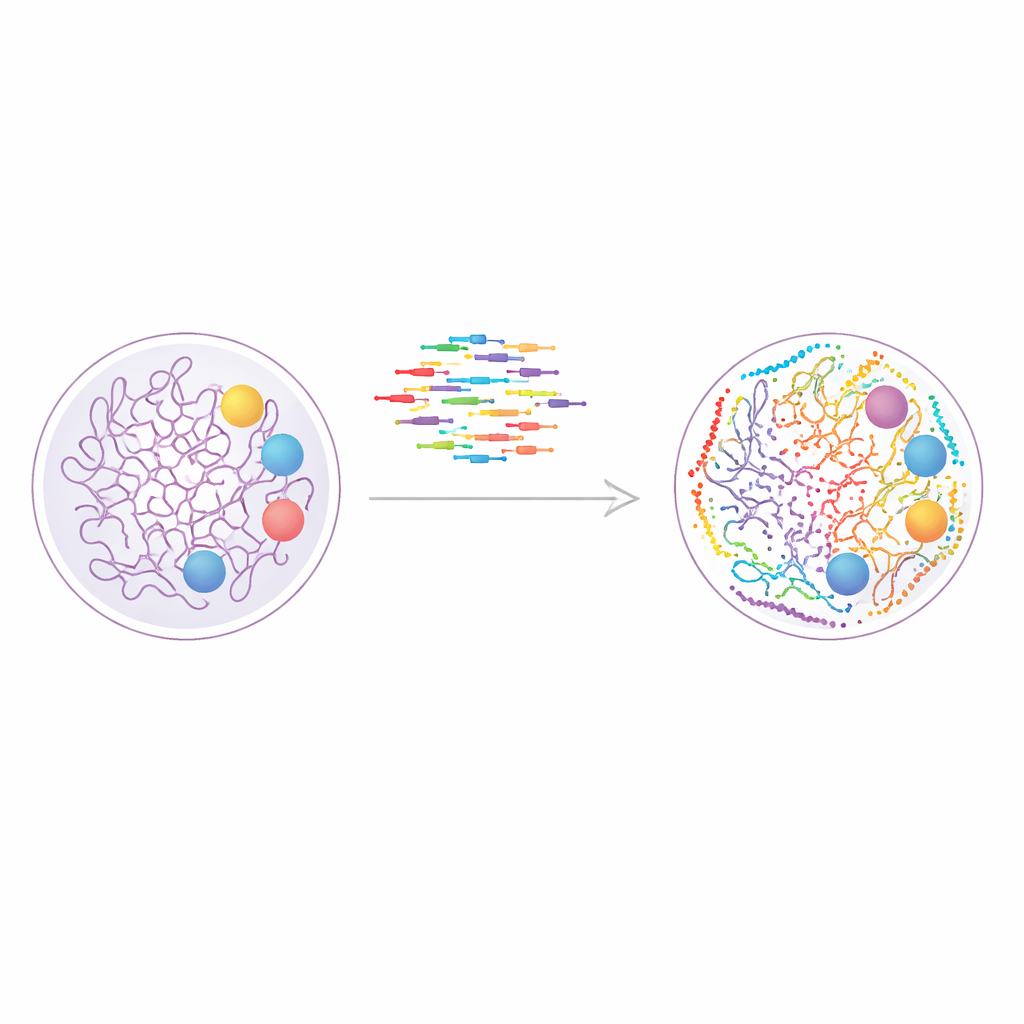
Uma nova forma de pintar o genoma
O estudo se baseia em uma técnica chamada DNA-PAINT, que usa curtas fitas de DNA fluorescente que se ligam e se desligam repetidamente de etiquetas de DNA correspondentes em estruturas celulares. Cada evento de ligação produz um pequeno flash de luz, e muitos desses eventos podem ser combinados para reconstruir uma imagem nítida muito além dos limites de microscópios convencionais. O DNA-PAINT é naturalmente bem adequado para observar muitos alvos na mesma célula, porque cada proteína ou marca de cromatina pode ser etiquetada com uma sequência de DNA distinta. O problema tem sido a velocidade: os designs de sequência tradicionais se ligam muito lentamente, transformando cada rodada de imageamento em experimentos de horas.
Ampliando a paleta de cores
Para enfrentar esse gargalo, os autores projetaram sistematicamente um conjunto mais amplo de sequências de DNA “otimizadas para velocidade” que se ligam com maior frequência mantendo a especificidade. Eles construíram nanomateriais de DNA desenhados, conhecidos como DNA origami, para testar o quão bem cada fita imagadora reconhecia sua fita âncora correspondente e com que frequência ela piscava. Ao montar ladrilhos de origami que carregavam sítios de ancoragem dispostos em uma grade precisa 4 por 3 a apenas 20 nanômetros de distância, puderam medir tanto a resolução quanto o vazamento indesejado entre canais. Esse trabalho produziu no total doze sequências rápidas, das quais dez puderam ser usadas em conjunto sem interferência, permitindo imageamento direto de até dez alvos em um experimento.
Imagens mais nítidas em menos tempo
Nem todas as sequências rápidas se comportaram da mesma forma. Um subconjunto produziu eventos de ligação de duração maior, que se mostraram especialmente úteis. Quando a equipe comparou uma sequência de ligação curta com uma de ligação longa na mesma grade de origami, a sonda de ligação longa produziu separação mais nítida entre sítios vizinhos e o fez mesmo com potência de laser menor. Eventos mais longos permitiram à câmera coletar mais fótons de cada ligação, aumentando a precisão de localização para apenas alguns nanômetros. Essas sondas também amostraram os sítios-alvo de forma mais eficiente, alcançando cobertura confiável em menos quadros. Na prática, isso significa que pesquisadores podem adquirir imagens de super-resolução de alta qualidade em minutos em vez de horas, com menor risco de danificar a amostra.
Mapeando a paisagem nuclear
Munidos de seu conjunto ampliado de sequências, os pesquisadores avançaram de estruturas artificiais de DNA para biologia celular viva. Eles usaram DNA-PAINT para imagear nove diferentes características nucleares em células humanas, incluindo formas ativas e pausadas da RNA polimerase II, várias marcas químicas em proteínas histonas que assinalam cromatina ativa ou silenciosa, a lâmina nuclear na periferia e os speckles nucleares—centros do tipo gotícula ricos em fatores de splicing. Ao acoplar anticorpos convencionais a fitas âncora de DNA e imagear os alvos em nove rodadas sequenciais, montaram um mapa multiplexado e de super-resolução do núcleo, onde cada ponto corresponde a um bairro molecular com apenas alguns nanômetros de diâmetro.
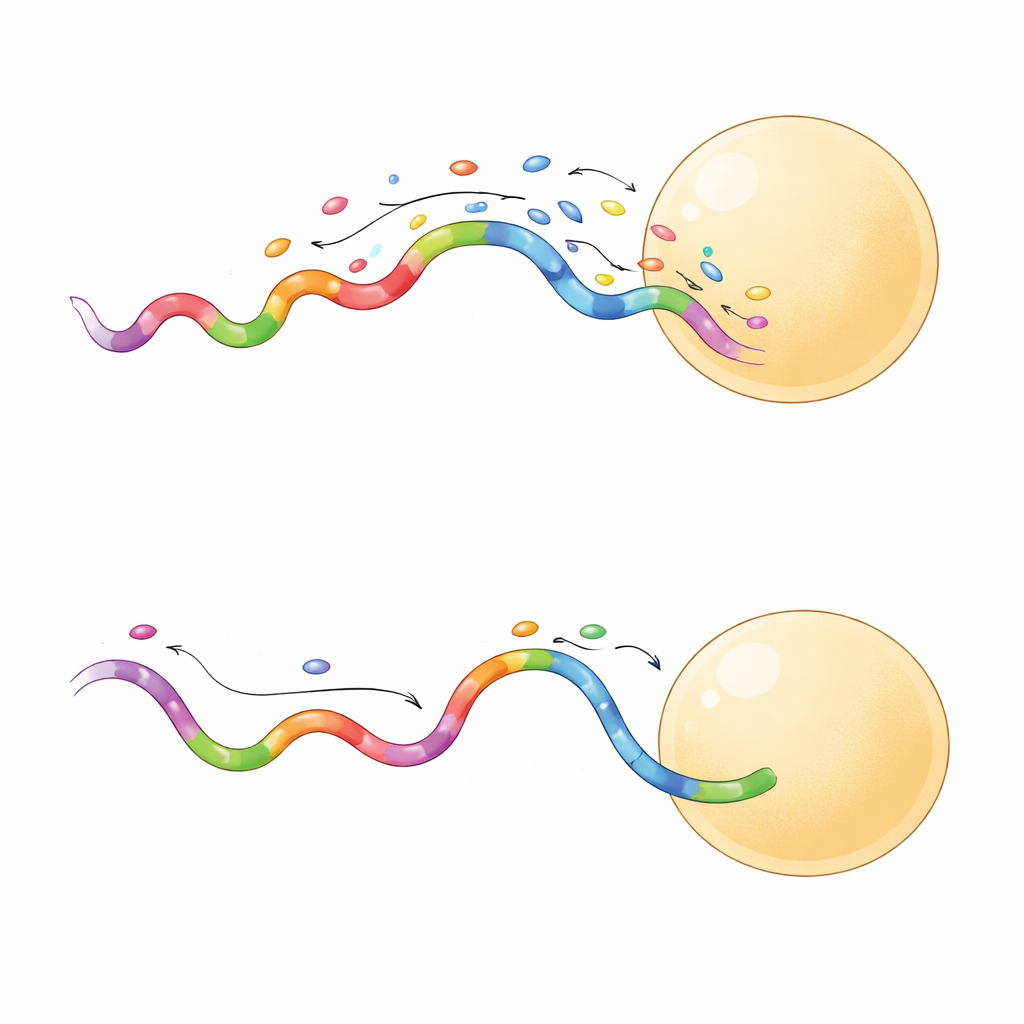
Observando a cromatina responder ao estresse
A equipe então investigou como esse mapa nuclear muda quando a transcrição—a cópia do DNA em RNA—é bloqueada. Tratar as células com o fármaco actinomicina D, que paralisa as RNA polimerases sobre o DNA, remodelou dramaticamente as relações espaciais dentro do núcleo. Os speckles nucleares, que normalmente têm contornos irregulares e ficam em meio à cromatina ativa, tornaram-se mais arredondados, e seus contatos próximos com locais de transcrição e marcas de histonas ativas desapareceram em grande parte. Ao mesmo tempo, marcas de cromatina repressiva mostraram associação reforçada com a lâmina nuclear, consistente com um genoma mais compactado e silenciado. Ao combinar várias camadas de análise estatística, os autores puderam distinguir tendências globais de bolsões locais de enriquecimento ou exclusão entre diferentes componentes nucleares.
Por que isso importa para a biologia
Essencialmente, este trabalho transforma o DNA-PAINT em uma ferramenta mais rápida e versátil para mapear a geografia interna da célula. Com uma biblioteca maior de sequências de DNA otimizadas para velocidade, os cientistas agora podem acompanhar muitos marcos nucleares na mesma célula com resolução em nanômetros e em escalas de tempo práticas. Os autores demonstram que essa abordagem é sensível o suficiente para capturar como a cromatina se descola dos speckles nucleares e se consolida na periferia quando a transcrição é interrompida. À medida que o método for estendido a mais proteínas e modificações, promete álgeos detalhados de organização nuclear em saúde e doença, ajudando a revelar como a regulação gênica é estruturada em três dimensões.
Citação: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Palavras-chave: imagem de super-resolução, DNA-PAINT, organização da cromatina, speckles nucleares, inibição da transcrição