Clear Sky Science · nl
Hoge-snelheid gemultiplexte DNA-PAINT-beelden van kernorganisatie met een uitgebreidere sequentierepertoire
De celkern in nieuw detail zien
In elke cel is het genoom op een verfijnde manier gevouwen en gerangschikt die helpt te bepalen welke genen aan- of uitgezet worden. Tot voor kort was veel van deze interne architectuur te klein en te dicht opeengepakt om duidelijk te zien. Dit artikel beschrijft een snellere, krachtigere beeldvormingstechniek waarmee onderzoekers veel verschillende kerncomponenten tegelijk met bijna-moleculaire precisie in kaart kunnen brengen, en onthult hoe het genoom en de omringende structuren zich reorganiseren wanneer genactiviteit wordt stilgelegd.
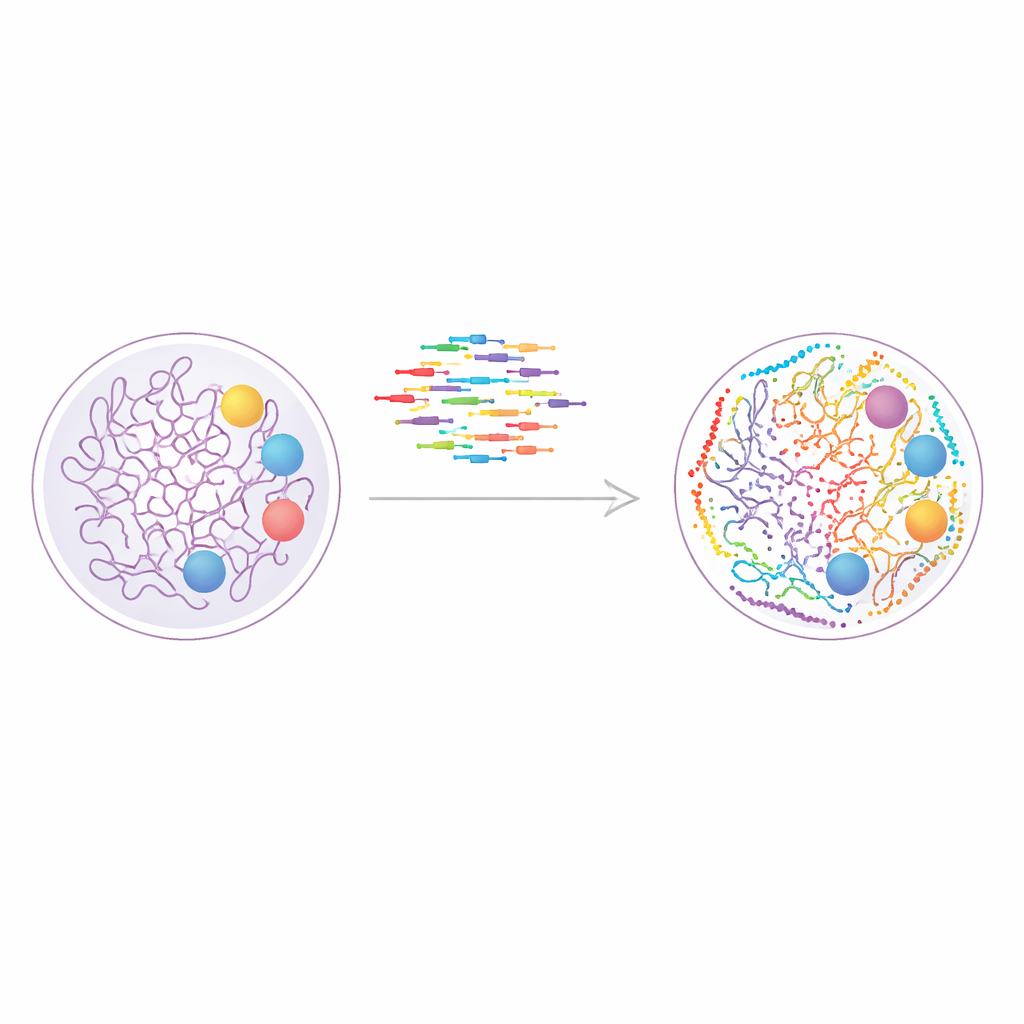
Een nieuwe manier om het genoom te 'verven'
De studie bouwt voort op een techniek genaamd DNA-PAINT, die korte fluorescerende DNA-strengen gebruikt die herhaaldelijk binden en loslaten aan corresponderende DNA-tags op cellulaire structuren. Elk bindingsgeval geeft een korte lichtflits, en veel van die gebeurtenissen samen kunnen worden samengevoegd om een scherp beeld te reconstrueren ver voorbij de limieten van gewone microscopen. DNA-PAINT leent zich van nature goed voor het bekijken van veel doelen in dezelfde cel, omdat elk eiwit of chromatinemerk met een onderscheidende DNA-sequentie kan worden gemarkeerd. Het probleem was de snelheid: traditionele sequentieontwerpen binden te traag, waardoor elke beeldronde uren kan duren.
Het kleurenpalet uitbreiden
Om deze bottleneck aan te pakken, ontwierpen de auteurs systematisch een breder pakket van "snelheids-geoptimaliseerde" DNA-sequenties die vaker binden terwijl ze toch specifiek blijven. Ze bouwden ontworpen DNA-nanostructuren, bekend als DNA-origami, om te testen hoe goed elke imager-streng zijn corresponderende dockingstreng herkende en hoe vaak deze oplichtte. Door origamitegels samen te stellen met dockingsites gerangschikt in een precies 4-bij-3 raster op slechts 20 nanometer afstand, konden ze zowel resolutie als ongewenste crosstalk meten. Dit werk leverde in totaal twaalf snelle sequenties op, waarvan er tien samen gebruikt konden worden zonder interferentie, waardoor directe beeldvorming van tot tien doelwitten in één experiment mogelijk werd.
Scherpere beelden in minder tijd
Niet alle snelle sequenties gedroegen zich op dezelfde manier. Een subset gaf langer durende bindingsgebeurtenissen, wat bijzonder nuttig bleek. Toen het team een kort-bindende en een lang-bindende sequentie vergeleek op hetzelfde origami-raster, gaf de lang-bindende probe een scherpere scheiding tussen aangrenzende sites en deed dit zelfs bij lagere laserkracht. Langere gebeurtenissen stelden de camera in staat meer fotonen van elke binding te verzamelen, waardoor de lokalisatieprecisie tot slechts enkele nanometers werd versterkt. Deze probes bemonsterden ook doelsites efficiënter, wat betrouwbare dekking in minder frames bereikte. In de praktijk betekent dit dat onderzoekers hoogwaardige superresolutiebeelden in minuten in plaats van uren kunnen verkrijgen, met een kleiner risico op schade aan het monster.
De nucleaire landschappen in kaart brengen
Gewapend met hun uitgebreide sequentieset gingen de onderzoekers van kunstmatige DNA-structuren naar levende celbiologie. Ze gebruikten DNA-PAINT om negen verschillende nucleaire kenmerken in menselijke cellen te beelden, waaronder actieve en gepauzeerde vormen van RNA-polymerase II, meerdere chemische tags op histon-eiwitten die actief of stil chromatine markeren, de nucleaire lamina aan de periferie, en nucleaire speckles—druppelachtige hubs die rijk zijn aan splitsingsfactoren. Door conventionele antilichamen aan DNA-dockingstrengen te koppelen en de doelen in negen opeenvolgende ronden te beelden, stelden ze een superresolutie, gemultiplexte kaart van de kern samen, waar elke stip overeenkomt met een moleculair buurtje van slechts een paar nanometer breed.
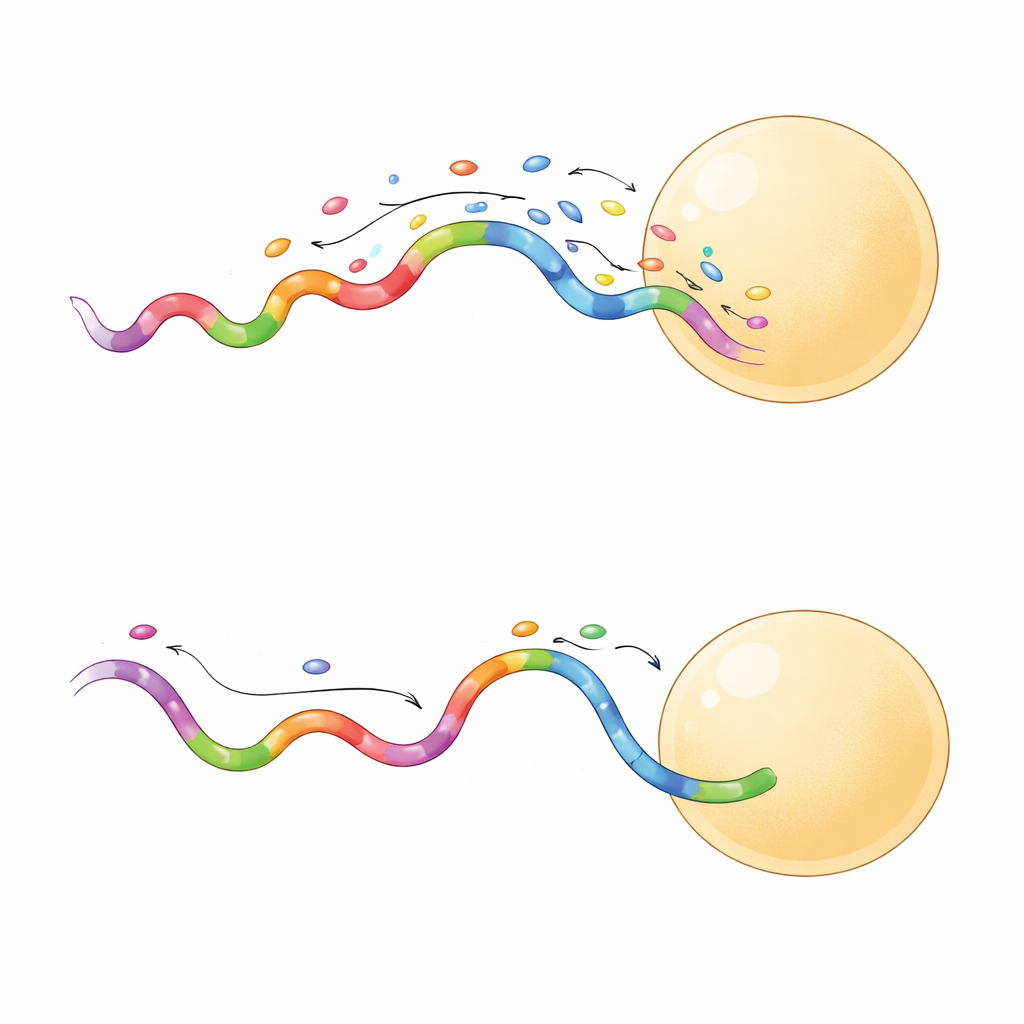
Chromatine zien reageren op stress
Het team vroeg zich vervolgens af hoe deze nucleaire kaart verandert wanneer transcriptie—het kopiëren van DNA naar RNA—wordt geblokkeerd. Het behandelen van cellen met het middel actinomycine D, dat RNA-polymerasen op DNA doet vastlopen, herschikte de ruimtelijke verhoudingen in de kern drastisch. Nucleaire speckles, die normaal onregelmatige omtrekken hebben en middenin actief chromatine liggen, werden ronder en hun nauwe contacten met transcriptieplaatsen en actieve histonmerken verdwenen grotendeels. Tegelijkertijd lieten repressieve chromatinemerken een versterkte associatie met de nucleaire lamina zien, wat consistent is met een compacter, stilgelegd genoom. Door meerdere lagen van statistische analyse te combineren konden de auteurs globale trends onderscheiden van lokale concentraties of uitsluitingen tussen verschillende nucleaire componenten.
Waarom dit belangrijk is voor de biologie
In wezen verandert dit werk DNA-PAINT in een sneller, veelzijdiger instrument om de innerlijke geografie van de cel in kaart te brengen. Met een grotere bibliotheek van snelheids-geoptimaliseerde DNA-sequenties kunnen wetenschappers nu veel nucleaire oriëntatiepunten in dezelfde cel volgen met nanometerresolutie en binnen praktische tijdschalen. De auteurs tonen aan dat deze aanpak gevoelig genoeg is om vast te leggen hoe chromatine losraakt van nucleaire speckles en zich aan de periferie verzamelt wanneer transcriptie wordt stopgezet. Naarmate de methode wordt uitgebreid naar meer eiwitten en modificaties, belooft ze gedetailleerde "atlassen" van nucleaire organisatie in gezondheid en ziekte, die helpen onthullen hoe genregulatie in drie dimensies is bekabeld.
Bronvermelding: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Trefwoorden: superresolutiebeeldvorming, DNA-PAINT, chromatineorganisatie, nucleaire speckles, transcriptieremming