Clear Sky Science · fr
Imagerie DNA-PAINT multiplexée à haute vitesse de l’organisation nucléaire grâce à un répertoire de séquences étendu
Voir le noyau cellulaire sous un nouveau jour
À l’intérieur de chacune de nos cellules, le génome est replié et disposé de façon complexe, ce qui contribue à contrôler quels gènes sont activés ou réprimés. Jusqu’à récemment, une grande partie de cette architecture interne était trop petite et trop dense pour être observée clairement. Cet article décrit une méthode d’imagerie plus rapide et plus puissante qui permet aux chercheurs de cartographier simultanément de nombreux composants nucléaires avec une précision quasi moléculaire, révélant comment le génome et ses structures environnantes se réorganisent lorsque l’activité génique est arrêtée.
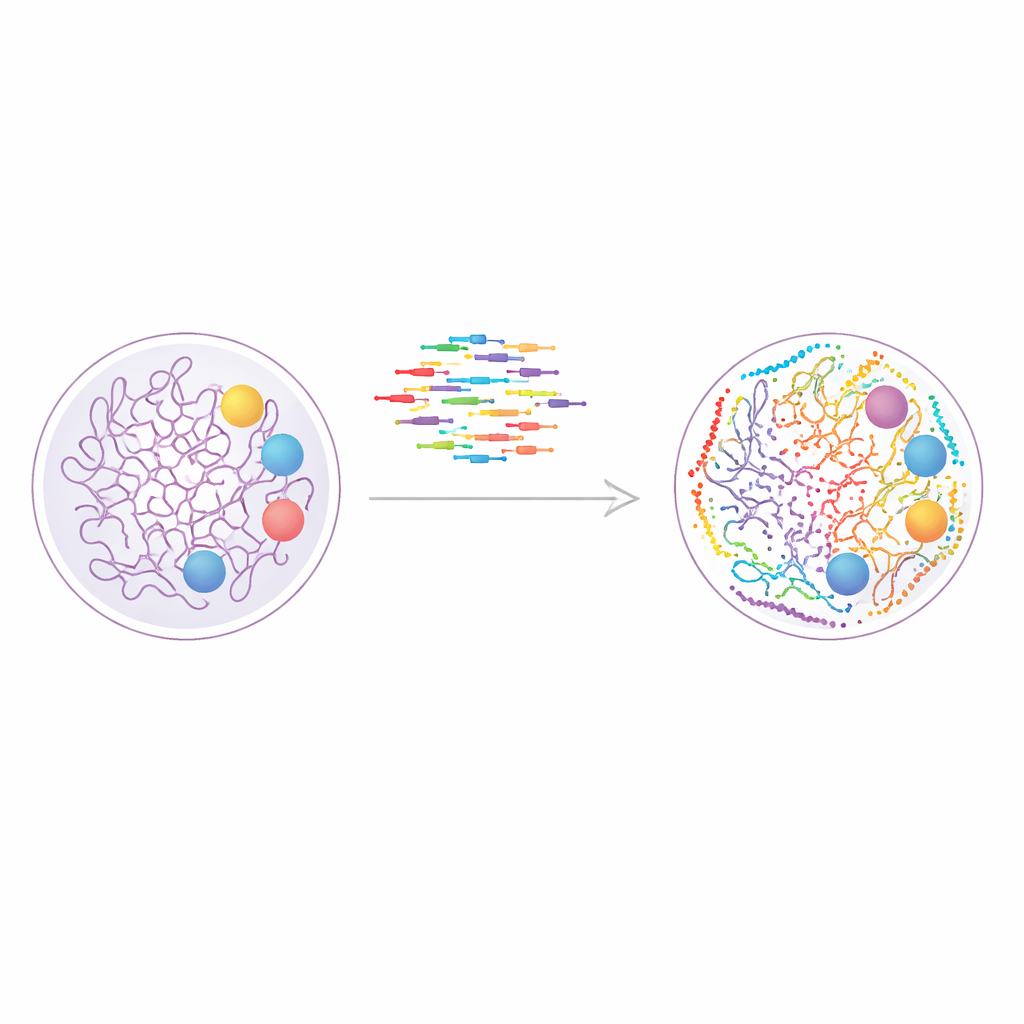
Une nouvelle façon de « peindre » le génome
L’étude s’appuie sur une technique appelée DNA-PAINT, qui utilise de courtes brins d’ADN fluorescents se liant et se délient de façon répétée à des étiquettes ADN complémentaires sur des structures cellulaires. Chaque événement de liaison produit une minuscule impulsion lumineuse, et la combinaison de nombreux événements permet de reconstruire une image nette bien au-delà des limites des microscopes conventionnels. DNA-PAINT se prête naturellement à l’observation de nombreuses cibles dans la même cellule, car chaque protéine ou marque de chromatine peut être marquée par une séquence d’ADN distincte. Le problème était la vitesse : les conceptions de séquences traditionnelles se lient trop lentement, transformant chaque cycle d’imagerie en une expérience de plusieurs heures.
Élargir la palette de couleurs
Pour résoudre ce goulot d’étranglement, les auteurs ont conçu de manière systématique un ensemble élargi de séquences d’ADN « optimisées pour la vitesse » qui se lient plus fréquemment tout en restant spécifiques. Ils ont construit des nanostructures d’ADN de synthèse, connues sous le nom d’origami d’ADN, pour tester la reconnaissance de chaque brin imageur par son site d’amarrage correspondant et la fréquence de ses signaux. En assemblant des tuiles d’origami portant des sites d’amarrage disposés en une grille précise de 4 par 3 espacée de seulement 20 nanomètres, ils ont pu mesurer à la fois la résolution et le bruit de parcours indésirable. Ce travail a abouti à douze séquences rapides au total, dont dix pouvaient être utilisées simultanément sans interférence, permettant l’imagerie directe allant jusqu’à dix cibles dans une même expérience.
Images plus nettes en moins de temps
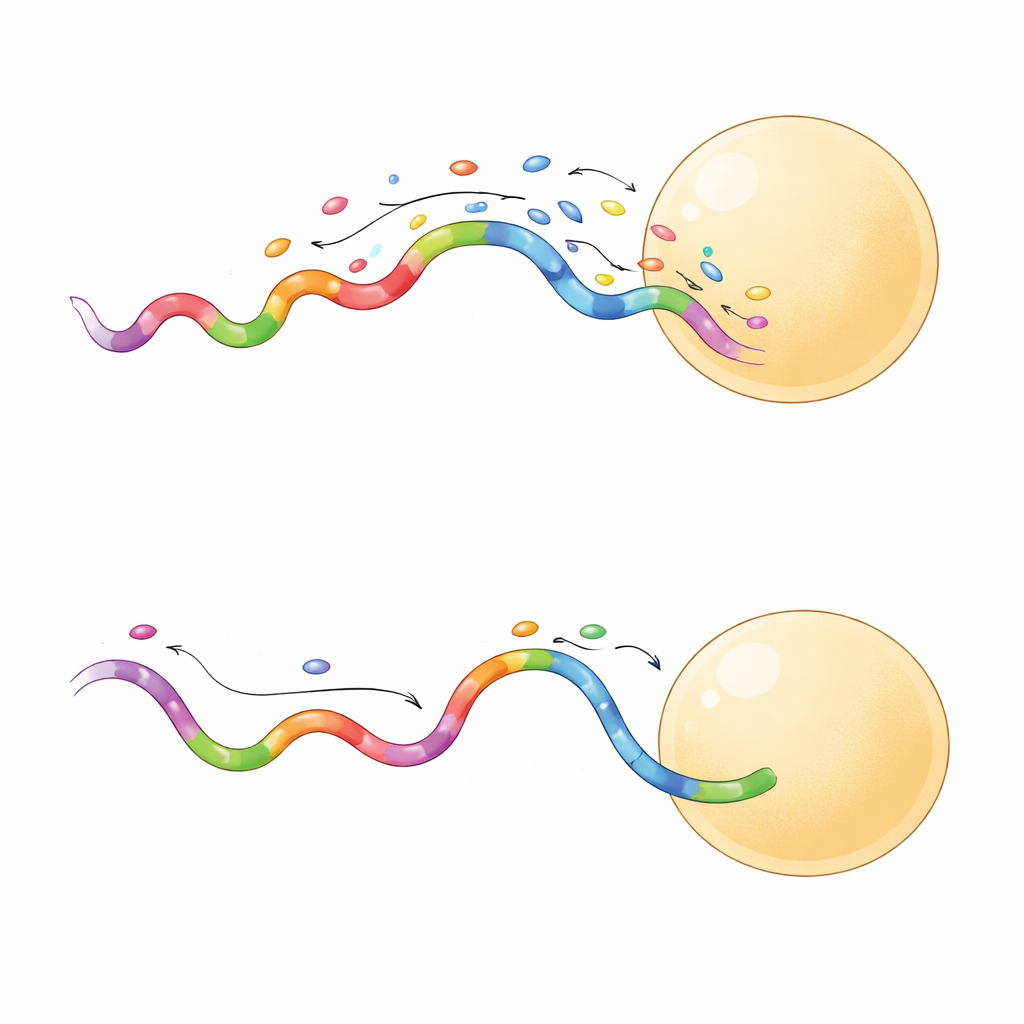
Toutes les séquences rapides ne se comportaient pas de la même façon. Un sous-ensemble produisait des événements de liaison de plus longue durée, qui se sont révélés particulièrement utiles. Lorsque l’équipe a comparé une séquence à liaison courte et une à liaison longue sur la même grille d’origami, la sonde à liaison longue a produit une séparation plus nette entre sites voisins et ce, même à une puissance laser plus faible. Des événements plus longs ont permis à la caméra de collecter davantage de photons par liaison, améliorant la précision de localisation à quelques nanomètres seulement. Ces sondes parcouraient aussi les sites cibles plus efficacement, atteignant une couverture fiable en moins de trames. En pratique, cela signifie que les chercheurs peuvent acquérir des images super-résolues de haute qualité en quelques minutes plutôt qu’en plusieurs heures, avec un risque moindre d’endommager l’échantillon.
Cartographier le paysage nucléaire
Munis de leur ensemble étendu de séquences, les chercheurs sont passés des structures d’ADN artificielles à la biologie cellulaire vivante. Ils ont utilisé DNA-PAINT pour imager neuf caractéristiques nucléaires différentes dans des cellules humaines, y compris les formes actives et « en pause » de l’ARN polymérase II, plusieurs marques chimiques sur les histones indiquant chromatine active ou silencieuse, la lamina nucléaire en périphérie, et les speckles nucléaires — des points semblables à des gouttelettes riches en facteurs d’épissage. En couplant des anticorps conventionnels à des brins d’amarrage en ADN et en imageant les cibles en neuf cycles séquentiels, ils ont assemblé une carte multiplexée et super-résolue du noyau, où chaque point correspond à un voisinage moléculaire de seulement quelques nanomètres de diamètre.
Observer la réaction de la chromatine au stress
L’équipe s’est ensuite intéressée à la façon dont cette carte nucléaire change lorsque la transcription — la copie de l’ADN en ARN — est bloquée. Le traitement des cellules par l’actinomycine D, qui bloque les ARN polymérases sur l’ADN, a profondément remodelé les relations spatiales à l’intérieur du noyau. Les speckles nucléaires, qui présentent normalement des contours irréguliers et se situent au milieu d’une chromatine active, sont devenus plus arrondis, et leurs contacts étroits avec les sites de transcription et les marques d’histones actives ont en grande partie disparu. En parallèle, les marques de chromatine répressive ont montré une association renforcée avec la lamina nucléaire, cohérente avec un génome plus compact et silencieux. En combinant plusieurs niveaux d’analyse statistique, les auteurs ont pu distinguer les tendances globales des poches locales d’enrichissement ou d’exclusion entre différents composants nucléaires.
Pourquoi c’est important pour la biologie
Essentiellement, ce travail transforme DNA-PAINT en un outil plus rapide et plus polyvalent pour cartographier la géographie interne de la cellule. Avec une bibliothèque plus large de séquences d’ADN optimisées pour la vitesse, les scientifiques peuvent désormais suivre de nombreux repères nucléaires dans une même cellule à une résolution de l’ordre du nanomètre et dans des délais pratiques. Les auteurs montrent que cette approche est suffisamment sensible pour capturer la façon dont la chromatine se détache des speckles nucléaires et se consolide en périphérie lorsque la transcription est arrêtée. À mesure que la méthode s’étendra à davantage de protéines et de modifications, elle promet des « atlas » détaillés de l’organisation nucléaire en santé et en maladie, contribuant à révéler comment la régulation génique est structurée en trois dimensions.
Citation: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Mots-clés: imagerie super-résolution, DNA-PAINT, organisation de la chromatine, speckles nucléaires, inhibition de la transcription