Clear Sky Science · de
Schnelle, multiplexe DNA-PAINT-Bildgebung der Kernorganisation mithilfe eines erweiterten Sequenzrepertoires
Den Zellkern in neuer Detailfülle sehen
Im Inneren jeder unserer Zellen ist das Genom auf komplexe Weise gefaltet und angeordnet, was mitreguliert, welche Gene ein- oder ausgeschaltet werden. Bis vor kurzem war ein Großteil dieser inneren Architektur zu klein und zu dicht gepackt, um sie klar zu erkennen. Dieses Paper beschreibt eine schnellere, leistungsfähigere Bildgebungsmethode, die Forschenden erlaubt, viele verschiedene nukleare Komponenten gleichzeitig mit nahezu molekularer Präzision zu kartieren und zu zeigen, wie sich das Genom und seine umgebenden Strukturen umorganisieren, wenn die Genaktivität abgeschaltet wird.
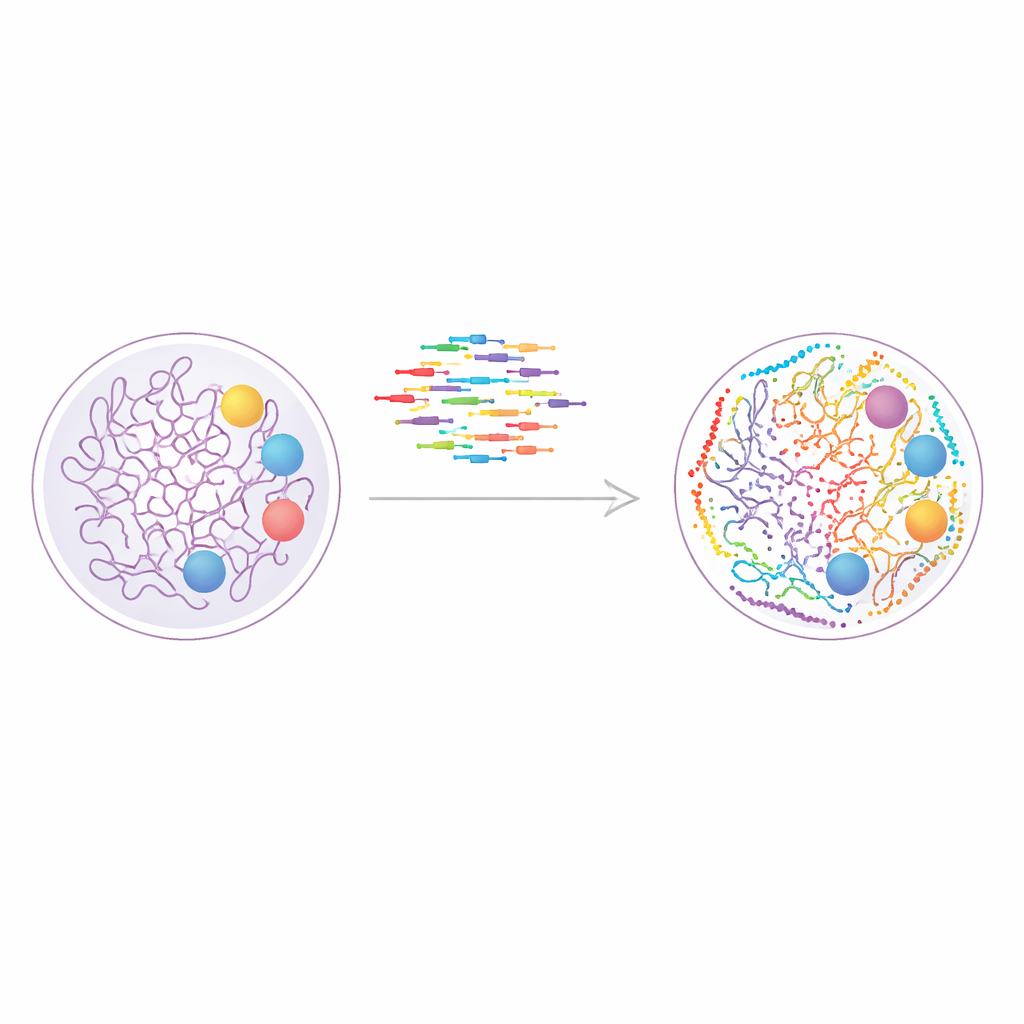
Eine neue Art, das Genom zu „malen"
Die Studie baut auf einer Technik namens DNA-PAINT auf, bei der kurze fluoreszierende DNA-Stränge wiederholt an passende DNA-Tags auf zellulären Strukturen binden und wieder dissoziieren. Jedes Bindungsereignis erzeugt einen kurzen Lichtblitz, und viele solcher Ereignisse lassen sich kombinieren, um ein scharfes Bild weit jenseits der Grenzen gewöhnlicher Mikroskope zu rekonstruieren. DNA-PAINT eignet sich besonders gut, um viele Ziele in derselben Zelle zu untersuchen, weil jedes Protein oder jede Chromatinmarkierung mit einer eigenen DNA-Sequenz versehen werden kann. Das Problem war die Geschwindigkeit: herkömmliche Sequenzdesigns binden zu langsam und machen jede Bildgebungsrunde zu einem stundenlangen Experiment.
Die Farbpalette erweitern
Um diesen Engpass zu beheben, entwarfen die Autorinnen und Autoren systematisch eine größere Reihe „geschwindigkeitsoptimierter" DNA-Sequenzen, die häufiger binden und gleichzeitig spezifisch bleiben. Sie bauten dafür Designer-DNA-Nanostrukturen, bekannt als DNA-Origami, um zu testen, wie gut jeder Imager-Strang seinen passenden Docking-Strang erkennt und wie häufig er aufleuchtet. Durch das Zusammenbauen von Origami-Fliesen mit Docking-Stellen in einem präzisen 4-mal-3-Gitter im Abstand von nur 20 Nanometern konnten sie sowohl die Auflösung als auch unerwünschten Crosstalk messen. Diese Arbeit ergab insgesamt zwölf schnelle Sequenzen, von denen zehn zusammen verwendet werden konnten, ohne sich gegenseitig zu stören, sodass in einem Experiment direkt bis zu zehn Ziele abgebildet werden konnten.
Scharfere Bilder in kürzerer Zeit
Nicht alle schnellen Sequenzen verhielten sich gleich. Ein Teil produzierte länger anhaltende Bindungsereignisse, die sich als besonders nützlich erwiesen. Als das Team eine kurzbindende und eine langbindende Sequenz auf demselben Origami-Gitter verglich, lieferte die langbindende Sonde eine deutlichere Trennung benachbarter Stellen und das sogar bei niedrigerer Laserleistung. Längere Ereignisse ermöglichten es der Kamera, mehr Photonen pro Bindung zu sammeln, was die Lokalisierungspräzision auf nur wenige Nanometer erhöhte. Diese Sonden tasteten Zielstellen außerdem effizienter ab und erreichten in weniger Frames eine zuverlässige Abdeckung. In der Praxis bedeutet das, dass Forschende hochqualitative, superaufgelöste Bilder in Minuten statt Stunden aufnehmen können, bei geringerem Risiko der Probenschädigung.
Die nukleare Landschaft kartieren
Mit ihrem erweiterten Sequenzsatz wechselten die Forschenden von künstlichen DNA-Strukturen zur lebenden Zellbiologie. Sie nutzten DNA-PAINT, um neun verschiedene nukleare Merkmale in menschlichen Zellen zu bildgeben, darunter aktive und pausierte Formen der RNA-Polymerase II, mehrere chemische Markierungen auf Histonproteinen, die aktives oder stilles Chromatin kennzeichnen, die Kernlamina am Peripheriebereich und nukleäre Speckles — tropfenähnliche Hubs, die reich an Spleißfaktoren sind. Durch die Kopplung konventioneller Antikörper an DNA-Docking-Stränge und das sequenzielle Bildgeben der Ziele in neun aufeinanderfolgenden Runden stellten sie eine superaufgelöste, multiplexe Karte des Kerns zusammen, bei der jeder Punkt einer molekularen Nachbarschaft von nur wenigen Nanometern entspricht.
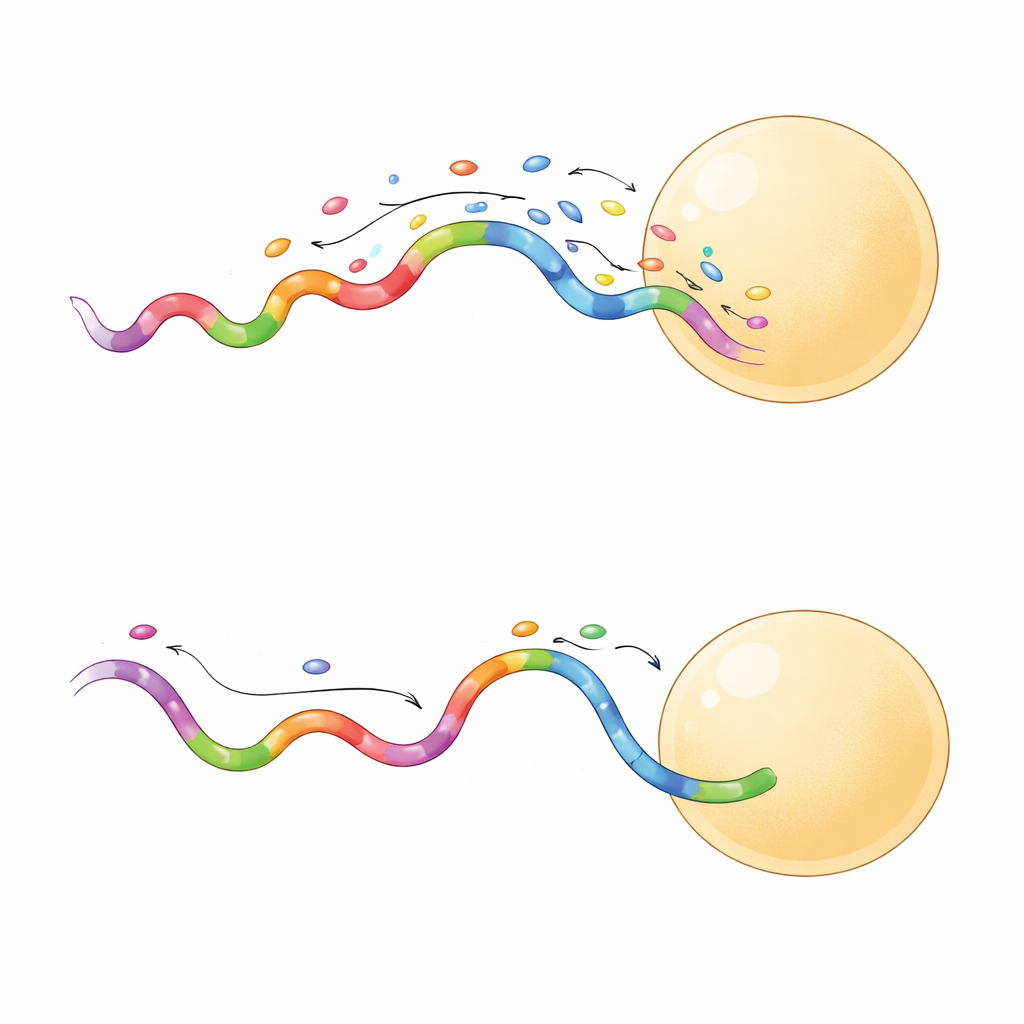
Zuschauen, wie Chromatin auf Stress reagiert
Das Team fragte dann, wie sich diese nukleare Karte verändert, wenn die Transkription — das Kopieren von DNA in RNA — blockiert wird. Die Behandlung der Zellen mit dem Wirkstoff Actinomycin D, der RNA-Polymerasen auf der DNA zum Stillstand bringt, veränderte die räumlichen Beziehungen im Kern dramatisch. Nukleäre Speckles, die normalerweise unregelmäßige Umrisse haben und inmitten aktiven Chromatins liegen, wurden runder, und ihre engen Kontakte zu Transkriptionsorten und aktiven Histonmarken verschwanden weitgehend. Gleichzeitig zeigten repressive Chromatinmarken eine verstärkte Assoziation mit der Kernlamina, was mit einem kompakteren, stummgeschalteten Genom übereinstimmt. Durch die Kombination mehrerer statistischer Analyseebenen konnten die Autorinnen und Autoren globale Trends von lokalen Bereichen mit Anreicherung oder Ausschluss zwischen verschiedenen nuklearen Komponenten unterscheiden.
Warum das für die Biologie wichtig ist
Im Kern verwandelt diese Arbeit DNA-PAINT in ein schnelleres, vielseitigeres Werkzeug zur Kartierung der inneren Geografie der Zelle. Mit einer größeren Bibliothek geschwindigkeitsoptimierter DNA-Sequenzen können Wissenschaftlerinnen und Wissenschaftler nun viele nukleare Orientierungspunkte in derselben Zelle mit Nanometerauflösung und in praktikablen Zeiträumen verfolgen. Die Autorinnen und Autoren zeigen, dass dieser Ansatz empfindlich genug ist, um einzufangen, wie sich Chromatin von nukleären Speckles löst und sich am Peripheriebereich zusammenzieht, wenn die Transkription gestoppt wird. Wenn die Methode auf weitere Proteine und Modifikationen ausgeweitet wird, verspricht sie detaillierte "Atlanten" der Kernorganisation in Gesundheit und Krankheit und hilft zu offenbaren, wie Genregulation dreidimensional verschaltet ist.
Zitation: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Schlüsselwörter: Superauflösende Bildgebung, DNA-PAINT, Chromatinorganisation, Nukleäre Speckles, Transkriptionshemmung