Clear Sky Science · pl
Szybkie wielopasmowe obrazowanie DNA-PAINT organizacji jądra komórkowego z wykorzystaniem rozszerzonego repertuaru sekwencji
Widzieć jądro komórkowe w nowym detalu
Wnętrze każdej naszej komórki zawiera genom złożony i ułożony w sposób, który pomaga kontrolować, które geny są aktywne, a które wyciszone. Jeszcze niedawno wiele z tej wewnętrznej architektury było zbyt małe i zatłoczone, by można je było zobaczyć wyraźnie. W tym artykule opisano szybszą, bardziej wydajną metodę obrazowania, która pozwala badaczom mapować wiele różnych składników jądra jednocześnie z niemal molekularną precyzją, ujawniając, jak genom i otaczające go struktury reorganizują się, gdy aktywność genów zostaje zatrzymana.
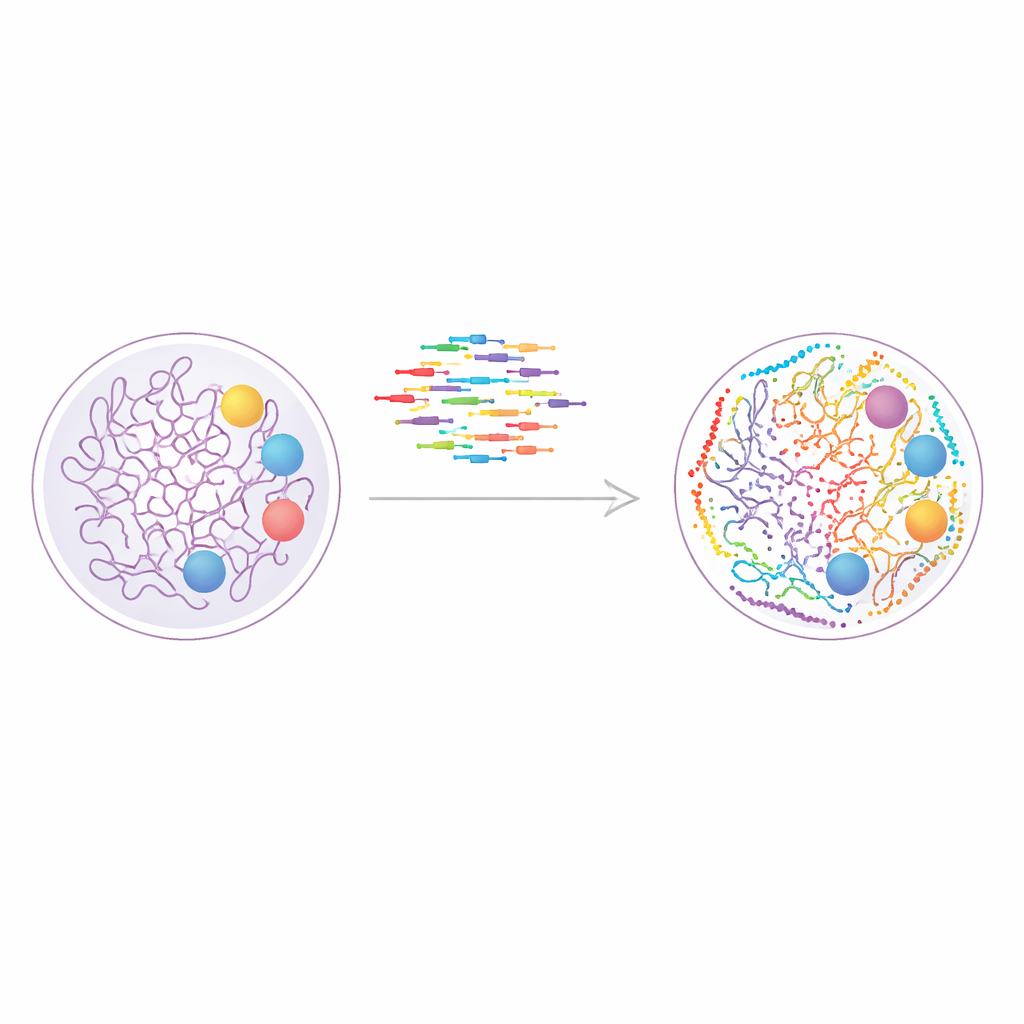
Nowy sposób „malowania” genomu
Badanie opiera się na technice zwanej DNA-PAINT, która wykorzystuje krótkie fluorescencyjne fragmenty DNA, wielokrotnie wiążące się i odłączające od dopasowanych znaczników DNA na strukturach komórkowych. Każde zdarzenie wiązania generuje krótką iskrę światła, a wiele takich zdarzeń można połączyć, aby odtworzyć ostry obraz daleko wykraczający poza ograniczenia zwykłych mikroskopów. DNA-PAINT naturalnie nadaje się do obserwacji wielu celów w tej samej komórce, ponieważ każdy białko lub znacznik chromatyny można otagować unikalną sekwencją DNA. Problemem była prędkość: tradycyjne projekty sekwencji wiążą się zbyt wolno, zamieniając każde koło obrazowania w eksperyment trwający godziny.
Rozszerzanie palety kolorów
Aby rozwiązać to wąskie gardło, autorzy systematycznie zaprojektowali szerszy zestaw „optymalizowanych pod kątem szybkości” sekwencji DNA, które wiążą się częściej, jednocześnie pozostając specyficzne. Zbudowali zaprojektowane nanostruktury DNA, znane jako DNA origami, aby przetestować, jak dobrze każda nić imerowa rozpoznaje odpowiadającą jej nić dokującą i jak często emitowała błysk. Składając płytki origami, które miały miejsca dokujące rozmieszczone w precyzyjnej siatce 4 na 3 oddalonej o zaledwie 20 nanometrów, mogli mierzyć zarówno rozdzielczość, jak i niepożądane zakłócenia krzyżowe. Ta praca dała w sumie dwanaście szybkich sekwencji, z których dziesięć mogło być użytych razem bez interferencji, umożliwiając bezpośrednie obrazowanie do dziesięciu celów w jednym eksperymencie.
Ostre obrazy w krótszym czasie
Nie wszystkie szybkie sekwencje zachowywały się jednakowo. Podzbiór generował dłużej trwające zdarzenia wiązania, które okazały się szczególnie przydatne. Gdy zespół porównał sekwencję krótkowiążącą i długowiążącą na tej samej siatce origami, sonda długowiążąca zapewniła ostrzejsze rozdzielenie sąsiednich miejsc i robiła to nawet przy niższej mocy lasera. Dłuższe zdarzenia pozwalały kamerze zebrać więcej fotonów z każdego wiązania, zwiększając precyzję lokalizacji do zaledwie kilku nanometrów. Te sondy również bardziej efektywnie próbkowały miejsca docelowe, osiągając niezawodne pokrycie przy mniejszej liczbie klatek. W praktyce oznacza to, że badacze mogą uzyskać wysokiej jakości obrazy o nadrozdzielczości w ciągu minut zamiast godzin, przy mniejszym ryzyku uszkodzenia próbki.
Mapowanie krajobrazu jądrowego
Uzbrojeni w rozszerzony zestaw sekwencji, badacze przenieśli się od sztucznych struktur DNA do biologii komórek żywych. Użyli DNA-PAINT do obrazowania dziewięciu różnych cech jądra w komórkach ludzkich, w tym aktywnych i zatrzymanych form polimerazy RNA II, kilku chemicznych znaczników na białonach histonowych wskazujących chromatynę aktywną lub cichą, laminy jądrowej na obwodzie oraz plamek jądrowych — przypominających krople centrów bogatych w czynniki splicingowe. Łącząc konwencjonalne przeciwciała ze stnadkami dokującymi DNA i obrazując cele w dziewięciu kolejnych rundach, złożyli super-rozdzielczą, wielopasmową mapę jądra, w której każda kropka odpowiada sąsiedztwu molekularnemu o rozmiarach zaledwie kilku nanometrów.
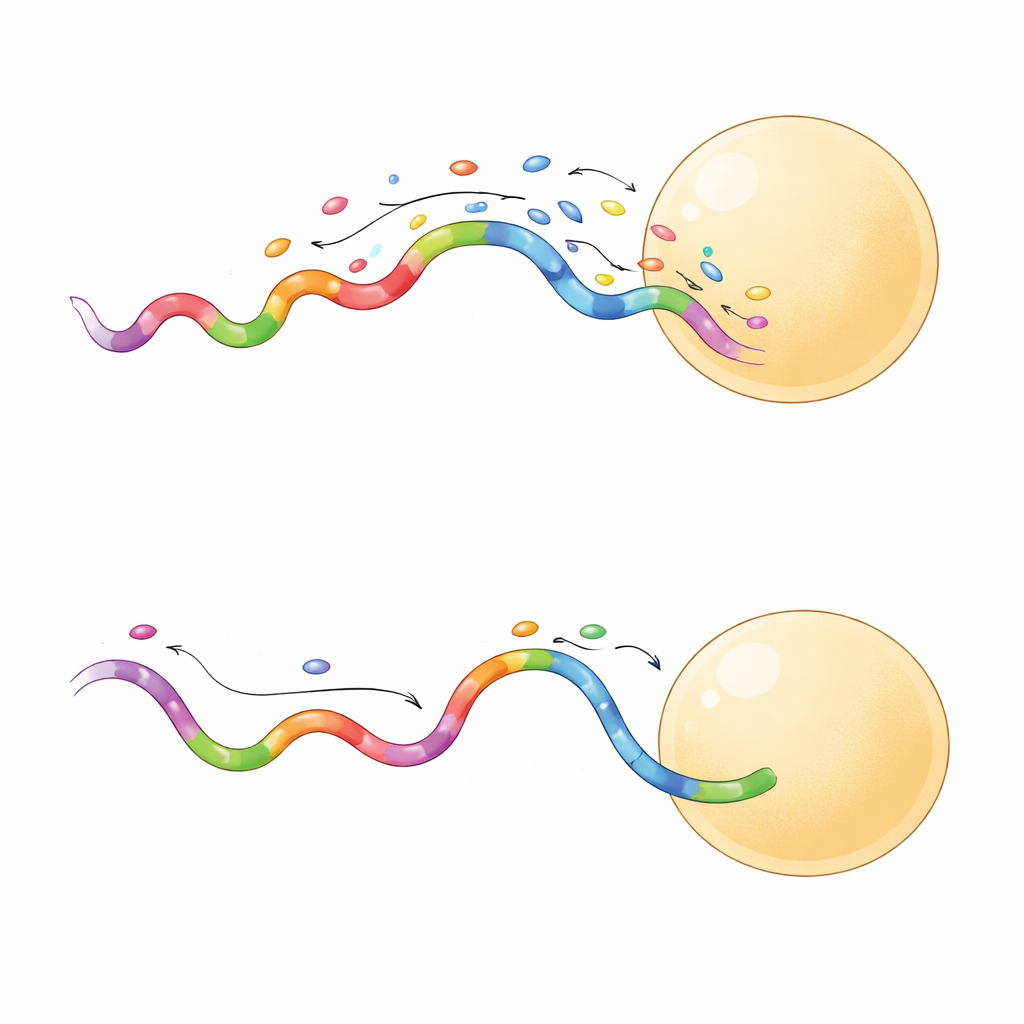
Obserwowanie reakcji chromatyny na stres
Zespół następnie zapytał, jak ta mapa jądrowa zmienia się, gdy transkrypcja — przepisywanie DNA na RNA — zostaje zablokowana. Leczenie komórek lekiem aktinomicyną D, który zatrzymuje polimerazy RNA na DNA, dramatycznie przekształciło przestrzenne relacje wewnątrz jądra. Plamki jądrowe, które zwykle mają nieregularne kontury i znajdują się wśród aktywnej chromatyny, stały się bardziej zaokrąglone, a ich bliskie kontakty z miejscami transkrypcji i aktywnymi znacznikami histonowymi w dużej mierze zniknęły. Jednocześnie represyjne znaczniki chromatyny wykazały wzmocnione powiązanie z laminą jądrową, co zgadza się z bardziej skompaktowanym, wyciszonym genomem. Poprzez połączenie kilku warstw analizy statystycznej autorzy mogli odróżnić globalne trendy od lokalnych kieszeni wzbogacenia lub wykluczenia pomiędzy różnymi składnikami jądra.
Dlaczego to ma znaczenie dla biologii
W istocie praca ta przekształca DNA-PAINT w szybsze, bardziej wszechstronne narzędzie do mapowania wewnętrznej geografii komórki. Dzięki większej bibliotece sekwencji zoptymalizowanych pod względem szybkości naukowcy mogą teraz śledzić wiele punktów orientacyjnych jądra w tej samej komórce na skali nanometrów i w praktycznym czasie. Autorzy pokazują, że podejście to jest wystarczająco czułe, by uchwycić, jak chromatyna odłącza się od plamek jądrowych i konsoliduje się przy obwodzie, gdy transkrypcja zostaje zahamowana. W miarę rozszerzania metody na większą liczbę białek i modyfikacji, obiecuje to szczegółowe „atlasy” organizacji jądra w zdrowiu i chorobie, pomagając ujawnić, jak regulacja genów jest zorganizowana w trzech wymiarach.
Cytowanie: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Słowa kluczowe: obrazowanie o nadrozdzielczości, DNA-PAINT, organizacja chromatyny, plamki jądrowe, hamowanie transkrypcji