Clear Sky Science · es
Imágenes multiplexadas de alta velocidad con DNA-PAINT de la organización nuclear usando un repertorio de secuencias ampliado
Ver el núcleo celular con nuevo detalle
Dentro de cada una de nuestras células, el genoma se pliega y organiza de manera intrincada que ayuda a controlar qué genes se activan o silencian. Hasta hace poco, gran parte de esta arquitectura interna era demasiado pequeña y compacta para observarse con claridad. Este artículo describe un método de imagen más rápido y potente que permite a los investigadores mapear muchos componentes nucleares a la vez con precisión casi molecular, revelando cómo el genoma y sus estructuras circundantes se reorganizan cuando la actividad génica se detiene.
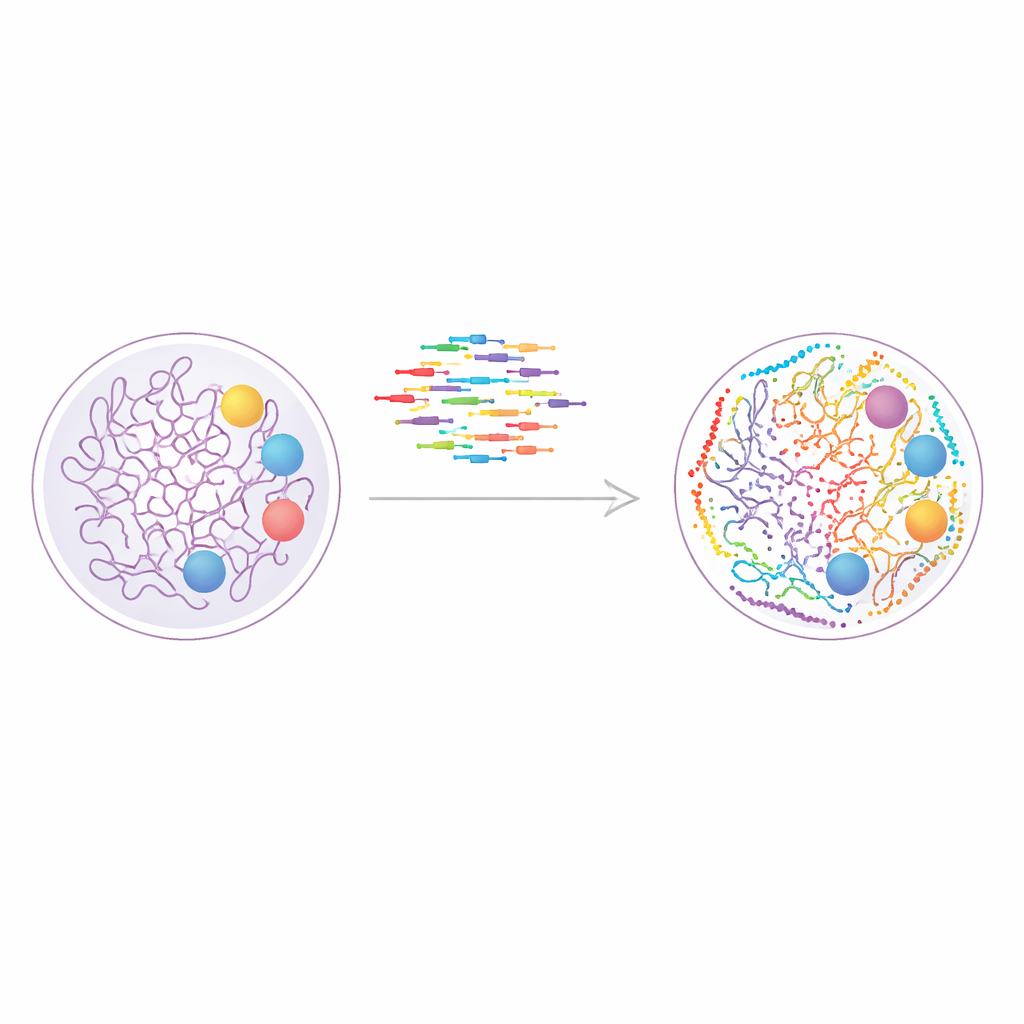
Una nueva forma de pintar el genoma
El estudio se basa en una técnica llamada DNA-PAINT, que utiliza hebras cortas de ADN fluorescente que se unen y se separan repetidamente de etiquetas de ADN coincidentes en las estructuras celulares. Cada evento de unión produce un pequeño destello de luz, y muchos de esos eventos pueden combinarse para reconstruir una imagen nítida muy por encima de los límites de los microscopios ordinarios. DNA-PAINT es de por sí adecuado para observar múltiples dianas en la misma célula, porque cada proteína o marca de cromatina puede etiquetarse con una secuencia de ADN distinta. El problema ha sido la velocidad: los diseños de secuencias tradicionales se unen demasiado despacio, convirtiendo cada ronda de imagen en un experimento de horas de duración.
Ampliando la paleta de colores
Para abordar este cuello de botella, los autores diseñaron sistemáticamente un conjunto más amplio de secuencias «optimizadas para la velocidad» que se unen con mayor frecuencia manteniendo la especificidad. Construyeron nanoestructuras de ADN diseñadas, conocidas como origami de ADN, para probar qué tan bien cada hebra imager reconocía su hebra docking correspondiente y con qué frecuencia emitía destellos. Al ensamblar losetas de origami que llevaban sitios docking dispuestos en una cuadrícula precisa de 4 por 3 con apenas 20 nanómetros de separación, pudieron medir tanto la resolución como el cruce no deseado entre señales. Este trabajo produjo en total doce secuencias rápidas, de las cuales diez podían usarse juntas sin interferencias, posibilitando la imagen directa de hasta diez dianas en un solo experimento.
Imágenes más nítidas en menos tiempo
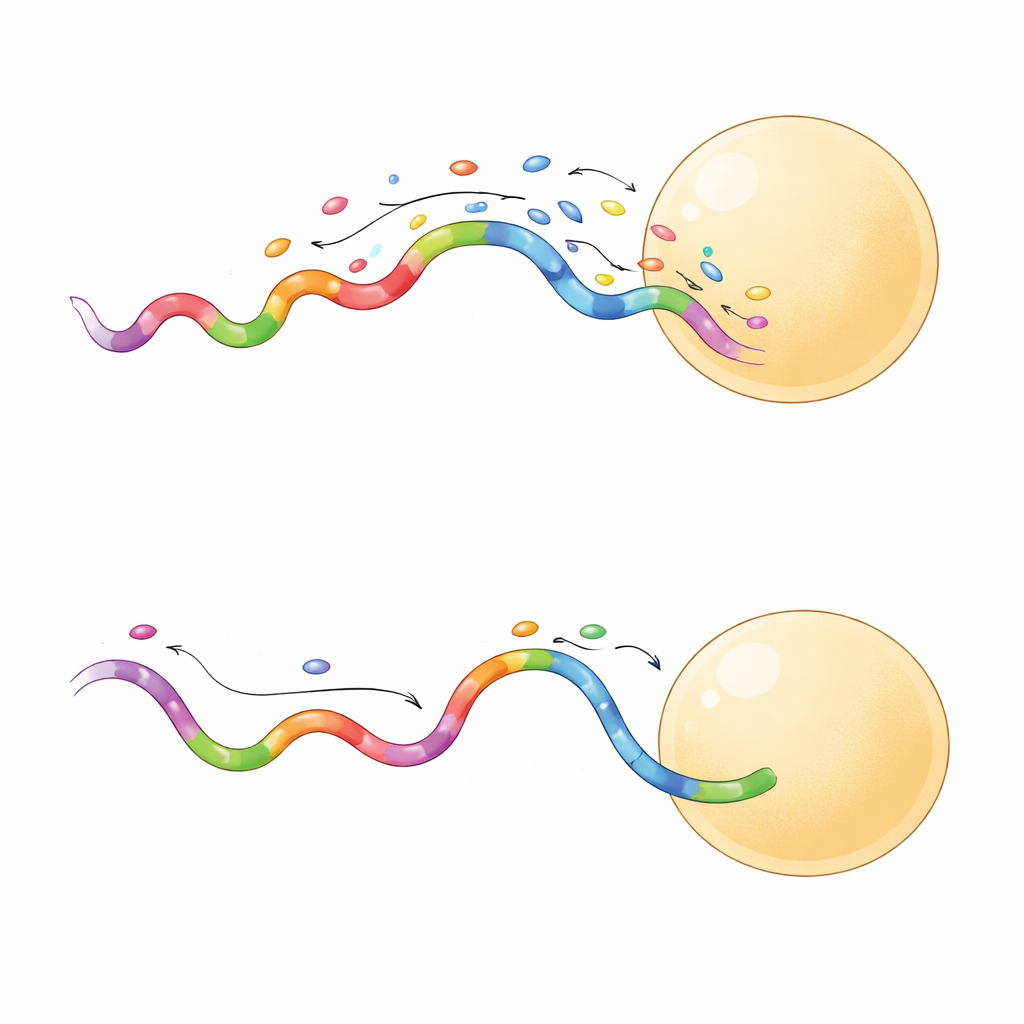
No todas las secuencias rápidas se comportaron igual. Un subconjunto produjo eventos de unión de mayor duración, que resultaron ser especialmente útiles. Cuando el equipo comparó una secuencia de unión corta y una de unión larga en la misma cuadrícula de origami, la sonda de unión larga proporcionó una separación más nítida entre sitios vecinos e incluso lo hizo con menor potencia láser. Los eventos más largos permitieron que la cámara recogiera más fotones de cada unión, mejorando la precisión de localización a apenas unos pocos nanómetros. Estas sondas también muestrearon los sitios objetivo de forma más eficiente, alcanzando una cobertura fiable en menos fotogramas. En la práctica, esto significa que los investigadores pueden adquirir imágenes superresueltas de alta calidad en minutos en lugar de horas, con menor riesgo de dañar la muestra.
Mapeando el paisaje nuclear
Armados con su conjunto ampliado de secuencias, los investigadores pasaron de estructuras de ADN artificiales a biología celular real. Usaron DNA-PAINT para visualizar nueve características nucleares diferentes en células humanas, incluidas formas activas y en pausa de la ARN polimerasa II, varias marcas químicas en histonas que señalan cromatina activa o silenciosa, la lámina nuclear en la periferia y las manchas nucleares: centros tipo gotícula ricos en factores de empalme. Al acoplar anticuerpos convencionales a hebras docking de ADN e imaginar las dianas en nueve rondas secuenciales, ensamblaron un mapa multiplexado y superresuelto del núcleo, donde cada punto corresponde a un vecindario molecular de apenas unos nanómetros de diámetro.
Observando cómo la cromatina responde al estrés
El equipo preguntó luego cómo cambia este mapa nuclear cuando la transcripción —la copia del ADN a ARN— se bloquea. El tratamiento de las células con el fármaco actinomicina D, que detiene a las ARN polimerasas sobre el ADN, reconfiguró drásticamente las relaciones espaciales dentro del núcleo. Las manchas nucleares, que normalmente tienen contornos irregulares y se sitúan en medio de cromatina activa, se volvieron más redondeadas y sus contactos cercanos con sitios de transcripción y marcas de histonas activas desaparecieron en gran medida. Al mismo tiempo, las marcas de cromatina represiva mostraron una asociación reforzada con la lámina nuclear, coherente con un genoma más compacto y silenciado. Al combinar varias capas de análisis estadístico, los autores pudieron distinguir tendencias globales de bolsillos locales de enriquecimiento o exclusión entre distintos componentes nucleares.
Por qué esto importa para la biología
En esencia, este trabajo convierte a DNA-PAINT en una herramienta más rápida y versátil para cartografiar la geografía interna de la célula. Con una biblioteca más amplia de secuencias optimizadas para la velocidad, los científicos pueden ahora rastrear muchos hitos nucleares en la misma célula con resolución nanométrica y en tiempos prácticos. Los autores demuestran que este enfoque es lo bastante sensible como para captar cómo la cromatina se separa de las manchas nucleares y se consolida en la periferia cuando la transcripción se detiene. A medida que el método se extienda a más proteínas y modificaciones, promete producir “atlas” detallados de la organización nuclear en salud y enfermedad, ayudando a revelar cómo se organiza la regulación génica en tres dimensiones.
Cita: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Palabras clave: imágenes de súperresolución, DNA-PAINT, organización de la cromatina, manchas nucleares, inhibición de la transcripción