Clear Sky Science · ja
拡張された配列レパートリーを用いた核内構造の高速多重化DNA-PAINTイメージング
細胞核を新たな細部で見る
我々の細胞それぞれの内部では、ゲノムが折りたたまれ、配置されることでどの遺伝子がオン/オフになるかを制御する複雑な構造が形成されています。これまでは、この内部構造の多くが小さすぎたり混み合っていたりして明瞭に観察することができませんでした。本論文は、より高速で強力なイメージング法を紹介し、研究者がほぼ分子レベルの精度で多くの異なる核内構成要素を同時にマッピングできるようにし、遺伝子活動が停止したときにゲノムとその周辺構造がどのように再編されるかを明らかにします。
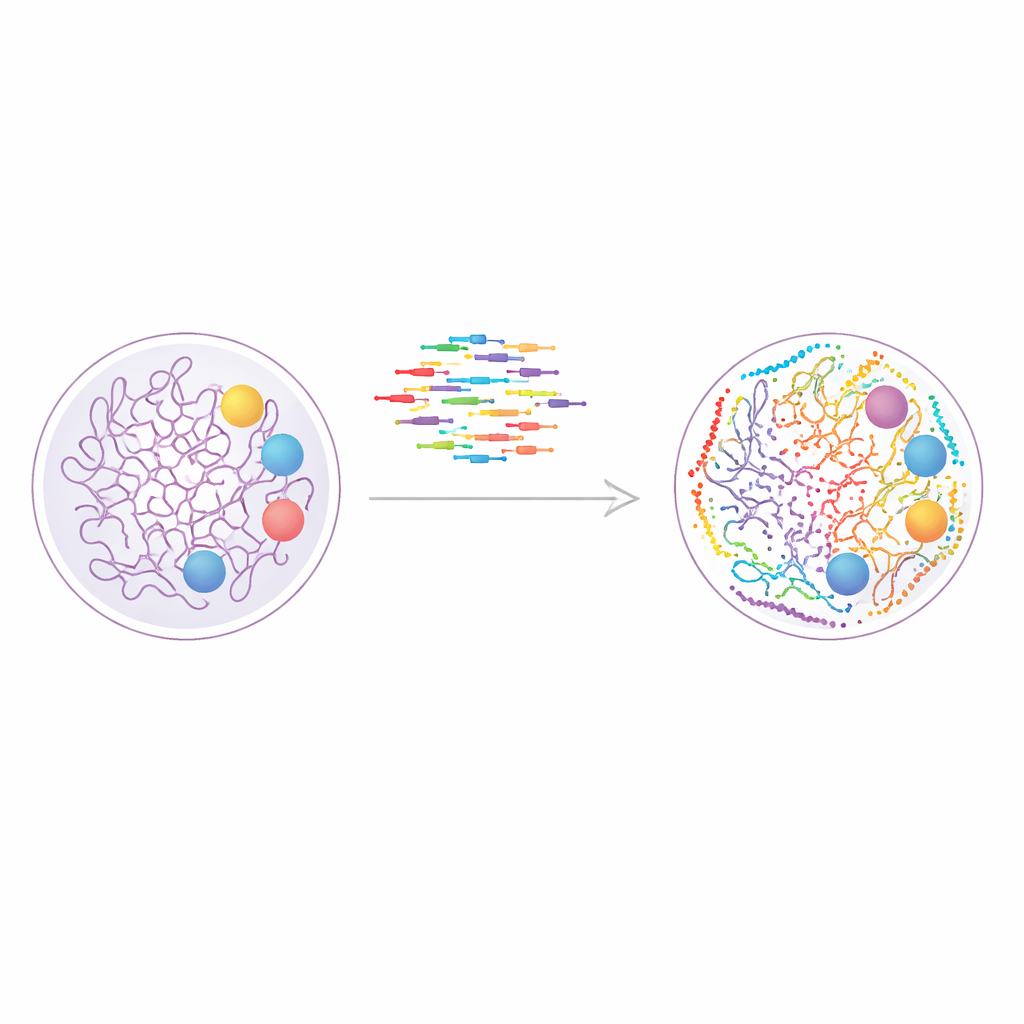
ゲノムを塗り分ける新しい方法
この研究はDNA-PAINTと呼ばれる手法に基づいています。DNA-PAINTは、短い蛍光標識されたDNA鎖が細胞構造上の対応するDNAタグに繰り返し結合・解離することを利用します。各結合イベントは微小な光のバーストを生み、多数のイベントを組み合わせることで通常の顕微鏡の限界をはるかに超えたシャープな像を再構成できます。DNA-PAINTは本質的に同一細胞内の多数のターゲットを観察するのに適しています。なぜなら各タンパク質やクロマチン修飾を異なるDNA配列でタグ付けできるためです。問題は速度でした。従来の配列設計は結合が遅すぎ、各イメージングラウンドが数時間に及ぶ実験になってしまいます。
カラーパレットを拡張する
このボトルネックに対処するため、著者らは系統的により広いセットの「速度最適化」DNA配列を設計し、特異性を保ちながらより頻繁に結合するようにしました。彼らはデザイナーDNAナノ構造(DNAオリガミ)を用いて、各イマージャー鎖が対応するドッキング鎖をどれだけよく認識するか、どのくらい頻繁に発光するかを試験しました。ドッキング部位を正確な4×3グリッドに20ナノメートル間隔で配置したオリガミタイルを組み立てることで、分解能と望ましくないクロストークの両方を測定できました。この作業により合計で12種類の高速配列が得られ、そのうち10種類は互いに干渉することなく併用可能で、1つの実験で最大10のターゲットを直接イメージングできるようになりました。
短時間でより鮮明な画像
すべての高速配列が同じ挙動を示したわけではありません。一部の配列はより長く持続する結合イベントを生み出し、これが特に有用であることがわかりました。同じオリガミグリッド上で短結合配列と長結合配列を比較したところ、長結合プローブは隣接サイト間の分離をより鮮明に示し、しかも低いレーザー出力でもそれを達成しました。結合イベントが長いことでカメラは各結合からより多くの光子を収集でき、局在精度は数ナノメートルにまで向上しました。これらのプローブはターゲットサイトをより効率的にサンプリングし、より少ないフレームで信頼できるカバレッジに到達しました。実際には、これにより研究者はサンプルを傷めるリスクを減らしつつ、数時間ではなく数分で高品質な超解像画像を取得できるようになります。
核内ランドスケープのマッピング
拡張された配列セットを武器に、研究者らは人工DNA構造から生きた細胞生物学へと応用を進めました。彼らはDNA-PAINTを用いてヒト細胞内の9種類の異なる核特徴をイメージングしました。対象には、活性型および一時停止型のRNAポリメラーゼII、活性あるいはサイレントなクロマチンを示すヒストンタンパク質の複数の化学的タグ、細胞周辺の核ラミナ、およびスプライシング因子が豊富な液滴状のハブである核スピークルが含まれます。従来の抗体をDNAドッキング鎖と結合させ、9ラウンドの連続イメージングでターゲットを取得することで、各点が数ナノメートルの分子近傍を表す超解像多重化核マップを構築しました。
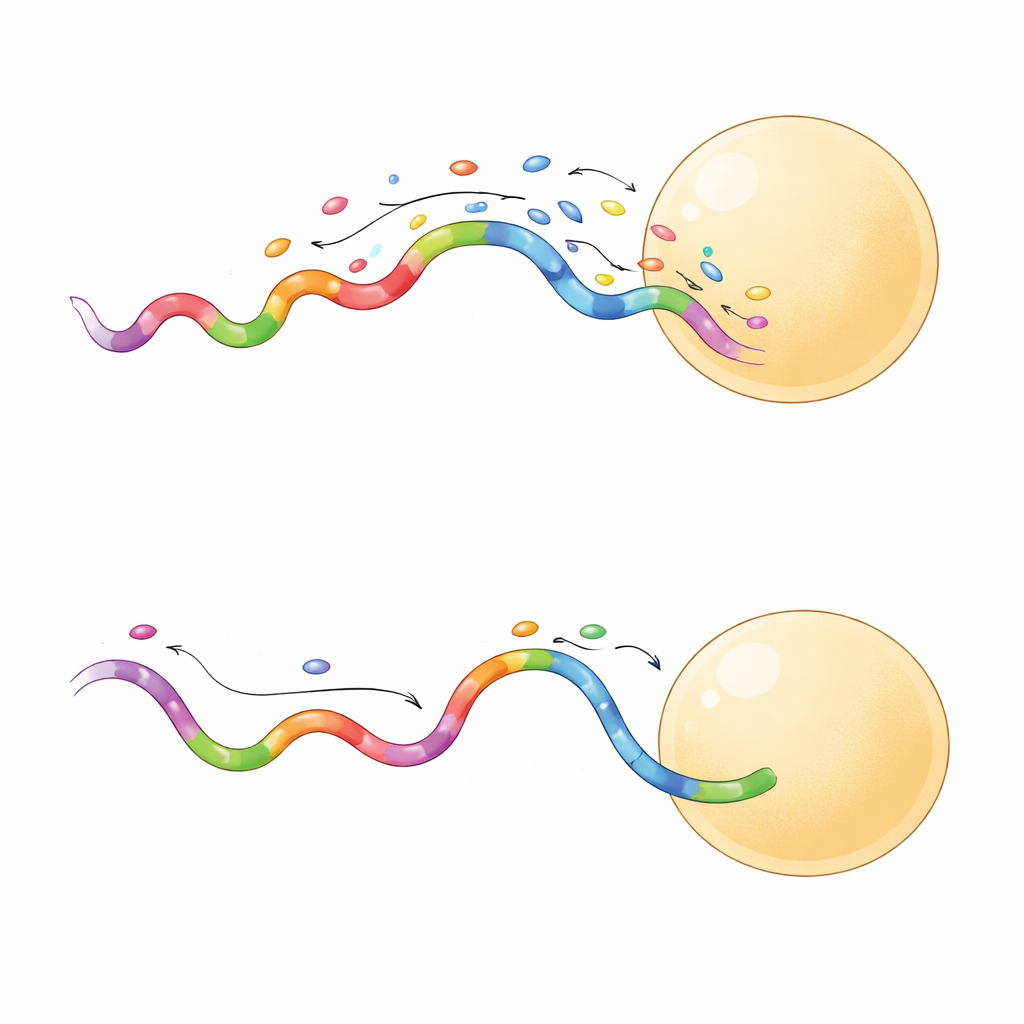
クロマチンがストレスに応答する様子を観察する
次にチームは、転写(DNAからRNAへの複製)が阻害されたときにこの核マップがどのように変化するかを検討しました。RNAポリメラーゼをDNA上で停止させる薬剤アクチノマイシンDで細胞を処理すると、核内の空間関係は劇的に再構築されました。通常は不規則な輪郭を持ち、活性クロマチンの間に位置する核スピークルはより丸くなり、転写サイトや活性ヒストンマークとの密接な接触は大部分が消失しました。一方で抑制的なクロマチンマークは核ラミナとの結びつきが強まり、より凝縮して沈黙したゲノムの状態と一致しました。複数の統計解析層を組み合わせることで、著者らは異なる核成分間の全体的な傾向と局所的な濃縮や排除のポケットを区別することができました。
生物学にとっての意義
本質的に、この研究はDNA-PAINTをより高速で多用途な細胞内部地図作成ツールへと変えます。速度最適化された配列のライブラリが拡充されたことで、科学者は実用的な時間スケールで同一細胞内の多くの核ランドマークをナノメートル分解能で追跡できるようになりました。著者らはこの手法が転写の停止時にクロマチンが核スピークルから離れ、周辺に集約される様子を捉えるのに十分感度があることを示しています。より多くのタンパク質や修飾に手法が拡張されれば、健康や疾患における核組織の詳細な「アトラス」を提供し、遺伝子調節が三次元的にどのように配線されているかを明らかにすることが期待されます。
引用: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
キーワード: 超解像イメージング, DNA-PAINT, クロマチン構造, 核スピークル, 転写阻害