Clear Sky Science · sv
Högupplöst multiplexerad DNA-PAINT-avbildning av nukleär organisation med ett utökat sekvensrepertoar
Att se cellkärnan i ny detalj
Inuti varje cell är genomet vikt och ordnat på ett invecklat sätt som hjälper till att styra vilka gener som är aktiva eller inaktiva. Fram tills nyligen var mycket av denna inre arkitektur för liten och tät för att kunna ses tydligt. Denna artikel beskriver en snabbare och kraftfullare avbildningsmetod som gör det möjligt för forskare att kartlägga många olika nukleära komponenter samtidigt med närmast molekylär precision, och avslöjar hur genomet och dess omgivande strukturer omorganiseras när genaktiviteten stängs av.
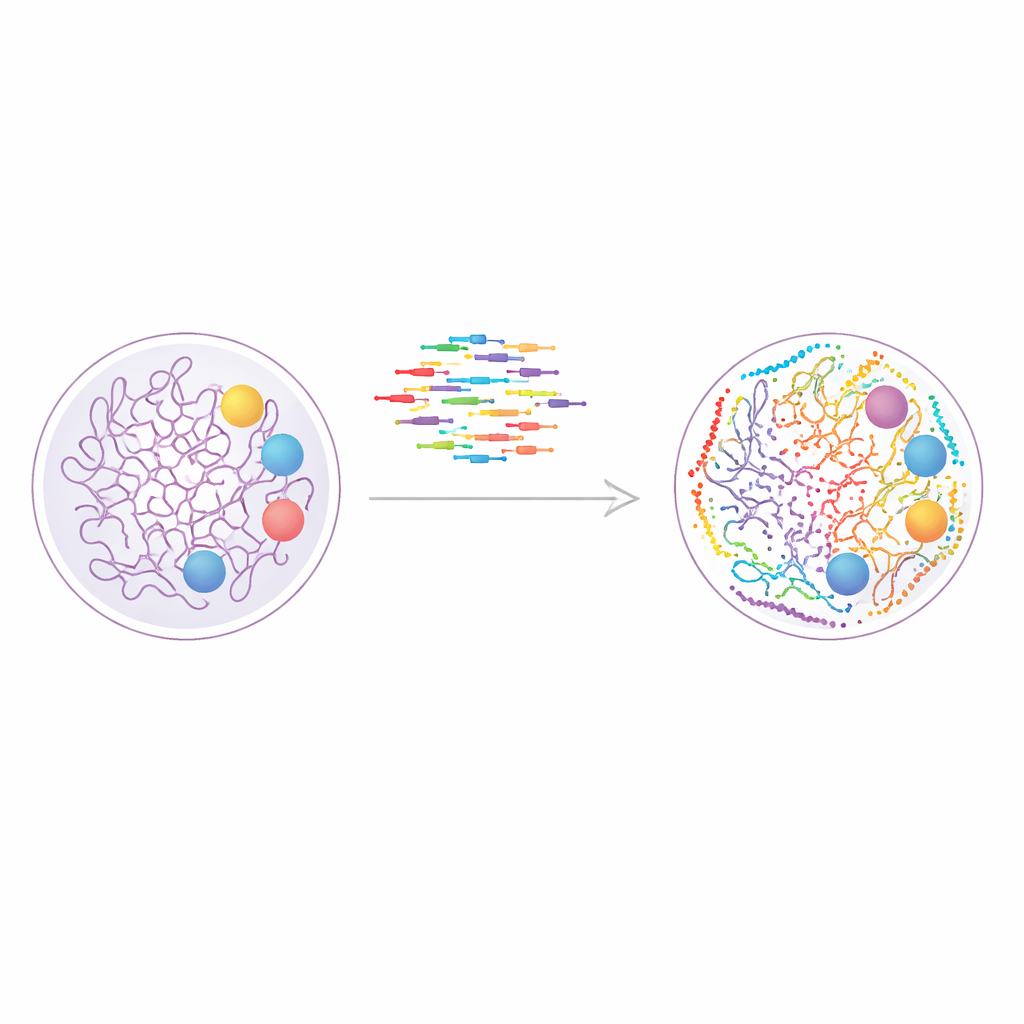
Ett nytt sätt att måla genomet
Studien bygger på en teknik kallad DNA-PAINT, som använder korta fluorescerande DNA-strängar som upprepade gånger binder och släpper från matchande DNA-taggar på cellulära strukturer. Varje bindningstillfälle ger upphov till ett litet ljusblixt, och många sådana händelser kan kombineras för att återskapa en skarp bild långt bortom vanliga mikroskopers gränser. DNA-PAINT är naturligt väl lämpat för att undersöka många mål i samma cell, eftersom varje protein eller kromatinmärke kan märkas med en distinkt DNA-sekvens. Problemet har varit hastigheten: traditionella sekvensdesigner binder för långsamt, vilket gör varje avbildningsrunda till ett timmar-långt experiment.
Att utöka färgpaletten
För att tackla den här flaskhalsen designade författarna systematiskt ett bredare set av "hastighetsoptimerade" DNA-sekvenser som binder oftare samtidigt som de förblir specifika. De byggde skräddarsydda DNA-nanostrukturer, kända som DNA-origami, för att testa hur väl varje imager-sträng kände igen sin matchande dockningssträng och hur ofta den blinkade. Genom att montera origami-plattor som bar dockningsställen arrangerade i ett precist 4×3-rutnät endast 20 nanometer från varandra, kunde de mäta både upplösning och oönskad korsprat. Detta arbete resulterade i tolv snabba sekvenser totalt, varav tio kunde användas tillsammans utan att störa varandra, vilket möjliggör direkt avbildning av upp till tio mål i ett experiment.
Skarpare bilder på kortare tid
Inte alla snabba sekvenser uppträdde likadant. En del gav längre bestående bindningstillfällen, vilket visade sig vara särskilt användbart. När teamet jämförde en kortbindande och en långbindande sekvens på samma origami-rutnät gav den långbindande proben skarpare separation mellan intilliggande platser och gjorde det även vid lägre lasereffekt. Längre händelser gjorde att kameran kunde samla fler fotoner från varje bindning, vilket förbättrade lokalisationsprecisionen till bara några nanometer. Dessa prober provtog också målplatserna mer effektivt och nådde pålitlig täckning på färre bildrutor. I praktiken betyder detta att forskare kan förvärva högkvalitativa superupplösta bilder på minuter istället för timmar, med mindre risk för provskada.
Kartlägga det nukleära landskapet
Beväpnade med sitt utökade sekvensset gick forskarna från artificiella DNA-strukturer till levande cellbiologi. De använde DNA-PAINT för att avbilda nio olika nukleära drag i humana celler, inklusive aktiva och pausade former av RNA-polymeras II, flera kemiska märken på histonproteiner som markerar aktivt eller tyst kromatin, den nukleära lamina vid periferin och nukleära speckles — droppliknande nav rika på splitsningsfaktorer. Genom att koppla konventionella antikroppar till DNA-dockningssträngar och avbilda målen i nio sekventiella rundor byggde de upp en superupplöst, multiplexerad karta av kärnan, där varje prick motsvarar ett molekylärt grannskap bara några nanometer stort.
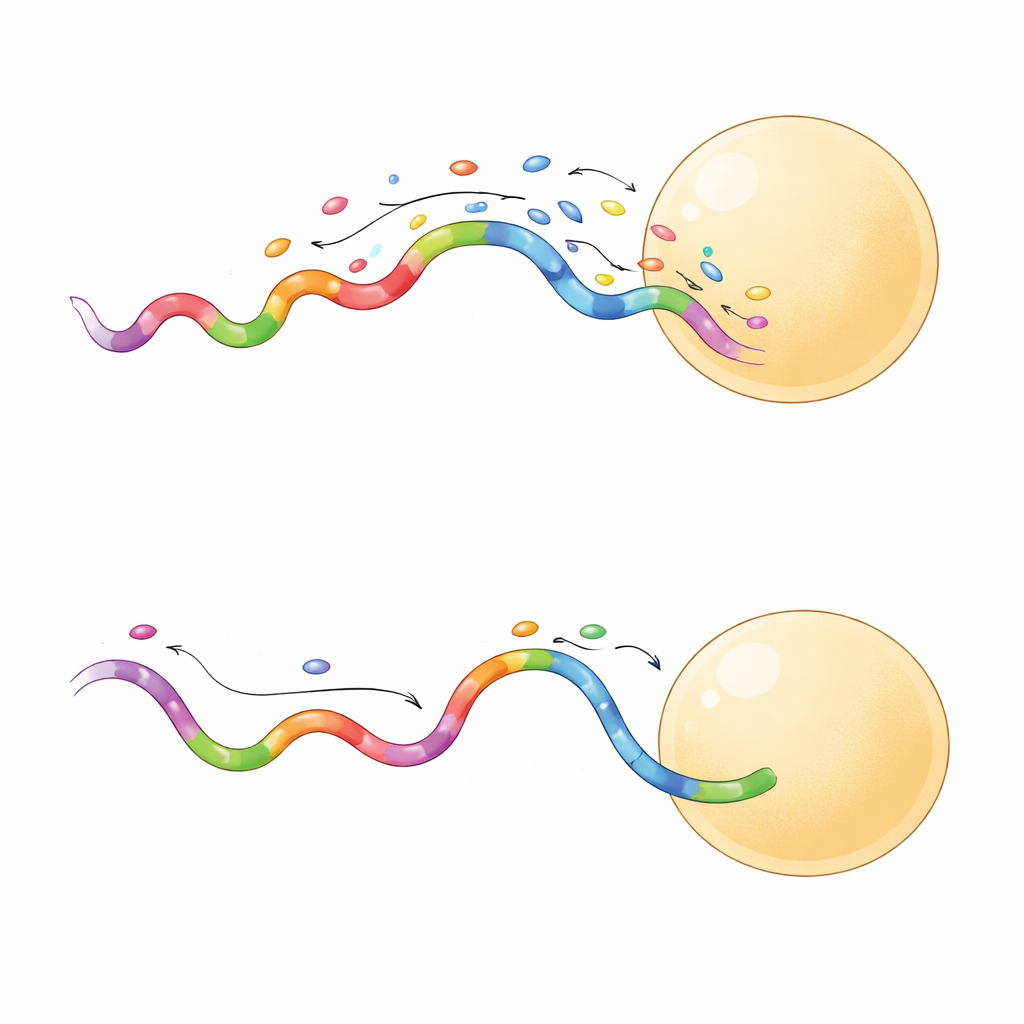
Se hur kromatin svarar på stress
Teamet frågade sedan hur denna nukleära karta förändras när transkriptionen — kopieringen av DNA till RNA — blockeras. Behandling av celler med läkemedlet actinomycin D, som stannar upp RNA-polymeraser på DNA, omformade dramatiskt de rumsliga relationerna i kärnan. Nukleära speckles, som normalt har oregelbundna konturer och ligger i aktivt kromatin, blev mer rundade och deras täta kontakter med transkriptionsplatser och aktiva histonmärken försvann till stor del. Samtidigt visade repressiva kromatinmärken stärkt association med den nukleära laminan, i linje med ett mer kompakt, tystat genom. Genom att kombinera flera lager av statistisk analys kunde författarna skilja globala trender från lokala fickor av berikning eller uteslutning mellan olika nukleära komponenter.
Varför detta är viktigt för biologin
I korthet förvandlar detta arbete DNA-PAINT till ett snabbare, mer mångsidigt verktyg för att kartlägga cellens inre geografi. Med ett större bibliotek av hastighetsoptimerade DNA-sekvenser kan forskare nu spåra många nukleära landmärken i samma cell på nanometernivå och inom praktiska tidsramar. Författarna visar att detta tillvägagångssätt är tillräckligt känsligt för att fånga hur kromatin lossnar från nukleära speckles och konsolideras vid periferin när transkriptionen stoppas. När metoden utökas till fler proteiner och modifieringar lovar den detaljerade "atlaser" över nukleär organisation vid hälsa och sjukdom, vilket hjälper till att avslöja hur genreglering är kopplad i tre dimensioner.
Citering: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Nyckelord: superupplösningsavbildning, DNA-PAINT, kromatinorganisation, nukleära speckles, transkriptionshämning