Clear Sky Science · it
Immagini DNA-PAINT multiplex ad alta velocità dell’organizzazione nucleare usando un repertorio di sequenze ampliato
Vedere il nucleo cellulare con nuovo dettaglio
All’interno di ciascuna delle nostre cellule, il genoma è ripiegato e disposto in modo complesso che contribuisce a controllare quali geni vengono attivati o disattivati. Fino a poco tempo fa gran parte di questa architettura interna era troppo piccola e affollata per essere vista chiaramente. Questo articolo descrive un metodo di imaging più veloce e potente che permette ai ricercatori di mappare contemporaneamente molti componenti nucleari con precisione quasi molecolare, rivelando come il genoma e le strutture circostanti si riorganizzino quando l’attività genica viene arrestata.
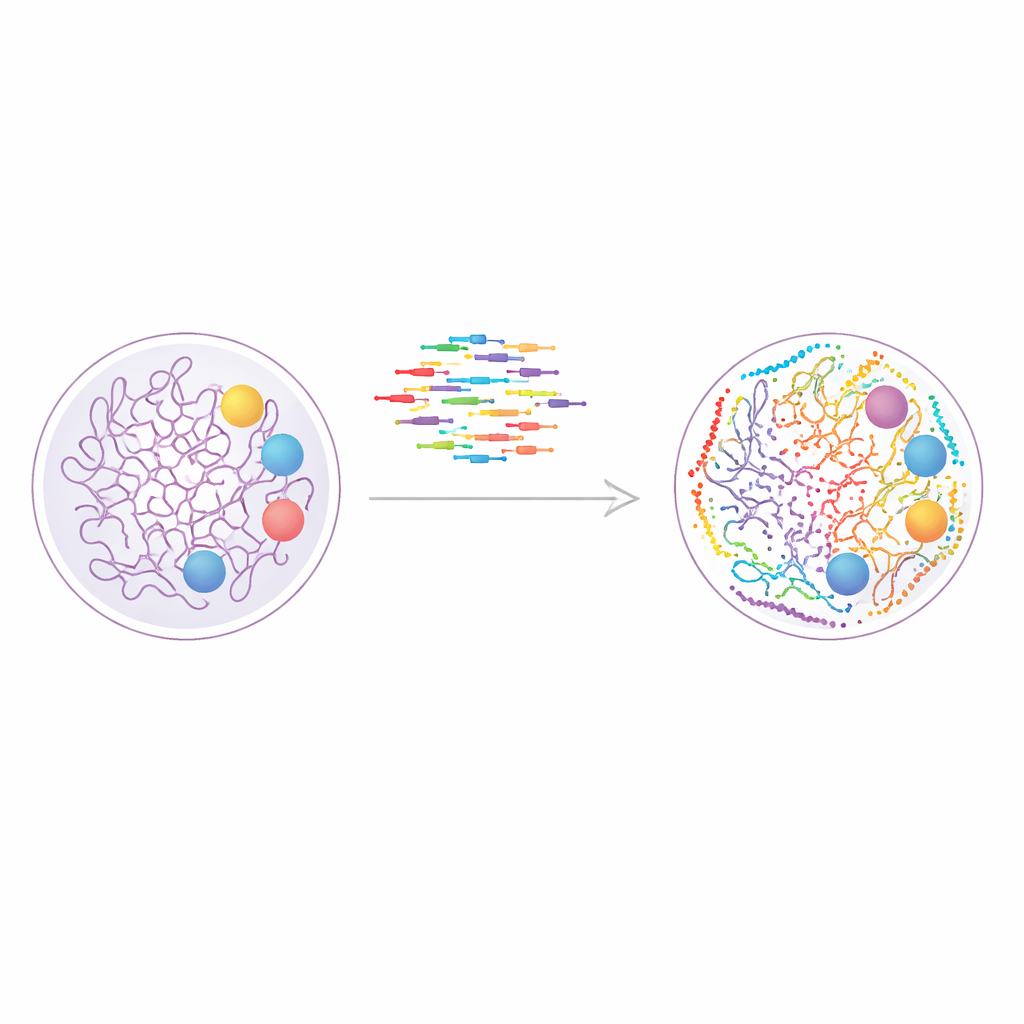
Un nuovo modo di ‘pitturare’ il genoma
Lo studio si basa su una tecnica chiamata DNA-PAINT, che utilizza brevi filamenti di DNA fluorescenti che si legano e si staccano ripetutamente da etichette di DNA corrispondenti sulle strutture cellulari. Ogni evento di legame produce un piccolo lampo di luce e molti di questi eventi possono essere combinati per ricostruire un’immagine nitida ben oltre i limiti dei microscopi convenzionali. DNA-PAINT si presta naturalmente all’osservazione di molti bersagli nella stessa cellula, perché ogni proteina o segno sulla cromatina può essere marcato con una sequenza di DNA distinta. Il problema è stata la velocità: i progetti di sequenza tradizionali si legano troppo lentamente, trasformando ogni ciclo di imaging in un esperimento di ore.
Espandere la tavolozza dei colori
Per affrontare questo collo di bottiglia, gli autori hanno progettato in modo sistematico un insieme più ampio di sequenze “ottimizzate per la velocità” che si legano più frequentemente mantenendo comunque specificità. Hanno costruito nanostrutture di DNA progettate, note come DNA origami, per testare quanto bene ogni filamento imager riconoscesse il corrispondente sito di ancoraggio e quanto spesso si illuminasse. Assemblando piastrelle di origami che portavano siti di docking disposti in una precisa griglia 4 per 3 distanti solo 20 nanometri, hanno potuto misurare sia la risoluzione sia il cross-talk indesiderato. Questo lavoro ha prodotto in totale dodici sequenze veloci, di cui dieci potevano essere usate insieme senza interferire, consentendo l’imaging diretto fino a dieci bersagli in un unico esperimento.
Immagini più nitide in meno tempo
Non tutte le sequenze veloci si comportavano allo stesso modo. Un sottoinsieme produceva eventi di legame più duraturi, che si sono rivelati particolarmente utili. Quando il gruppo ha confrontato una sequenza a legame breve e una a legame lungo sulla stessa griglia di origami, la sonda a legame lungo ha fornito una separazione più netta tra siti vicini e lo ha fatto anche a potenze laser inferiori. Eventi più lunghi hanno permesso alla camera di raccogliere più fotoni da ogni legame, migliorando la precisione di localizzazione a poche nanometers. Queste sonde hanno anche campionato i siti bersaglio in modo più efficiente, raggiungendo una copertura affidabile in meno frame. In pratica, questo significa che i ricercatori possono acquisire immagini super-risolte di alta qualità in minuti anziché ore, con un rischio minore di danneggiare il campione.
Mappare il paesaggio nucleare
Armati del loro set di sequenze ampliato, i ricercatori sono passati dalle strutture di DNA artificiali alla biologia cellulare reale. Hanno usato DNA-PAINT per immagini nove diverse caratteristiche nucleari in cellule umane, incluse le forme attive e pause della RNA polimerasi II, vari marchi chimici sulle proteine istoniche che segnalano cromatina attiva o silente, la lamina nucleare al perimetro e gli speckles nucleari—hub simili a goccioline ricchi di fattori di splicing. Collegando anticorpi convenzionali a filamenti di docking in DNA e imagedo i bersagli in nove cicli sequenziali, hanno assemblato una mappa multiplex e super-risolta del nucleo, dove ogni punto corrisponde a un quartiere molecolare largo solo pochi nanometri.
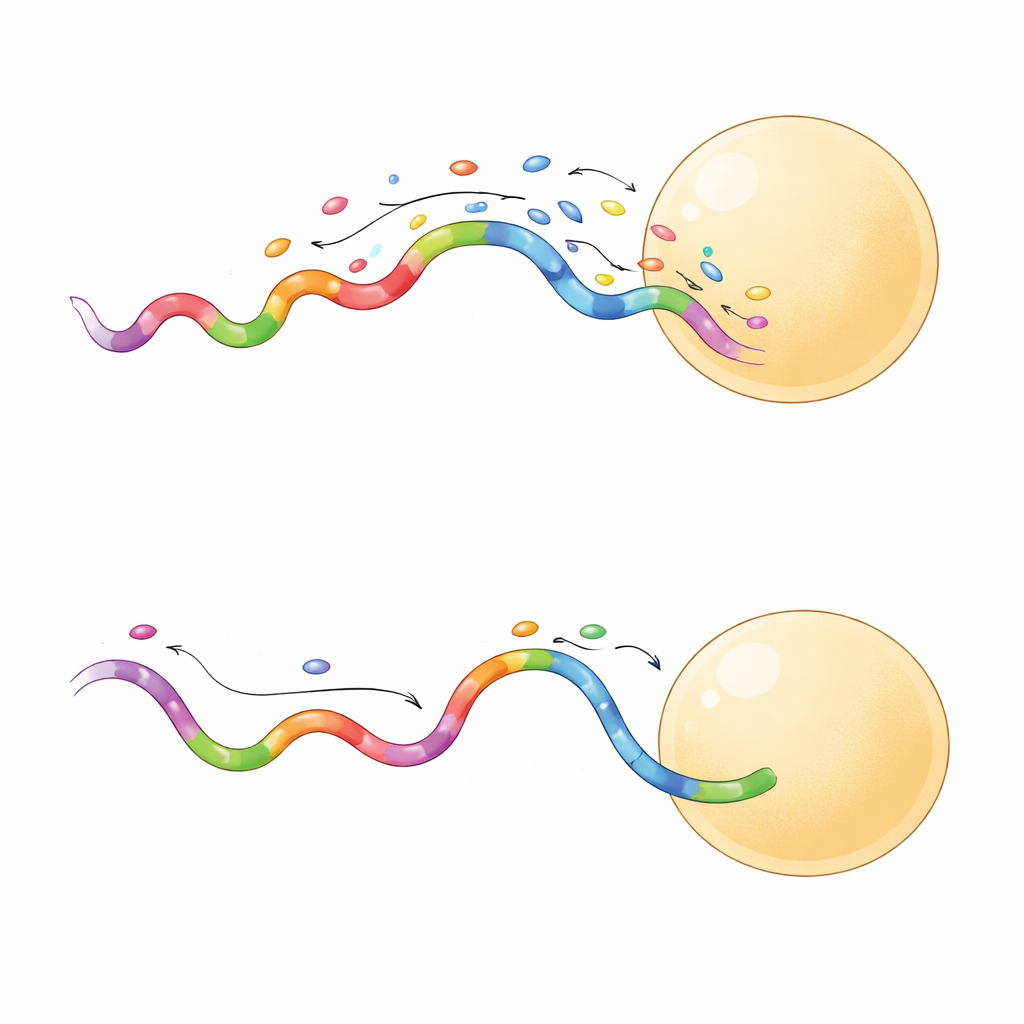
Osservare la risposta della cromatina allo stress
Il team ha poi chiesto come questa mappa nucleare cambi quando la trascrizione—la copia del DNA in RNA—viene bloccata. Il trattamento delle cellule con il farmaco actinomicina D, che arresta le RNA polimerasi sul DNA, ha rimodellato sensibilmente le relazioni spaziali all’interno del nucleo. Gli speckles nucleari, che normalmente hanno contorni irregolari e stazionano in mezzo a cromatina attiva, sono diventati più arrotondati e i loro contatti ravvicinati con i siti di trascrizione e i marchi istonici attivi sono in gran parte scomparsi. Contemporaneamente, i marchi di cromatina repressiva hanno mostrato un’associazione rafforzata con la lamina nucleare, coerente con un genoma più compatto e silenziato. Combinando diversi livelli di analisi statistica, gli autori sono riusciti a distinguere tendenze globali da nicchie locali di arricchimento o esclusione tra i diversi componenti nucleari.
Perché questo è importante per la biologia
In sostanza, questo lavoro trasforma il DNA-PAINT in uno strumento più veloce e più versatile per mappare la geografia interna della cellula. Con una libreria più ampia di sequenze di DNA ottimizzate per la velocità, gli scienziati possono ora seguire molti punti di riferimento nucleari nella stessa cellula con risoluzione nanometrica e in tempi pratici. Gli autori mostrano che questo approccio è sufficientemente sensibile per catturare come la cromatina si stacca dagli speckles nucleari e si consolida al perimetro quando la trascrizione è sospesa. Man mano che il metodo viene esteso a più proteine e modificazioni, promette “atlanti” dettagliati dell’organizzazione nucleare in salute e malattia, aiutando a rivelare come la regolazione genica è cablata nello spazio tridimensionale.
Citazione: Banerjee, A., Anand, M., Srivastava, M. et al. High-speed multiplexed DNA-PAINT imaging of nuclear organization using an expanded sequence repertoire. Nat Commun 17, 3655 (2026). https://doi.org/10.1038/s41467-026-72206-0
Parole chiave: imaging a super-risoluzione, DNA-PAINT, organizzazione della cromatina, speckles nucleari, inibizione della trascrizione