Clear Sky Science · zh
细胞丧失扰乱机械稳态,驱动体外视网膜色素上皮呈现衰老样表型
为什么老化的眼细胞难以维持清晰视力
随着年龄增长,许多人出现中心视力问题,常与位于眼后部的一层薄细胞——视网膜色素上皮(RPE)受损有关。这些细胞每天默默支持上方的感光视杆/视锥细胞,但单纯细胞丢失如何改变其物理状态并削弱其功能一直难以明确。该研究在实验室中重建了类似老化的情景,显示即使是适度数量的RPE细胞消失,也能在机械上“重接线”剩余组织,使其变得更硬、更不柔韧,并降低清理视觉垃圾的核心功能。
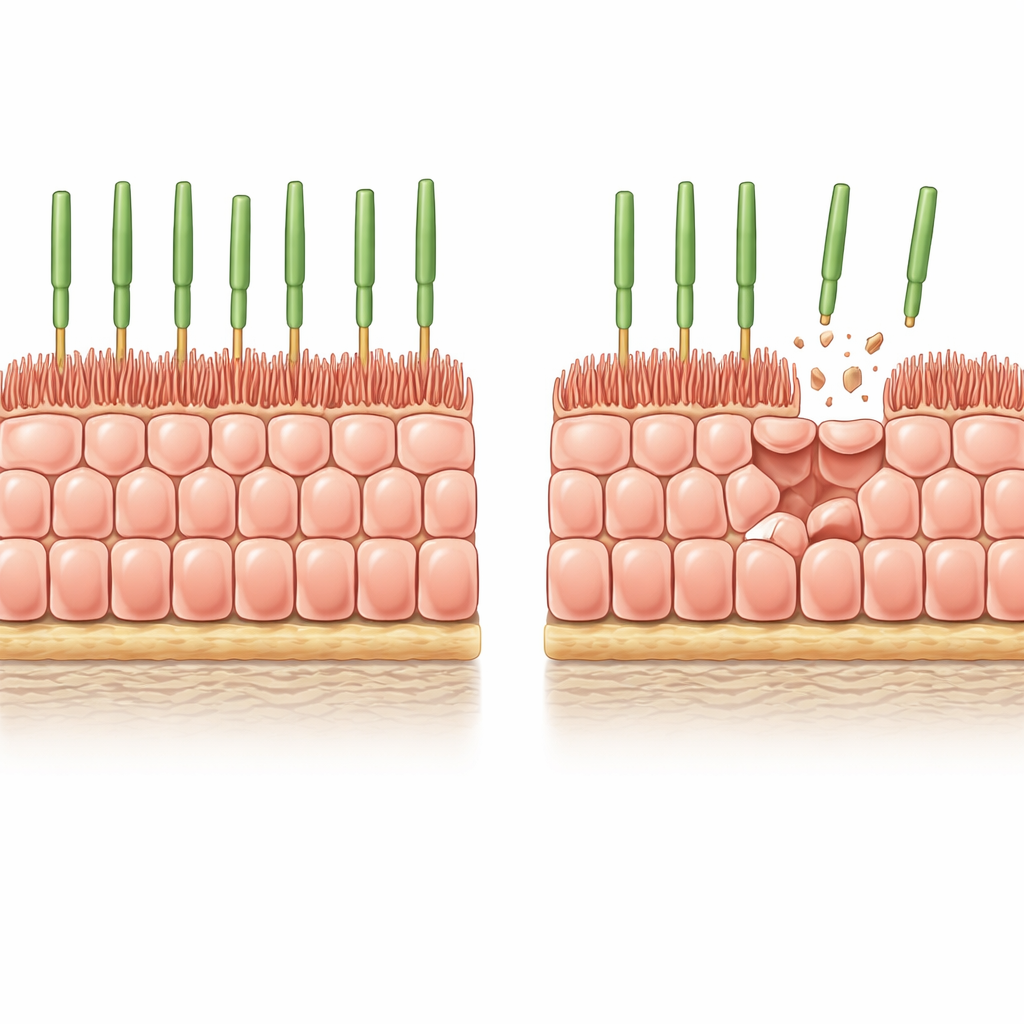
对老化眼组织的细致实验室模型
研究者从人类干细胞来源的RPE开始,在一种软且具有生物学相似性的凝胶上培养成均匀、紧密堆积的细胞片。在这些条件下,细胞停止分裂,呈现健康RPE中常见的蜂窝状排列,并在顶面发育出与感光细胞相互作用的指状微绒毛。为模拟老化眼中渐进性的细胞丢失,团队在细胞中引入了一个可控的“自杀”开关并触发了广泛但部分的细胞死亡。几天内约有8%的细胞消失,幸存细胞不得不在没有新细胞分裂帮助的情况下拉伸以覆盖空隙。
细胞层在丧失后如何重塑
在诱导性变薄之后,剩余的RPE细胞变得更宽但明显更短,保持体积同时横向扩展以封闭组织空隙。它们的顶端微绒毛缩小且更杂乱,一些细胞出现横跨细胞的粗大肌动蛋白应力纤维——这些特征也见于老化的人类RPE。测量证实,诸如ezrin及其活性磷酸化形式等与微绒毛相关的关键蛋白减少。换言之,仅仅邻居细胞的丧失就足以将结构上年轻的细胞推动到与眼内老化RPE高度相似的构架状态。
刚性与清理能力的权衡
组织结构不仅关乎外观,还决定功能。RPE细胞每天必须摄取并消化大量来自感光细胞外段的碎片。研究团队用荧光标记的猪视网膜碎片来测量这种清理活性。密度降低的RPE片总体吞入的碎片更少,但吞入的碎片往往更大。高分辨成像显示了原因:在健康细胞片中,顶面会向上拱起,形成围绕每个碎片的明显杯状结构,由动态的肌动蛋白和肌球蛋白重排支撑。在密度降低的细胞片中,表面看起来更平滑、较难变形,清晰的杯状结构减少,且出现大量富含肌动蛋白的大突起,这些突起似乎并不利于吞噬颗粒。
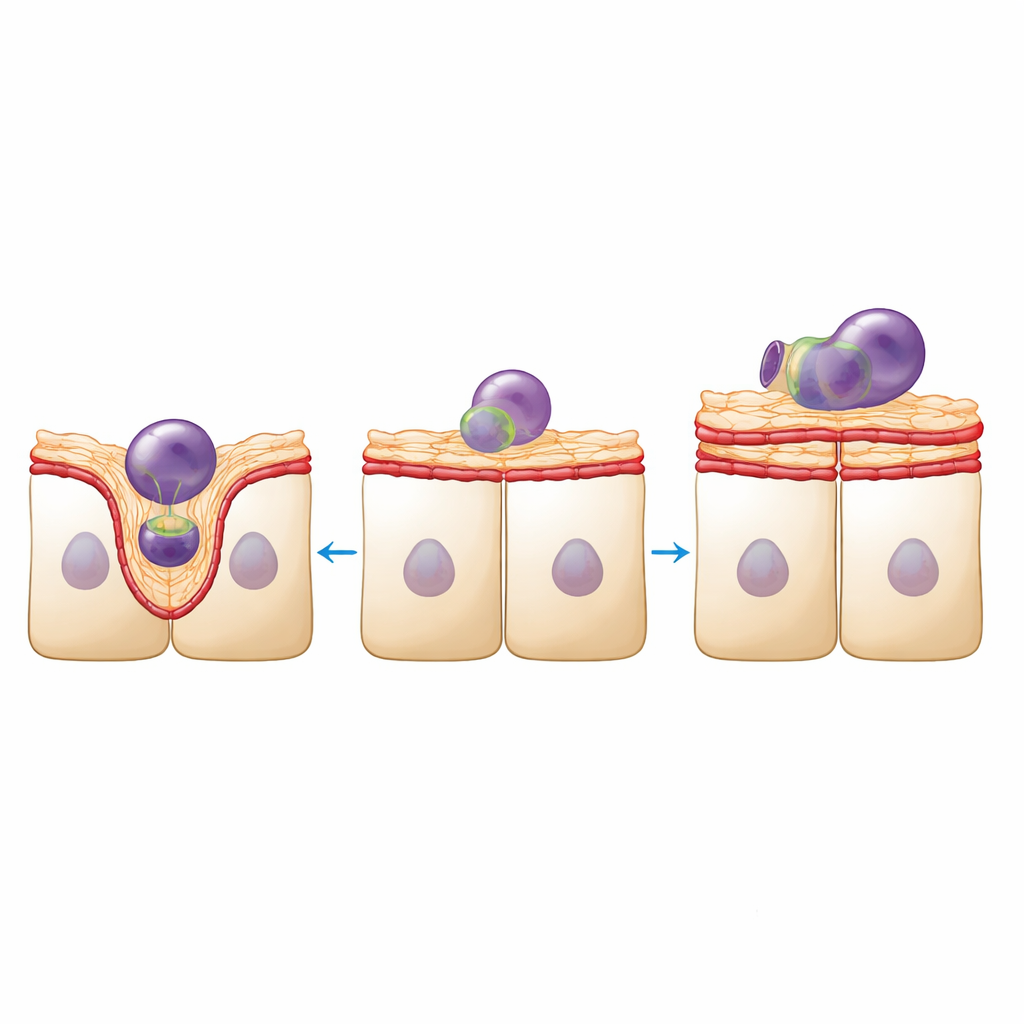
机械稳态转向僵硬
为将这些可视变化与力学联系起来,作者在两个尺度上探测了组织的物理特性。纳米压痕法——用微小球形探针压入顶面——显示密度降低的RPE作为多细胞片整体变得大约三分之一更硬且更有弹性。与此同时,收缩力和连接强度的分子标志物——磷酸化肌球蛋白轻链和粘附蛋白vinculin——在细胞间边界附近富集。然而,布里尔森显微镜(Brillouin microscopy),一种基于光学感知细胞内部局部刚度和含水量的方法,显示顶层皮质在某些方面实际上变得机械上更为不同并且更柔软。综合来看,这些发现表明单层通过加强侧向连接来保持片层完整,而顶端表面则丧失了通常允许其弯曲并围绕颗粒形成杯状结构的精细微观结构。
肌动蛋白调控子在强度与柔性之间掌舵
基因表达分析指出,密度降低的RPE中肌动蛋白系统发生了广泛的重编程。促进分支状肌动蛋白网络和交联的蛋白上调,而多种formin类蛋白(有利于形成长直的肌动蛋白丝)和ezrin下调。随后团队用药理手段调节这些系统。在正常RPE中抑制formin使细胞片变硬并使被吞噬的碎片变大,部分模拟了老化样状态。在密度降低的RPE中,阻断Arp2/3复合体(一种关键的分支肌动蛋白成核子)增加了内吞碎片的数量并恢复了更明显的顶面拱起。这些干预表明,调节肌动蛋白成核可以在更刚性、保护性的构型与更易变形、利于吞噬的构型之间来回切换组织状态。
这对老化眼睛意味着什么
总体来看,该工作表明适度的细胞丧失本身就能将RPE组织推入新的机械平衡:单层作为整体被更强地缝合并变得更僵硬,但其顶端表面失去有效吞噬感光碎片所需的可塑性。实际上,细胞优先选择维持组织完整性而非执行其专门的清理职责。这种由肌动蛋白细胞骨架和连接张力变化驱动的结构性权衡,而非传统的生化老化损伤,或许能解释为什么老化的RPE常常看起来完好却功能衰退。理解并可能调控稳固性与柔韧性之间的这种平衡,或可为在年龄相关性黄斑变性等疾病中保护视力开辟新路径。
引用: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
关键词: 视网膜色素上皮, 细胞力学, 年龄相关性黄斑变性, 肌动蛋白细胞骨架, 吞噬作用