Clear Sky Science · it
La perdita cellulare altera l’omeostasi meccanica e induce in vitro un fenotipo dell’epitelio pigmentato retinico simile all’invecchiamento
Perché le cellule oculari invecchiate fanno più fatica a mantenere una visione nitida
Con l’avanzare dell’età molte persone sviluppano problemi alla vista centrale, spesso collegati a danni in un sottile strato di cellule sul retro dell’occhio chiamato epitelio pigmentato retinico (RPE). Queste cellule lavorano quotidianamente per sostenere i fotorecettori sovrastanti, ma è stato difficile chiarire come la semplice perdita cellulare legata all’età modifichi il loro stato fisico e comprometta le loro funzioni. Questo studio ricrea in laboratorio uno scenario simile all’invecchiamento e mostra che la perdita anche di un numero modesto di cellule RPE può “ricablarne” meccanicamente il tessuto rimanente, rendendolo più rigido, meno flessibile e meno efficiente nel loro compito principale di rimuovere i detriti visivi.
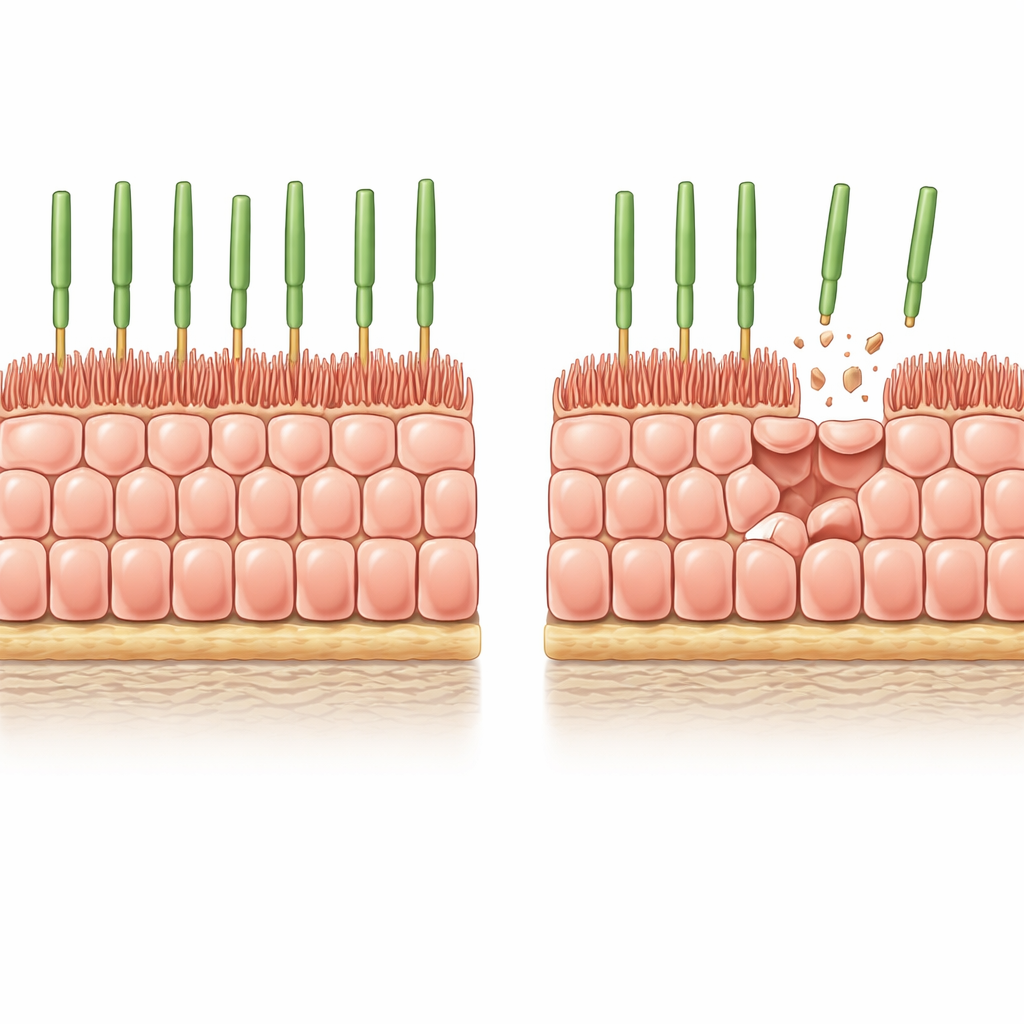
Un modello sperimentale accurato del tessuto oculare invecchiato
I ricercatori hanno iniziato con RPE derivate da cellule staminali umane coltivate come un foglio uniforme e densamente impaccato su un gel morbido, biologicamente realistico. In queste condizioni le cellule smettono di dividersi, assumono il classico schema a nido d’ape visto nell’RPE sano e sviluppano microvilli rigidi sulla superficie apicale che interagiscono con i fotorecettori. Per imitare la perdita graduale di cellule che avviene con l’età, il gruppo ha introdotto nelle cellule un interruttore “suicida” controllabile e ha poi indotto una morte cellulare diffusa ma parziale. Nel giro di pochi giorni circa l’8% delle cellule è scomparso e le sopravvissute hanno dovuto allungarsi per coprire i vuoti senza il contributo di nuova proliferazione.
Come il foglio cellulare si rimodella dopo la perdita
Dopo questo assottigliamento indotto, le cellule RPE rimaste si sono allargate ma sono divenute visibilmente più basse, preservando il loro volume mentre si spandevano lateralmente per sigillare il tessuto. I loro microvilli apicali si sono ridotti e disorganizzati, e alcune cellule hanno formato spessi stress fiber di actina che li attraversavano—caratteristiche osservate anche nell’RPE umana invecchiata. Le misurazioni hanno confermato la riduzione di proteine associate ai microvilli chiave, come l’ezrina e la sua forma fosforilata attiva. In altre parole, la semplice perdita dei vicini è stata sufficiente a spingere cellule strutturalmente giovani verso un’architettura molto simile a quella dell’RPE anziano nell’occhio.
Quando la rigidità compromette la capacità di pulizia
La struttura del tessuto non riguarda solo l’aspetto; è alla base della funzione. Le cellule RPE devono ingerire e digerire quotidianamente innumerevoli frammenti degli strati esterni dei fotorecettori. Utilizzando frammenti fluorescenti derivati da retine di maiale, il team ha misurato questa attività di pulizia. I fogli di RPE a densità ridotta internalizzavano meno frammenti complessivamente, sebbene quelli che venivano inglobati tendessero a essere più grandi. L’imaging ad alta risoluzione ha spiegato il motivo: nei fogli sani la superficie apicale si gonfiava verso l’alto formando coppe ben definite intorno a ogni frammento, sostenute da dinamici rimaneggiamenti di actina e miosina. Nei fogli a densità ridotta la superficie appariva più liscia e meno deformabile, con meno forme a coppa evidenti e la presenza di grandi protrusioni ricche di actina che non sembravano agevolare l’inglobamento delle particelle.
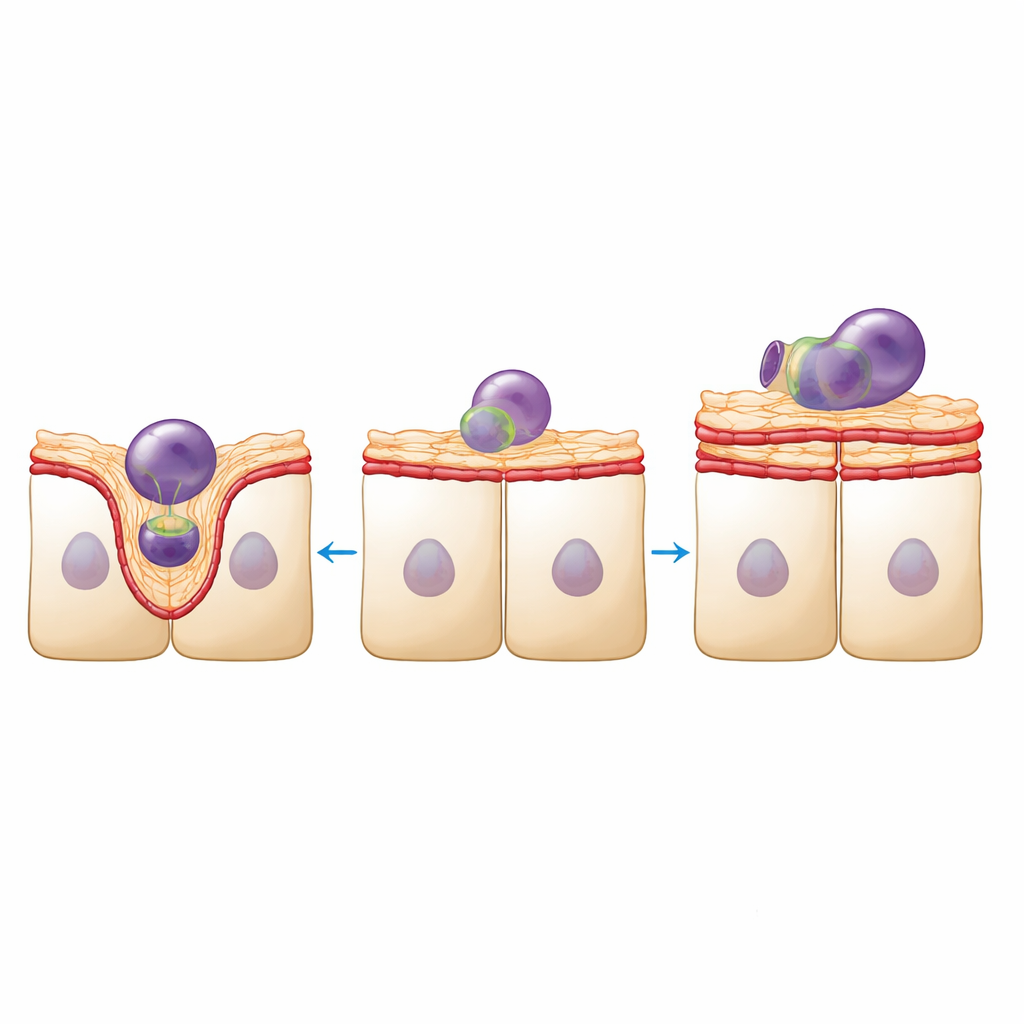
L’omeostasi meccanica si sposta verso la rigidità
Per collegare questi cambiamenti visivi alla meccanica, gli autori hanno sondato le proprietà fisiche del tessuto su due scale. La nanoindentazione, che preme una piccola punta sferica sulla superficie apicale, ha rivelato che l’RPE a densità ridotta è diventata grosso modo un terzo più rigida e più elastica come foglio multicellulare. Allo stesso tempo, marker molecolari della contrattilità e della forza delle giunzioni—la catena leggera della miosina fosforilata e la proteina di adesione vinculina—erano arricchiti lungo i bordi cellula‑cellula. Tuttavia, la microscopia di Brillouin, un metodo ottico che rileva la rigidità locale e il contenuto d’acqua all’interno delle cellule, ha mostrato che la corteccia apicale stessa era meccanicamente distinta e, sotto certi aspetti, più morbida. Nel complesso, questi risultati suggeriscono che il monostrato rinforza le connessioni laterali per mantenere l’integrità del foglio mentre la superficie apicale perde la microstruttura finemente regolata che le consente normalmente di piegarsi e formare coppe intorno alle particelle.
I regolatori dell’actina governano l’equilibrio tra resistenza e flessibilità
L’analisi dell’espressione genica ha indicato un ampio riassetto della macchina dell’actina nell’RPE a densità ridotta. Proteine che favoriscono reti di actina ramificata e il crosslinking risultavano sovra‑regolate, mentre diversi formini, che privilegiano filamenti lunghi e lineari, ed ezrina erano sotto‑regolati. Il gruppo ha quindi modulato farmacologicamente questi sistemi. Inibire i formin in RPE normali ha irrigidito il foglio e aumentato le dimensioni dei frammenti inglobati, riproducendo parzialmente lo stato simile all’invecchiamento. Nell’RPE a densità ridotta, bloccare il complesso Arp2/3, un nucleatore chiave di actina ramificata, ha aumentato il numero di frammenti internalizzati e ha ripristinato un più marcato rigonfiamento della superficie apicale. Queste interventi dimostrano che modulare la nucleazione dell’actina può spostare il tessuto tra una configurazione più rigida e protettiva e una più deformabile e favorevole alla fagocitosi.
Cosa significa per gli occhi che invecchiano
Nel complesso, il lavoro dimostra che una perdita cellulare modesta da sola può spingere il tessuto RPE verso un nuovo equilibrio meccanico: il foglio diventa più strettamente cucito e più rigido nel suo insieme, ma la sua superficie apicale perde la plasticità necessaria per inglobare efficacemente i detriti dei fotorecettori. Di fatto, le cellule danno priorità al mantenimento della coesione tissutale rispetto al loro compito specializzato di pulizia. Questo compromesso strutturale, guidato da cambiamenti nel citoscheletro di actina e nella tensione giunzionale piuttosto che da danni biochimici classici legati all’invecchiamento, può aiutare a spiegare perché l’RPE invecchiato appare spesso intatto ma funziona male. Comprendere e eventualmente modulare questo equilibrio tra stabilità e flessibilità potrebbe aprire nuove strade per preservare la visione in patologie come la degenerazione maculare legata all’età.
Citazione: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Parole chiave: epitelio pigmentato retinico, meccanica cellulare, degenerazione maculare legata all’età, citoplasma di actina, fagocitosi