Clear Sky Science · nl
Celverlies verstoort mechanische homeostase en veroorzaakt een verouderingsachtig fenotype van het retinale pigmentepitheel in vitro
Waarom verouderende oculaircellen moeite hebben om het gezichtsvermogen helder te houden
Met het ouder worden krijgen veel mensen problemen met het centraal zien, vaak gerelateerd aan schade in een dunne cellaag achter in het oog, het retinaal pigmentepitheel (RPE). Deze cellen werken elke dag onopvallend om de lichtgevoelige fotoreceptoren boven hen te ondersteunen, maar het is moeilijk vast te stellen hoe eenvoudig celverlies met de leeftijd hun fysieke toestand verandert en hun functie ondermijnt. Deze studie reconstrueert een verouderingsachtig scenario in het laboratorium en toont aan dat het verlies van zelfs een bescheiden aantal RPE‑cellen het resterende weefsel mechanisch kan "herbekabelen" op manieren die het stugger, minder flexibel en slechter maken in hun kernfunctie: het opruimen van visueel afval.
Een nauwkeurig laboratoriummodel van verouderend oculair weefsel
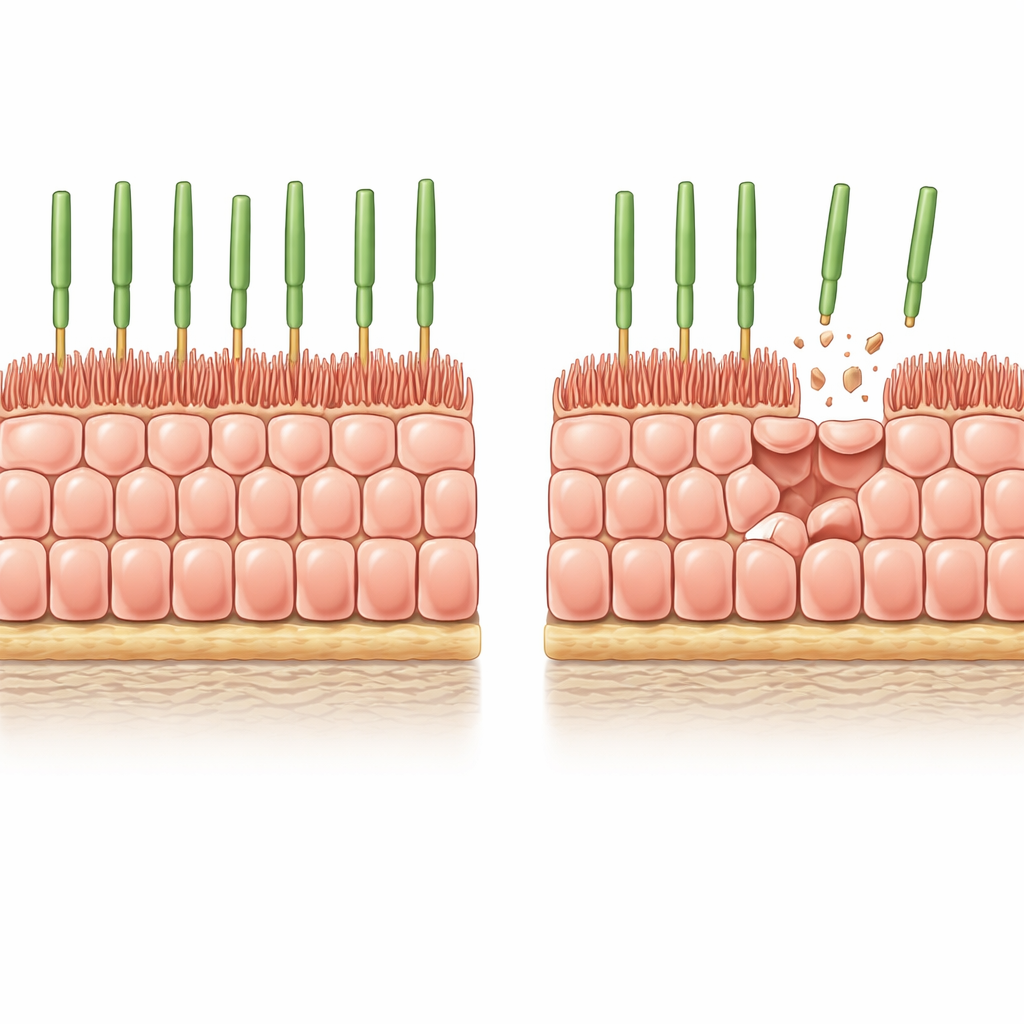
De onderzoekers begonnen met RPE afgeleid van menselijke stamcellen, gekweekt als een uniforme, dicht opeengepakte laag op een zacht, biologisch realistisch gel. Onder deze omstandigheden stoppen de cellen met delen, nemen ze het kenmerkende honingraatpatroon aan dat bij gezond RPE wordt gezien, en ontwikkelen ze vingervormige microvilli op hun bovenste oppervlak die met fotoreceptoren interageren. Om het geleidelijke celverlies na te bootsen dat optreedt in het verouderende oog, introduceerde het team een controleerbare "zelfmoord"‑schakelaar in de cellen en activeerde vervolgens wijdverspreide maar gedeeltelijke celdood. Over enkele dagen verdwenen ongeveer 8% van de cellen, en de overlevenden moesten zich uitstrekken om de gaps te bedekken zonder hulp van nieuwe celdeling.
Hoe de cellaag zich hervormt na verlies
Na deze geïnduceerde verdunning werden de resterende RPE‑cellen breder maar merkbaar korter, waarbij ze hun volume behielden terwijl ze zijwaarts uitspreidden om het weefsel te sluiten. Hun apicale microvilli krimpten en raakten meer gedesorganiseerd, en sommige cellen ontwikkelden dikke actine‑stressvezels die recht over hen liepen — kenmerken die ook worden gezien in oud menselijk RPE. Metingen bevestigden dat sleutelproteïnen geassocieerd met microvilli, zoals ezrin en de actieve gefosforyleerde vorm ervan, afnamen. Met andere woorden, simpel verlies van buren was voldoende om structureel jonge cellen te duwen naar een architectuur die sterk lijkt op die van oud RPE in het oog.
Wanneer stijfheid ten koste gaat van opruimvermogen
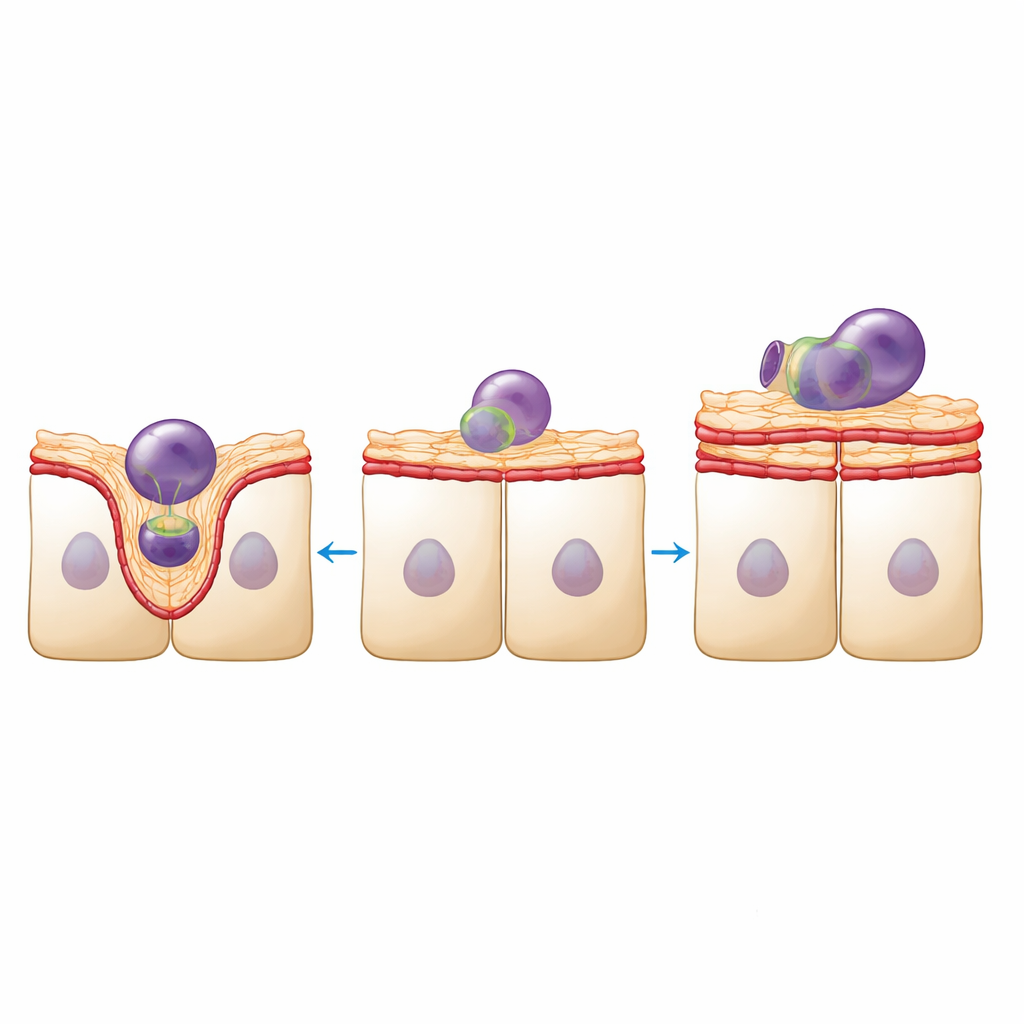
Structuur in dit weefsel gaat niet alleen om uiterlijk; het vormt de basis van functie. RPE‑cellen moeten elke dag talloze fragmenten van fotoreceptoren opnemen en verteren. Met behulp van fluorescent gelabelde fragmenten van varkensretina's maten de onderzoekers deze opruimactiviteit. Dichtheidsverminderde RPE‑lagen internaliseerden in totaal minder fragmenten, maar degenen die ze opnamen waren doorgaans groter. Hoge resolutie beeldvorming toonde de reden: in gezonde lagen bolde het apicale oppervlak omhoog om goed gedefinieerde cups rond elk fragment te vormen, ondersteund door dynamische herschikkingen van actine en myosine. In dichtheidsverminderde lagen zag het oppervlak er gladder en minder vervormbaar uit, met minder duidelijke cupvormen en de verschijning van grote actinerijke uitstulpingen die niet leken te helpen bij het opnemen van deeltjes.
Mechanische homeostase verschuift richting rigiditeit
Om deze visuele veranderingen aan mechanica te koppelen, onderzochten de auteurs de fysieke eigenschappen van het weefsel op twee schalen. Nanoindentatie, waarbij een klein bolvormig puntje in het apicale oppervlak wordt gedrukt, liet zien dat het dichtheidsverminderde RPE ruwweg een derde stugger en veerkrachtiger werd als meercellig blad. Tegelijkertijd waren moleculaire merkers van contractiliteit en junction‑sterkte — gefosforyleerde myosine light chain en het adhesieproteïne vinculine — verrijkt langs cel‑celranden. Brillouin‑microscopie, een lichtgebaseerde methode die lokale stijfheid en watergehalte in cellen detecteert, toonde echter dat de apicale cortex zelf mechanisch onderscheidend en in sommige opzichten zachter werd. Samen suggereren deze bevindingen dat het monolayer zijn laterale verbindingen versterkt om het blad intact te houden terwijl het apicale oppervlak de fijn afgestemde microstructuur verliest die het normaal in staat stelt te buigen en cups rond deeltjes te vormen.
Actineregelaars sturen de balans tussen sterkte en flexibiliteit
Analyse van genexpressie wees op brede herschakeling van de actine‑machinerie in dichtheidsverminderde RPE. Eiwitten die vertakte actinenetwerken en crosslinking bevorderen waren upgereguleerd, terwijl meerdere forminen, die lange lineaire filamenten bevorderen, en ezrin waren gedownreguleerd. Het team manipuleerde deze systemen vervolgens farmacologisch. Het remmen van forminen in normaal RPE maakte het blad stijver en vergrootte de opgenomen fragmenten, deels het verouderingsachtige stadium nabootsend. In dichtheidsverminderde RPE verhoogde het blokkeren van het Arp2/3‑complex, een belangrijkste vertakte‑actine nucleator, het aantal geïnternaliseerde fragmenten en herstelde het meer uitgesproken bol vormen van het apicale oppervlak. Deze ingrepen laten zien dat het bijsturen van actinenucleatie het weefsel kan verschuiven tussen een meer rigide, beschermende configuratie en een meer vervormbare, fagocytose‑vriendelijke toestand.
Wat dit betekent voor verouderende ogen
Samengevat laat het werk zien dat bescheiden celverlies op zichzelf RPE‑weefsel naar een nieuw mechanisch evenwicht kan duwen: het blad wordt sterker aan elkaar genaaid en stugger als geheel, maar het bovenste oppervlak verliest de plasticiteit die nodig is om efficiënt fotoreceptorafval op te nemen. In feite geven de cellen prioriteit aan het bijeenhouden van het weefsel boven het uitvoeren van hun gespecialiseerde opruimtaak. Deze structurele afweging, gedreven door veranderingen in het actinecytoskelet en junctionale spanning in plaats van klassieke biochemische verouderingsschade, kan helpen verklaren waarom oud RPE er vaak intact uitziet maar slecht functioneert. Begrijpen en mogelijk afstemmen van deze balans tussen stabiliteit en flexibiliteit kan nieuwe wegen openen om het gezichtsvermogen te behouden bij aandoeningen zoals leeftijdsgebonden maculadegeneratie.
Bronvermelding: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Trefwoorden: retinaal pigmentepitheel, celmechanica, leeftijdsgebonden maculadegeneratie, actine cytoskelet, fagocytose