Clear Sky Science · es
Pérdida celular altera la homeostasis mecánica para impulsar un fenotipo similar al envejecimiento del epitelio pigmentario retinal in vitro
Por qué las células oculares envejecidas tienen dificultades para mantener la visión clara
A medida que envejecemos, muchas personas desarrollan problemas con la visión central, a menudo relacionados con daño en una capa delgada de células en la parte posterior del ojo llamada epitelio pigmentario retinal (EPR). Estas células trabajan silenciosamente cada día para apoyar a los fotorreceptores que se encuentran por encima de ellas; sin embargo, ha sido difícil precisar cómo la simple pérdida de células con la edad altera su estado físico y socava su función. Este estudio recrea en el laboratorio un escenario similar al envejecimiento y muestra que la pérdida incluso de un número modesto de células del EPR puede "reconfigurar" mecánicamente el tejido restante de maneras que lo hacen más rígido, menos flexible y peor en su tarea principal de eliminar los desechos visuales.
Un modelo de laboratorio cuidadoso del tejido ocular envejecido
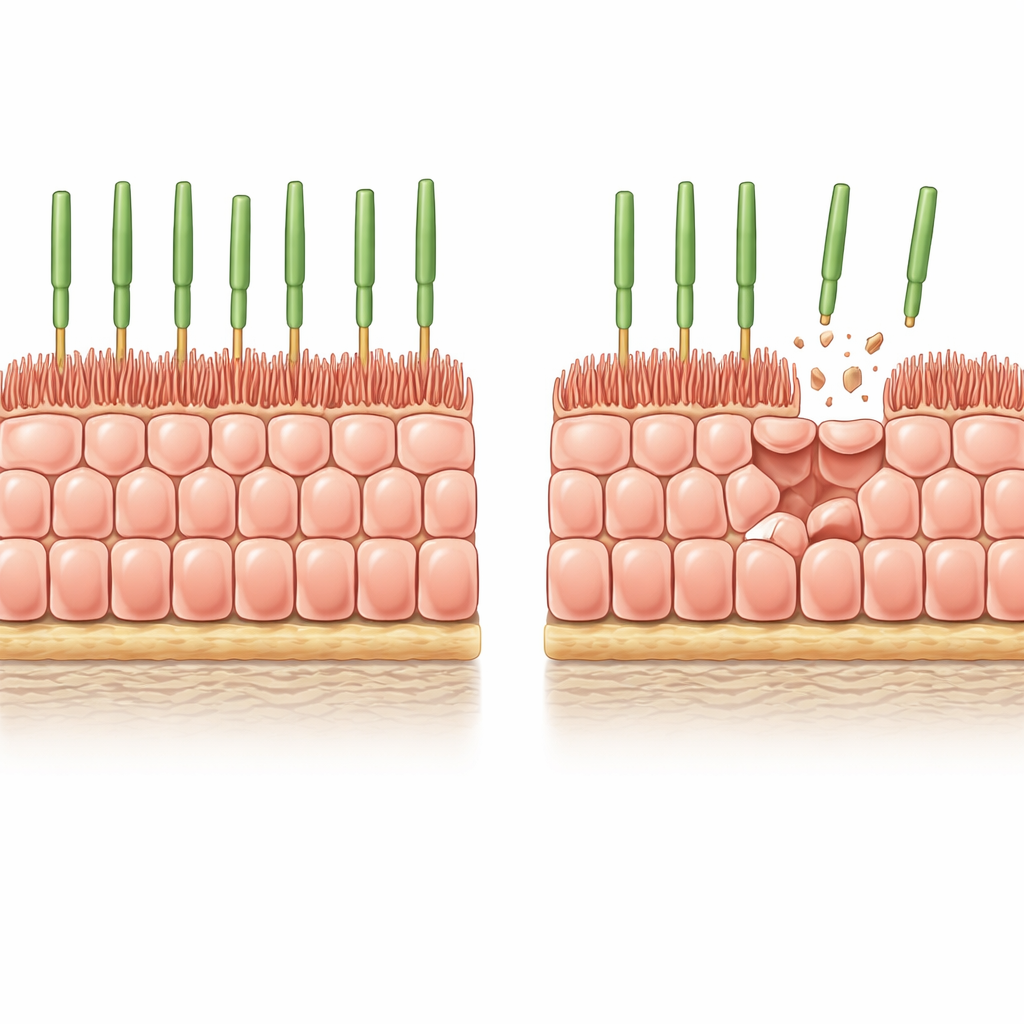
Los investigadores comenzaron con EPR derivado de células madre humanas cultivado como una lámina uniforme y densamente empaquetada sobre un gel blando y biológicamente realista. En estas condiciones, las células dejan de dividirse, adoptan el patrón clásico en panal observado en EPR sano y desarrollan microvellosidades en forma de dedos en su superficie apical que interactúan con los fotorreceptores. Para imitar la pérdida gradual de células que ocurre en el ojo envejecido, el equipo introdujo un interruptor de "suicidio" controlable en las células y después activó una muerte celular parcial y generalizada. Durante unos días, aproximadamente el 8% de las células desapareció, y las supervivientes tuvieron que estirarse para cubrir los huecos sin ayuda de la división celular.
Cómo se remodela la capa celular tras la pérdida
Tras este adelgazamiento inducido, las células EPR restantes se hicieron más anchas pero notablemente más bajas, preservando su volumen mientras se expandían lateralmente para sellar el tejido. Sus microvellosidades apicales se encogieron y se desorganizaron, y algunas células desarrollaron gruesas fibras de estrés de actina que las atravesaban de lado a lado —características también vistas en EPR humano envejecido. Las mediciones confirmaron que proteínas clave asociadas a las microvellosidades, como ezrina y su forma activada fosforilada, estaban reducidas. En otras palabras, la simple pérdida de vecinas fue suficiente para empujar a células estructuralmente jóvenes hacia una arquitectura que se asemeja fuertemente a la del EPR envejecido en el ojo.
Cuando la rigidez se intercambia por la capacidad de limpieza
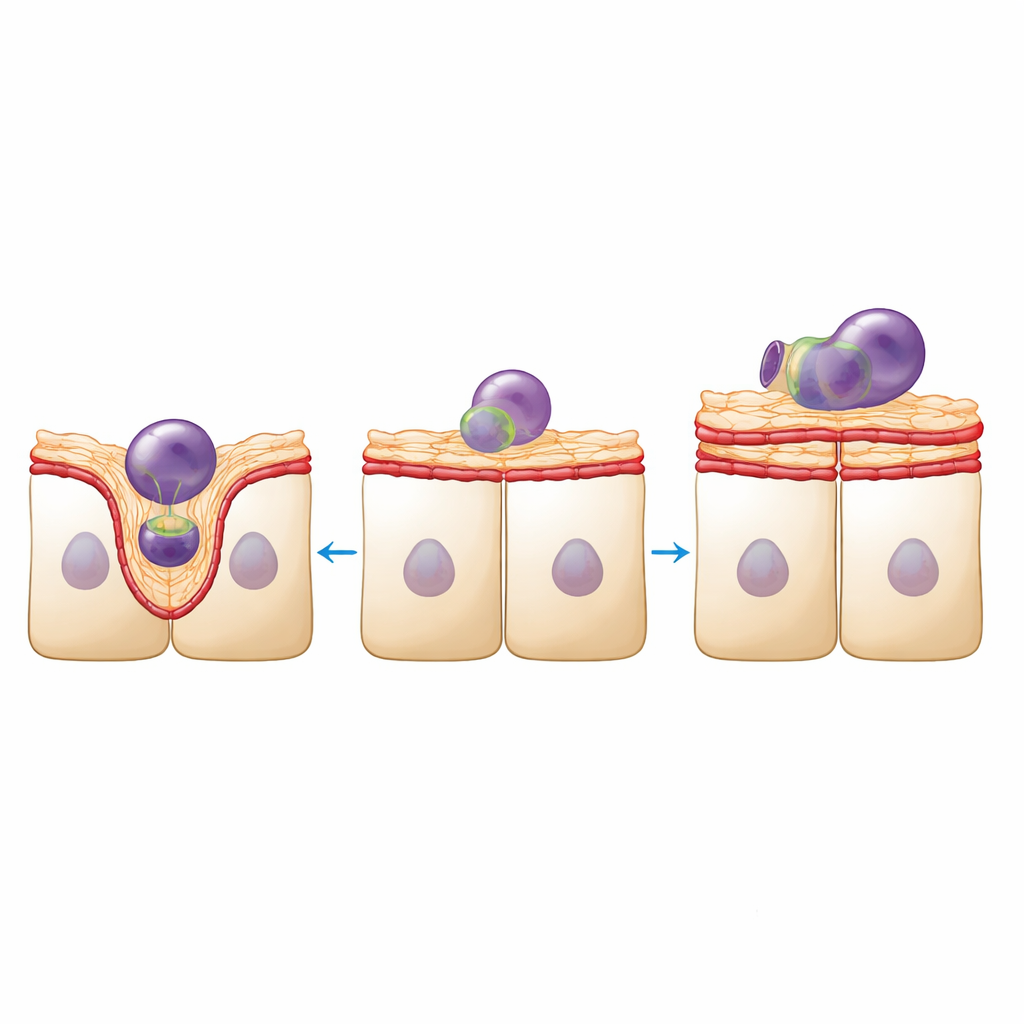
La estructura en este tejido no es solo estética; sustenta la función. Las células del EPR deben ingerir y digerir innumerables fragmentos de los segmentos externos de los fotorreceptores cada día. Usando fragmentos marcados fluorescente procedentes de retina porcina, el equipo midió esta actividad de limpieza. Las láminas de EPR con densidad reducida internalizaron menos fragmentos en conjunto, aunque los fragmentos que sí engullían tendían a ser más grandes. Imágenes de alta resolución mostraron la causa: en láminas sanas, la superficie apical se abultaba hacia arriba formando copas bien definidas alrededor de cada fragmento, sostenidas por reordenamientos dinámicos de actina y miosina. En las láminas con menor densidad, la superficie parecía más lisa y menos deformable, con menos formas de copa claras y la aparición de grandes protrusiones ricas en actina que no parecían ayudar a engullir partículas.
La homeostasis mecánica se desplaza hacia la rigidez
Para vincular estos cambios visuales con la mecánica, los autores sondearon las propiedades físicas del tejido a dos escalas. La nanoindentación, que presiona una punta esférica diminuta en la superficie apical, reveló que el EPR con densidad reducida se volvió aproximadamente un tercio más rígido y más elástico como lámina multicelular. Al mismo tiempo, marcadores moleculares de contractilidad y fuerza en las uniones —la cadena ligera de miosina fosforilada y la proteína de adhesión vinculina— se enriquecieron a lo largo de los bordes entre células. Sin embargo, la microscopía de Brillouin, un método basado en la luz que detecta la rigidez local y el contenido de agua dentro de las células, mostró que la corteza apical en sí se volvió mecánicamente distinta y, en algunos aspectos, más blanda. En conjunto, estos hallazgos sugieren que el monocapa refuerza sus conexiones laterales para mantener la integridad de la lámina mientras que la superficie apical pierde la microestructura finamente ajustada que normalmente le permite doblarse y formar copas alrededor de partículas.
Los reguladores de la actina orientan el equilibrio entre resistencia y flexibilidad
El análisis de expresión génica apuntó a una reconfiguración amplia de la maquinaria de actina en el EPR con densidad reducida. Proteínas que promueven redes de actina ramificada y el entrecruzamiento estuvieron reguladas al alza, mientras que varias forminas, que favorecen filamentos largos y lineales, y ezrina estuvieron reguladas a la baja. El equipo luego moduló farmacológicamente estos sistemas. Inhibir forminas en EPR normal endureció la lámina e hizo que los fragmentos engullidos fueran más grandes, imitando parcialmente el estado similar al envejecimiento. En EPR con densidad reducida, bloquear el complejo Arp2/3, un nucleador clave de actina ramificada, aumentó el número de fragmentos internalizados y restauró un abultamiento apical más pronunciado. Estas intervenciones muestran que ajustar la nucleación de actina puede desplazar el tejido entre una configuración más rígida y protectora y otra más deformable y favorable a la fagocitosis.
Qué significa esto para los ojos envejecidos
En conjunto, el trabajo muestra que una pérdida celular modesta por sí sola puede empujar al tejido del EPR hacia un nuevo equilibrio mecánico: la lámina se vuelve más fuertemente cosida y más rígida en su conjunto, pero su superficie superior pierde la plasticidad necesaria para engullir eficientemente los desechos de los fotorreceptores. En efecto, las células priorizan mantener unido el tejido por encima de desempeñar su función especializada de limpieza. Este compromiso estructural, impulsado por cambios en el citoesqueleto de actina y la tensión en las uniones más que por el daño bioquímico clásico del envejecimiento, puede ayudar a explicar por qué el EPR envejecido a menudo parece intacto pero funciona mal. Comprender y, potencialmente, ajustar este equilibrio entre estabilidad y flexibilidad podría abrir nuevas vías para preservar la visión en trastornos como la degeneración macular relacionada con la edad.
Cita: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Palabras clave: epitelio pigmentario retinal, mecánica celular, dégeneración macular relacionada con la edad, citoesqueleto de actina, fagocitosis