Clear Sky Science · pt
Perda de células perturba a homeostase mecânica e induz fenótipo semelhante ao envelhecimento do epitélio pigmentar da retina in vitro
Por que as células oculares envelhecidas têm dificuldade em manter a visão nítida
À medida que envelhecemos, muitas pessoas desenvolvem problemas de visão central, frequentemente associados a danos em uma camada fina de células na parte posterior do olho chamada epitélio pigmentar da retina (RPE). Essas células trabalham silenciosamente todos os dias para sustentar os fotorreceptores sensíveis à luz acima delas, mas como a simples perda de células com a idade altera seu estado físico e compromete sua função tem sido difícil de definir. Este estudo recria um cenário semelhante ao envelhecimento em laboratório e mostra que a perda mesmo de um número modesto de células RPE pode "reconfigurar" mecanicamente o tecido restante de maneiras que o tornam mais rígido, menos flexível e pior em sua tarefa central de eliminar resíduos visuais.
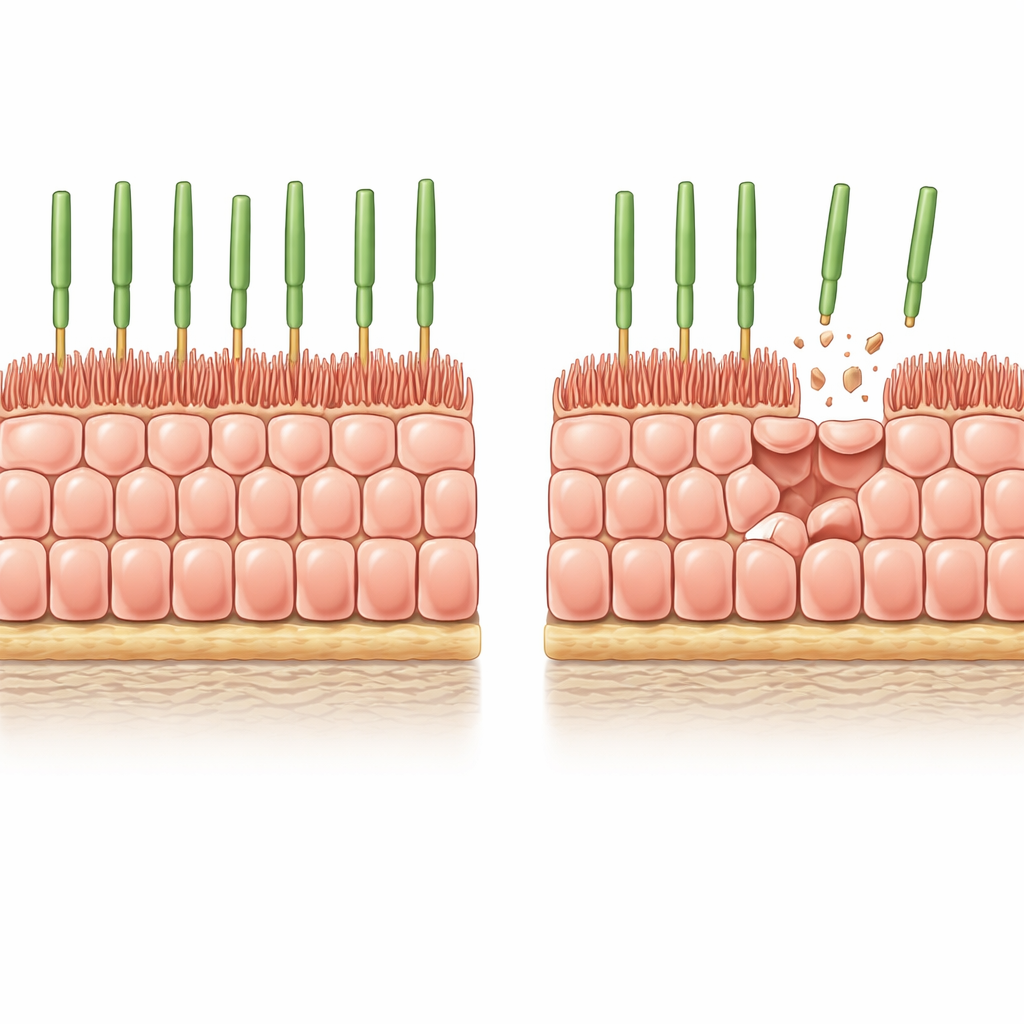
Um modelo laboratorial cuidadoso do tecido ocular envelhecido
Os pesquisadores começaram com RPE derivado de células‑tronco humanas cultivado como uma camada uniforme e bem compacta sobre um gel macio, biologicamente realista. Nestas condições, as células param de se dividir, adotam o padrão clássico em favo de mel observado em RPE saudável e desenvolvem microvilosidades digitiformes em sua superfície apical que interagem com os fotorreceptores. Para mimetizar a perda gradual de células que ocorre no envelhecimento do olho, a equipe introduziu um interruptor controlável de "suicídio" nas células e então desencadeou morte celular disseminada, porém parcial. Ao longo de alguns dias, cerca de 8% das células desapareceram, e as sobreviventes tiveram que se esticar para cobrir os espaços sem auxílio de nova divisão celular.
Como a camada celular se remodela após a perda
Após esse afinamento induzido, as células RPE remanescentes alargaram‑se, mas tornaram‑se visivelmente mais baixas, preservando seu volume enquanto se espalhavam lateralmente para selar o tecido. Suas microvilosidades apicais encolheram e ficaram mais desorganizadas, e algumas células desenvolveram espessas fibras de estresse de actina cruzando‑as—características também observadas em RPE humano envelhecido. Medições confirmaram que proteínas-chave associadas às microvilosidades, como ezrina e sua forma fosforilada ativa, foram reduzidas. Em outras palavras, a simples perda de vizinhos foi suficiente para empurrar células estruturalmente jovens para uma arquitetura que se assemelha fortemente à do RPE envelhecido no olho.
Quando a rigidez compensa a capacidade de limpeza
A estrutura neste tecido não é apenas estética; ela sustenta a função. Células RPE devem ingerir e digerir fragmentos dos segmentos externos dos fotorreceptores continuamente. Usando fragmentos marcados por fluorescência de retinas suínas, a equipe mediu essa atividade de limpeza. As lâminas de RPE com densidade reduzida internalizaram, no total, menos fragmentos, embora os que foram englobados tenderam a ser maiores. Imagens de alta resolução mostraram o porquê: em lâminas saudáveis, a superfície apical se projetava para formar copos bem definidos em torno de cada fragmento, sustentados por rearranjos dinâmicos de actina e miosina. Nas lâminas de densidade reduzida, a superfície parecia mais lisa e menos deformável, com menos formas claras de copo e o aparecimento de grandes protrusões ricas em actina que não pareciam ajudar na internalização de partículas.
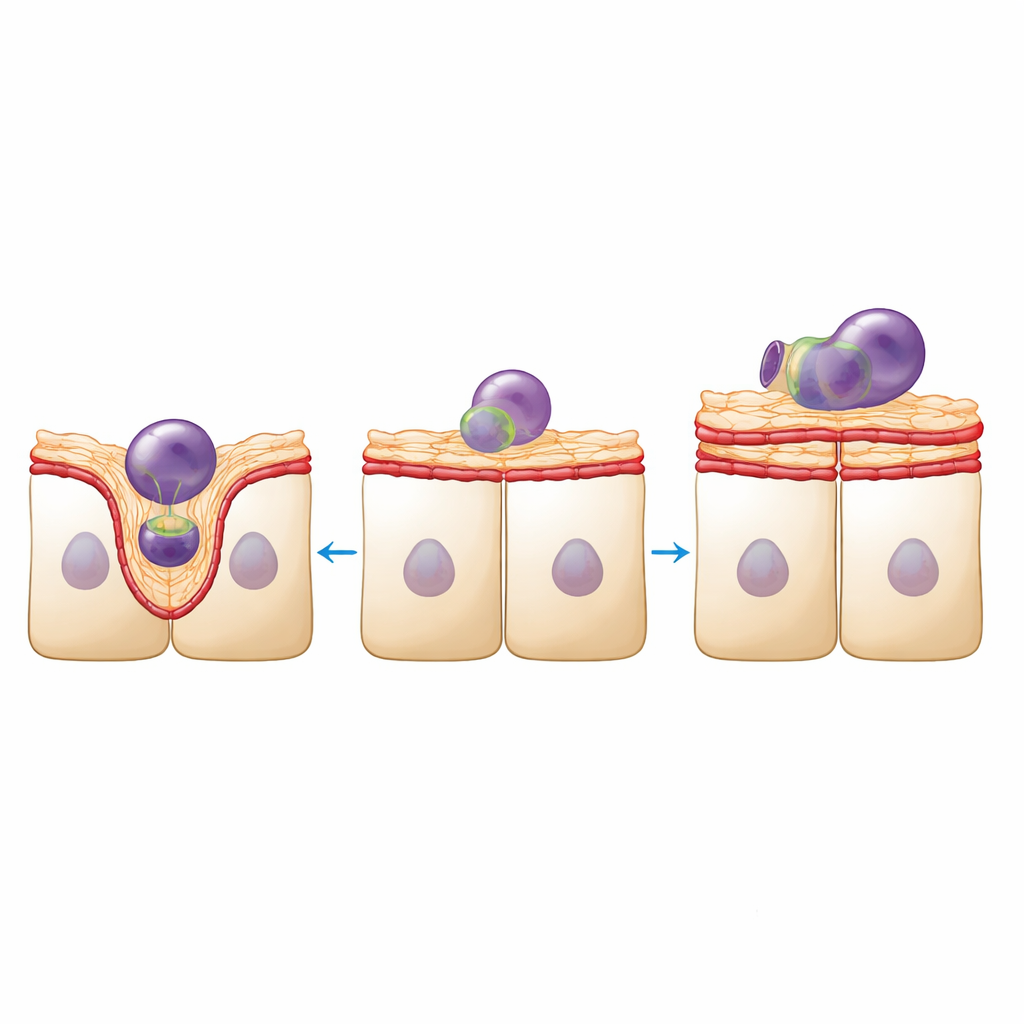
A homeostase mecânica desloca‑se em direção à rigidez
Para relacionar essas mudanças visuais à mecânica, os autores sondaram as propriedades físicas do tecido em duas escalas. Nanoindentação, que pressiona uma pequena ponta esférica na superfície apical, revelou que o RPE com densidade reduzida ficou aproximadamente um terço mais rígido e mais elástico como uma lâmina multicelular. Ao mesmo tempo, marcadores moleculares de contratilidade e força de junção—cadeia leve de miosina fosforilada e a proteína de adesão vinculina—estavam enriquecidos ao longo das bordas entre células. Ainda assim, a microscopia de Brillouin, um método óptico que detecta rigidez local e conteúdo de água dentro das células, mostrou que o córtex apical em si tornou‑se mecanicamente distinto e, em certos aspectos, mais macio. Juntas, essas descobertas sugerem que a monocamada reforça suas conexões laterais para manter a integridade do filme enquanto a superfície apical perde a microestrutura finamente ajustada que normalmente lhe permite dobrar‑se e formar copos em torno das partículas.
Reguladores da actina guiam o equilíbrio entre força e flexibilidade
A análise de expressão gênica apontou para uma ampla reconfiguração da maquinaria de actina no RPE com densidade reduzida. Proteínas que promovem redes de actina ramificadas e entrelaçamento foram reguladas positivamente, enquanto vários formins, que favorecem filamentos longos e lineares, e ezrina foram regulados negativamente. A equipe então modulou esses sistemas farmacologicamente. Inibir formins em RPE normal tornou a lâmina mais rígida e fez com que os fragmentos englobados fossem maiores, mimetizando parcialmente o estado semelhante ao envelhecimento. No RPE com densidade reduzida, bloquear o complexo Arp2/3, um nucleador-chave de actina ramificada, aumentou o número de fragmentos internalizados e restaurou saliências apicais mais pronunciadas. Essas intervenções mostram que ajustar a nucleação de actina pode deslocar o tecido entre uma configuração mais rígida e protetora e outra mais deformável e favorável à fagocitose.
O que isso significa para olhos envelhecidos
Em conjunto, o trabalho mostra que a perda modesta de células por si só pode levar o tecido RPE a um novo equilíbrio mecânico: a lâmina torna‑se mais fortemente costurada e mais rígida como um todo, mas sua superfície superior perde a plasticidade necessária para englobar de forma eficiente os detritos dos fotorreceptores. Em efeito, as células privilegiam manter o tecido coeso em detrimento de sua função especializada de limpeza. Essa troca estrutural, impulsionada por alterações no citoesqueleto de actina e na tensão junçãoal em vez dos danos bioquímicos clássicos do envelhecimento, pode ajudar a explicar por que o RPE envelhecido frequentemente parece intacto, mas funciona mal. Entender e, potencialmente, ajustar esse equilíbrio entre estabilidade e flexibilidade pode abrir novos caminhos para preservar a visão em doenças como a degeneração macular relacionada à idade.
Citação: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Palavras-chave: epitélio pigmentar da retina, mecânica celular, degeneração macular relacionada à idade, citoesqueleto de actina, fagocitose