Clear Sky Science · fr
La perte cellulaire perturbe l’homéostasie mécanique pour provoquer un phénotype de vieillissement du pigment épithélial rétinien in vitro
Pourquoi les cellules oculaires vieillissantes peinent à maintenir une vision claire
En vieillissant, de nombreuses personnes développent des problèmes de vision centrale, souvent liés à des dommages d’une fine couche de cellules à l’arrière de l’œil appelée épithélium pigmentaire rétinien (RPE). Ces cellules travaillent discrètement chaque jour pour soutenir les photorécepteurs sensibles à la lumière qui se trouvent au‑dessus d’elles, et pourtant il a été difficile de déterminer comment une simple perte cellulaire liée à l’âge modifie leur état physique et compromet leur fonction. Cette étude recrée en laboratoire un scénario proche du vieillissement et montre que la disparition même d’un nombre modeste de cellules RPE peut « reconfigurer » mécaniquement le tissu restant de manière à le rendre plus rigide, moins flexible et moins efficace pour sa tâche principale de recyclage des déchets visuels.
Un modèle expérimental soigné du tissu oculaire vieillissant
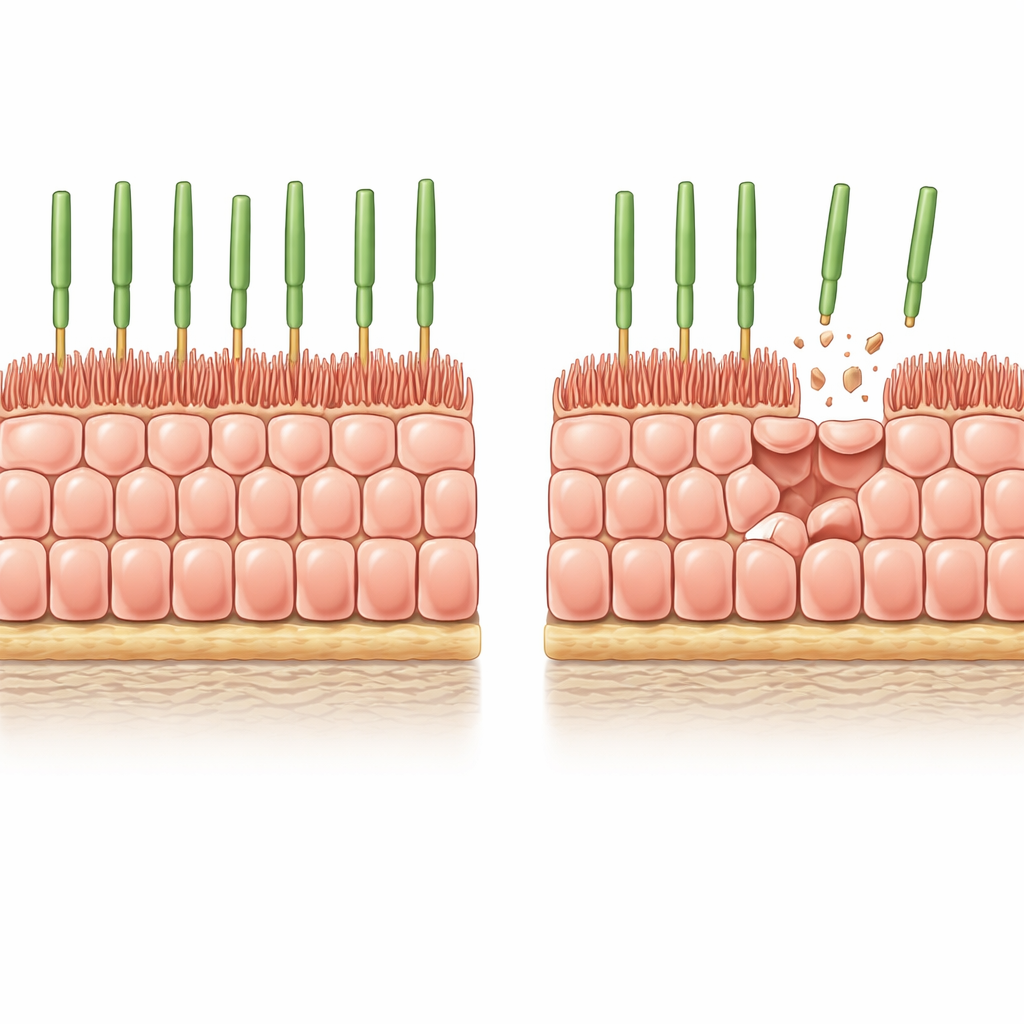
Les chercheurs ont commencé par des RPE dérivées de cellules souches humaines, cultivées en une nappe uniforme et étroitement compacte sur un gel mou à caractère biologique réaliste. Dans ces conditions, les cellules cessent de se diviser, adoptent le motif alvéolé classique observé dans un RPE sain et développent des microvillosités en « doigts » sur leur face apicale en contact avec les photorécepteurs. Pour imiter la perte cellulaire progressive qui survient avec l’âge, l’équipe a introduit un interrupteur « suicide » contrôlable dans les cellules puis a déclenché une mort cellulaire partielle et étendue. En quelques jours, environ 8 % des cellules avaient disparu, et les survivantes ont dû s’étirer pour combler les vides sans bénéficier d’une division cellulaire compensatrice.
Comment la couche cellulaire se reconfigure après la perte
Après cet amincissement forcé, les cellules RPE restantes se sont élargies mais sont devenues visiblement plus courtes, préservant leur volume tout en s’étalant latéralement pour sceller le tissu. Leurs microvillosités apicales ont rétréci et se sont désorganisées, et certaines cellules ont développé d’épaisses fibres de stress d’actine traversant la cellule — des caractéristiques également observées dans le RPE humain âgé. Les mesures ont confirmé que des protéines clés associées aux microvillosités, comme l’ezrine et sa forme phosphorylée active, étaient diminuées. En d’autres termes, la simple perte de voisins suffisait à pousser des cellules structurellement jeunes vers une architecture très semblable à celle du RPE âgé de l’œil.
Quand la rigidité se fait au détriment du nettoyage
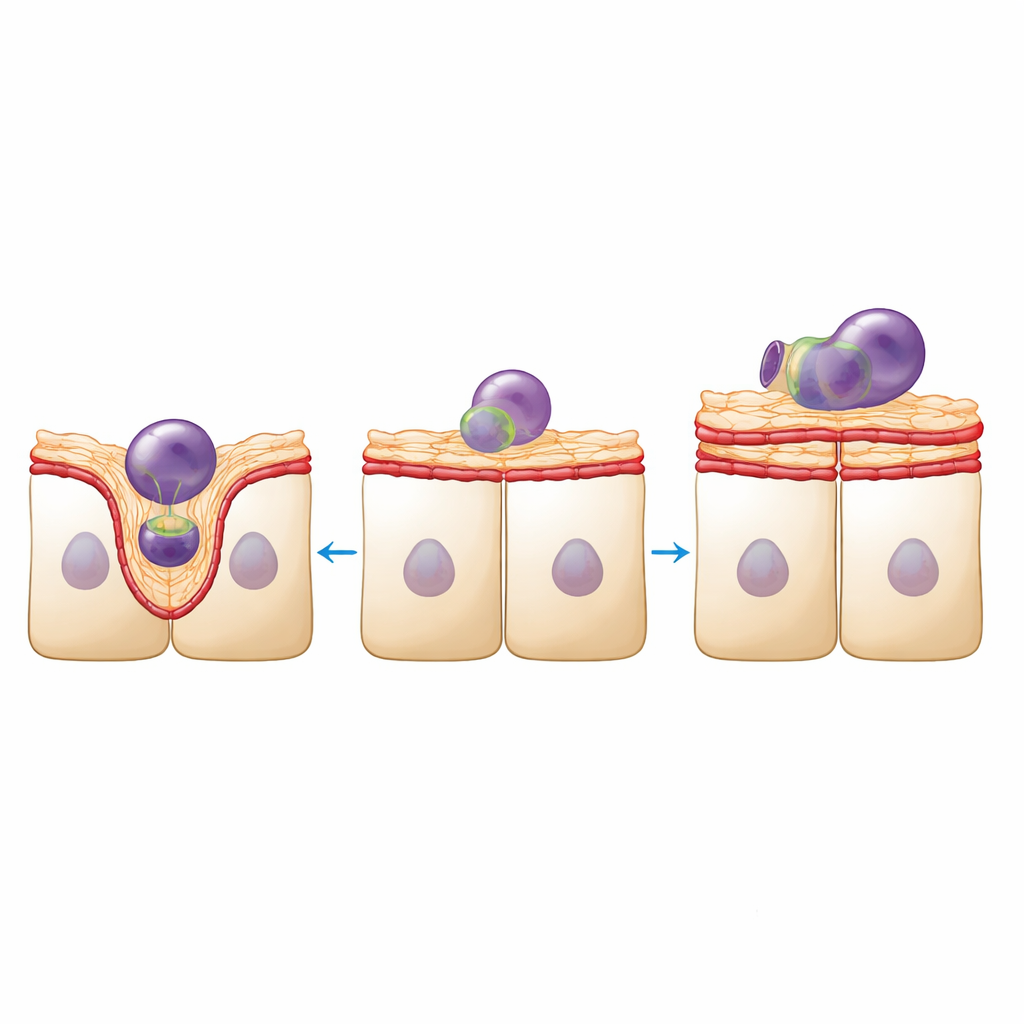
La structure de ce tissu n’est pas qu’esthétique ; elle sous‑tend la fonction. Les cellules RPE doivent ingérer et digérer quotidiennement d’innombrables fragments issus des segments externes des photorécepteurs. En utilisant des fragments marqués par fluorescence issus de rétines porcines, l’équipe a mesuré cette activité de nettoyage. Les nappes de RPE à densité réduite ont internalisé moins de fragments au total, mais ceux qu’elles ont phagocytés avaient tendance à être plus volumineux. L’imagerie haute résolution a expliqué pourquoi : dans les nappes saines, la surface apicale se bombait pour former des coupelles bien définies autour de chaque fragment, soutenues par des réarrangements dynamiques d’actine et de myosine. Dans les nappes à densité réduite, la surface paraissait plus lisse et moins déformable, avec moins de formes de coupelles évidentes et l’apparition de larges protrusions riches en actine qui ne semblaient pas aider à englober les particules.
L’homéostasie mécanique bascule vers la rigidité
Pour relier ces modifications visuelles à la mécanique, les auteurs ont sondé les propriétés physiques du tissu à deux échelles. La nanoindentation, qui enfonce une petite pointe sphérique dans la surface apicale, a révélé que le RPE à densité réduite devenait environ un tiers plus dur et plus élastique en tant que nappe multicellulaire. Parallèlement, des marqueurs moléculaires de contractilité et de solidité des jonctions — la chaîne légère de myosine phosphorylée et la protéine d’adhésion vinculine — étaient enrichis le long des bords cellule‑cellule. Pourtant, la microscopie de Brillouin, méthode optique sensible à la rigidité locale et au contenu en eau à l’intérieur des cellules, montrait que le cortex apical lui‑même devenait mécaniquement distinct et, à certains égards, plus mou. Ensemble, ces résultats suggèrent que la monocouche renforce ses connexions latérales pour maintenir l’intégrité de la nappe tandis que la surface apicale perd la microstructure finement réglée qui lui permettait normalement de se courber et de former des coupelles autour des particules.
Les régulateurs de l’actine orientent l’équilibre entre solidité et souplesse
L’analyse de l’expression génique a mis en évidence une réorganisation large de la machinerie d’actine dans le RPE à densité réduite. Les protéines favorisant les réseaux d’actine branchés et le réticulage étaient surexprimées, tandis que plusieurs formines, qui favorisent les filaments longs et linéaires, et l’ezrine étaient sous‑exprimées. L’équipe a ensuite modulé ces systèmes pharmacologiquement. Inhiber les formines dans un RPE normal rigidifiait la nappe et augmentait la taille des fragments internalisés, reproduisant partiellement l’état proche du vieillissement. Dans le RPE à densité réduite, bloquer le complexe Arp2/3, un nucléateur clé de l’actine branchée, augmentait le nombre de fragments internalisés et rétablissait un bombement apical plus prononcé. Ces interventions montrent que jouer sur la nucléation de l’actine peut faire basculer le tissu entre une configuration plus rigide et protectrice et une configuration plus déformable, favorable à la phagocytose.
Ce que cela signifie pour les yeux vieillissants
En somme, le travail montre qu’une perte cellulaire modeste suffit à pousser le tissu RPE vers un nouvel équilibre mécanique : la nappe devient plus fortement soudée et plus rigide dans son ensemble, mais sa surface supérieure perd la plasticité nécessaire pour engloutir efficacement les débris de photorécepteurs. En pratique, les cellules privilégient le maintien de l’intégrité du tissu au détriment de leur fonction spécialisée de nettoyage. Cet arbitrage structurel, piloté par des modifications du cytosquelette d’actine et de la tension jonctionnelle plutôt que par des dommages biochimiques classiques liés à l’âge, pourrait expliquer pourquoi le RPE âgé semble souvent intact tout en fonctionnant mal. Comprendre et potentiellement ajuster cet équilibre entre stabilité et flexibilité pourrait ouvrir de nouvelles voies pour préserver la vision dans des maladies comme la dégénérescence maculaire liée à l’âge.
Citation: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Mots-clés: épithélium pigmentaire rétinien, mécanique cellulaire, dégénérescence maculaire liée à l’âge, cytosquelette d’actine, phagocytose