Clear Sky Science · sv
Cellförlust rubbar mekanisk homeostas och driver ett åldringsliknande fenotyp i retinalt pigmentepitel in vitro
Varför åldrande ögonceller har svårt att hålla synen klar
När vi åldras utvecklar många problem med central syn, ofta kopplat till skador i ett tunt cellager längst bak i ögat som kallas retinalt pigmentepitel (RPE). Dessa celler arbetar tyst varje dag för att stödja de ljuskänsliga fotoreceptorerna ovanför dem, men hur enkel cellförlust vid ålder förändrar deras fysiska tillstånd och undergräver deras funktion har varit svår att fastställa. Denna studie återskapar ett åldringsliknande scenario i laboratoriet och visar att förlust av även ett måttligt antal RPE‑celler kan mekaniskt ”omkoppla” den kvarvarande vävnaden på sätt som gör den styvare, mindre flexibel och sämre på sin kärnuppgift att städa upp visuellt avfall.
En noggrann laboratoriemodell av åldrande ögonvävnad
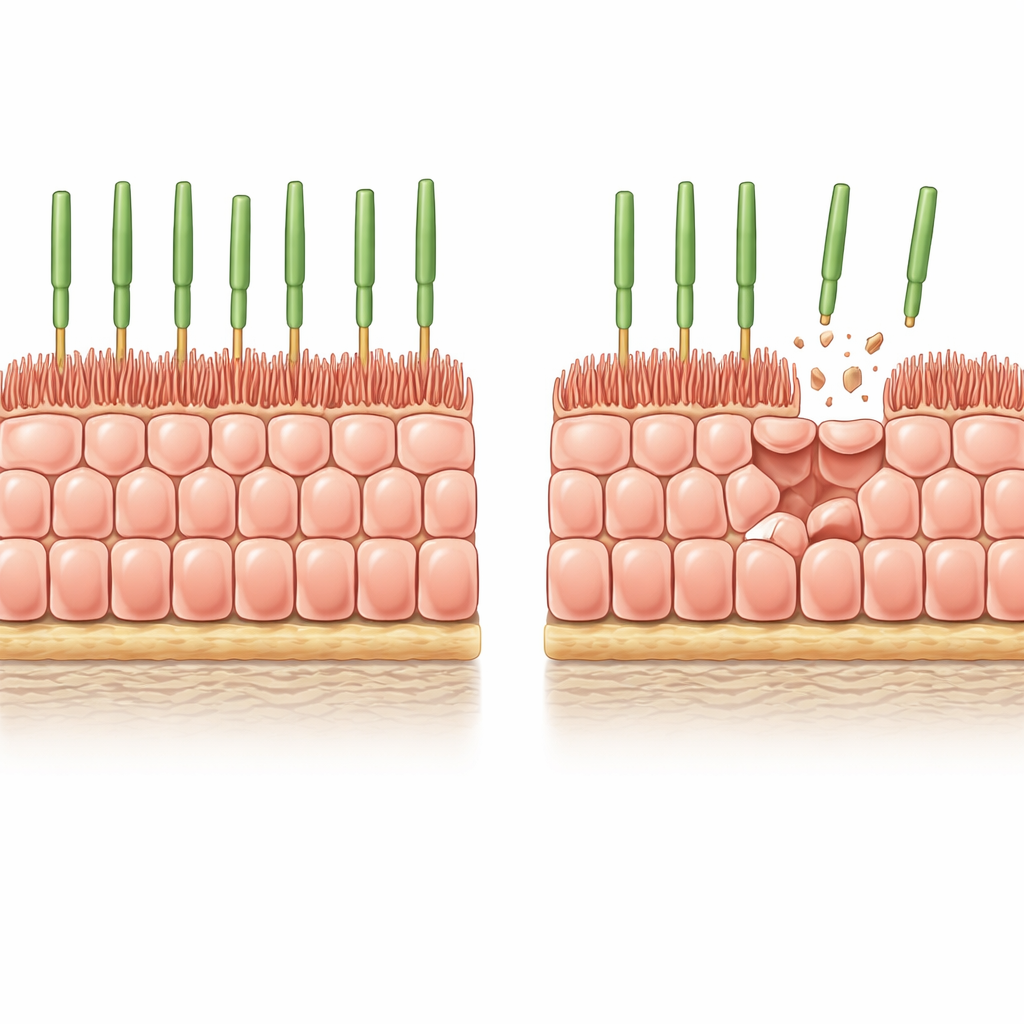
Forskarna började med mänskligt stamcellsderiverat RPE odlat som ett homogent, tätt packat skikt på ett mjukt, biologiskt realistiskt gelmaterial. Under dessa förhållanden slutar cellerna dela sig, antar det klassiska bikakemönstret som ses i friskt RPE och utvecklar fingerlika mikrovilli på sin övre yta som interagerar med fotoreceptorer. För att efterlikna den gradvisa cellförlust som sker i det åldrande ögat introducerade teamet en kontrollerbar ”självmords”brytare i cellerna och utlöste sedan omfattande men partiell celldöd. Över några dagar försvann ungefär 8 % av cellerna, och överlevarna tvingades sträcka ut sig för att täcka luckorna utan hjälp av ny celldelning.
Hur cellagret omformar sig efter förlust
Efter denna inducerade utglesning blev de kvarvarande RPE‑cellerna bredare men märkbart kortare, och bevarade sin volym samtidigt som de spred ut sig sidledes för att täta vävnaden. Deras apikala mikrovilli krympte och blev mer oorganiserade, och vissa celler utvecklade tjocka aktinstressfibrer som löpte rakt över dem — drag som också ses i åldrad mänsklig RPE. Mätningar bekräftade att nyckelproteiner associerade med mikrovilli, såsom ezrin och dess aktiva fosforylerade form, var minskade. Med andra ord var enkel förlust av grannar tillräcklig för att tvinga strukturellt unga celler in i en arkitektur som starkt liknar den hos gammalt RPE i ögat.
När styvhet byts mot rengöringsförmåga
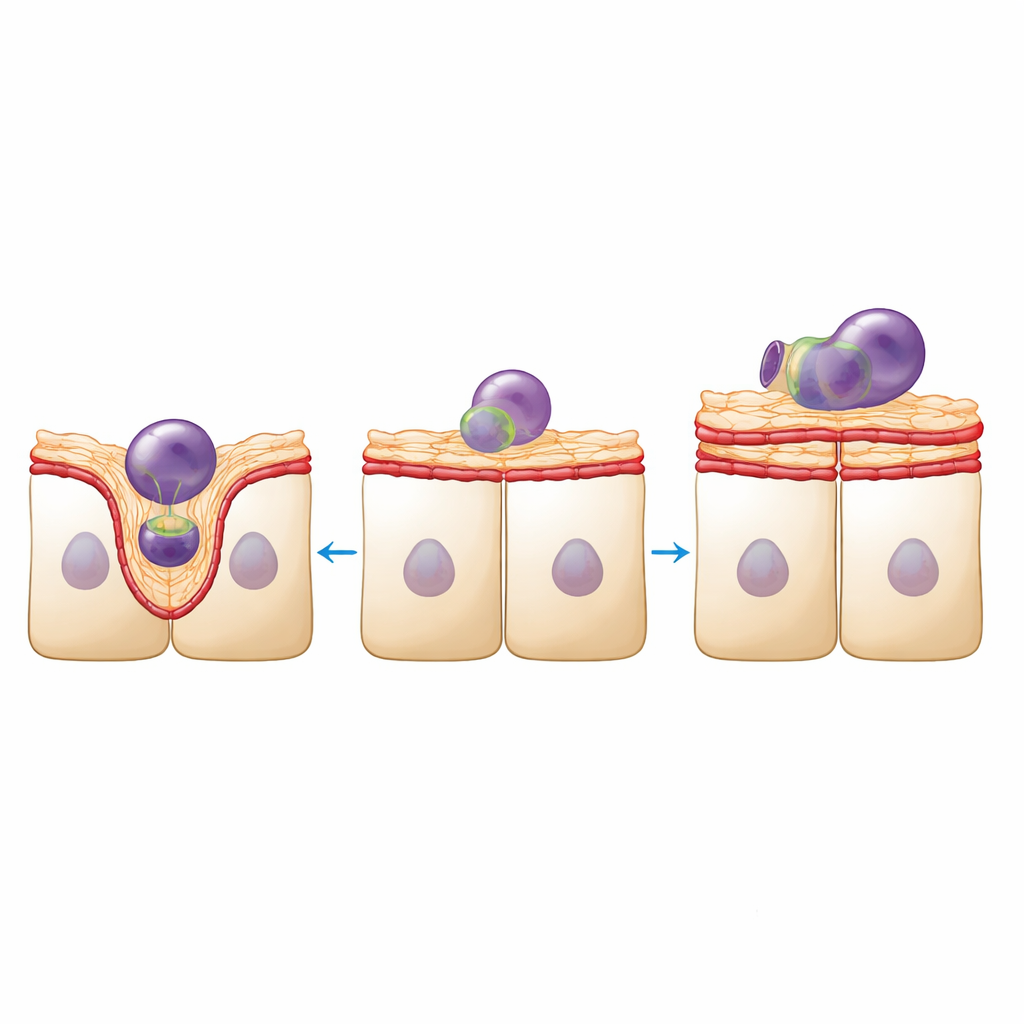
Struktur i denna vävnad handlar inte bara om utseende; den ligger också till grund för funktion. RPE‑celler måste inta och smälta otaliga fragment från fotoreceptorernas yttre segment varje dag. Genom att använda fluorescensmärka fragment från grisretinas mätte teamet denna städfunktion. Tätleksreducerade RPE‑skikt internaliserade färre fragment totalt, men de fragment som de väl fångade tenderade att vara större. Högupplöst avbildning visade varför: i friska skikt buktade den apikala ytan uppåt för att bilda välavgränsade koppar runt varje fragment, stödda av dynamisk aktin‑ och myosinomarrangemang. I tätleksreducerade skikt såg ytan slätare och mindre deformbar ut, med färre tydliga koppformer och framträdandet av stora aktinrika utstickare som inte verkade hjälpa till att omsluta partiklarna.
Mekanisk homeostas förskjuts mot styvhet
För att koppla dessa visuella förändringar till mekanik undersökte författarna vävnadens fysiska egenskaper på två skalor. Nanoindentation, som pressar en liten sfärisk spets in i den apikala ytan, visade att det tätleksreducerade RPE ungefär blev en tredjedel styvare och mer elastiskt som ett multicellulärt skikt. Samtidigt var molekylära markörer för kontraktilitet och kontaktstyrka — fosforylerad myosin light chain och adhesionsproteinet vinculin — förhöjda längs cell‑cell‑gränserna. Men Brillouin‑mikroskopi, en ljusburen metod som känner av lokal styvhet och vatteninnehåll inne i celler, visade att den apikala kortexen faktiskt blev mekaniskt distinkt och i vissa avseenden mjukare. Tillsammans antyder dessa fynd att monolagret förstärker sina laterala förbindelser för att hålla skiktet intakt medan den apikala ytan förlorar den finstämda mikrostruktur som normalt tillåter den att böja sig och bilda koppar runt partiklar.
Aktinregulatorer styr balansen mellan styrka och flexibilitet
Genuttrycksanalys pekade på en omfattande omkoppling av aktinmaskineriet i tätleksreducerat RPE. Proteiner som främjar grenade aktinnätverk och korsbindning var uppreglerade, medan flera forminer, som gynnar långa, linjära filament, och ezrin var nedreglerade. Teamet petade sedan farmakologiskt i dessa system. Att hämma forminer i normalt RPE gjorde skiktet styvare och gjorde de intagna fragmenten större, delvis efterliknande det åldringsliknande tillståndet. I tätleksreducerat RPE ökade blockering av Arp2/3‑komplexet, en nyckelnukleator för grenade aktin, antalet internaliserade fragment och återställde mer uttalad uppbuktning av den apikala ytan. Dessa interventioner visar att finjustering av aktinnukleation kan skifta vävnaden fram och tillbaka mellan en mer styv, skyddande konfiguration och en mer deformabel, fagocytosvänlig sådan.
Vad detta betyder för åldrande ögon
Sammantaget visar arbetet att måttlig cellförlust i sig kan föra RPE‑vävnad till ett nytt mekaniskt jämviktsläge: skiktet blir starkare ihopsytt och stelare som helhet, men dess överyta förlorar den plasticitet som behövs för att effektivt omsluta fotoreceptoravfall. I praktiken prioriterar cellerna att hålla vävnaden samman framför att utföra sin specialiserade rengöringsuppgift. Denna strukturella avvägning, driven av förändringar i aktincytoskelettet och junctionell spänning snarare än av klassisk biokemisk åldersskada, kan bidra till att förklara varför åldrat RPE ofta ser intakt ut men fungerar dåligt. Att förstå och potentiellt justera denna balans mellan stabilitet och flexibilitet kan öppna nya vägar för att bevara synen vid tillstånd som åldersrelaterad makuladegeneration.
Citering: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Nyckelord: retinalt pigmentepitel, cellmekanik, åldersrelaterad makuladegeneration, aktin cytoskelett, fagocytos