Clear Sky Science · ru
Потеря клеток нарушает механическую гомеостазу и вызывает в культуре фенотип, похожий на старение пигментного эпителия сетчатки
Почему стареющим клеткам глаза сложнее сохранять ясное зрение
С возрастом у многих людей возникают проблемы с центральным зрением, часто связанные с повреждением тонкого слоя клеток на задней стенке глаза, называемого пигментным эпителием сетчатки (RPE). Эти клетки ежедневно тихо поддерживают расположенные над ними светочувствительные фоторецепторы, однако было трудно понять, как простая потеря клеток с возрастом меняет их физическое состояние и нарушает функцию. В исследовании в лабораторных условиях воспроизведена сходная со старением ситуация: показано, что утрата даже умеренного числа клеток RPE может механически «перестроить» оставшуюся ткань так, что она становится жестче, менее гибкой и хуже справляется со своей ключевой задачей — уборкой зрительного мусора.
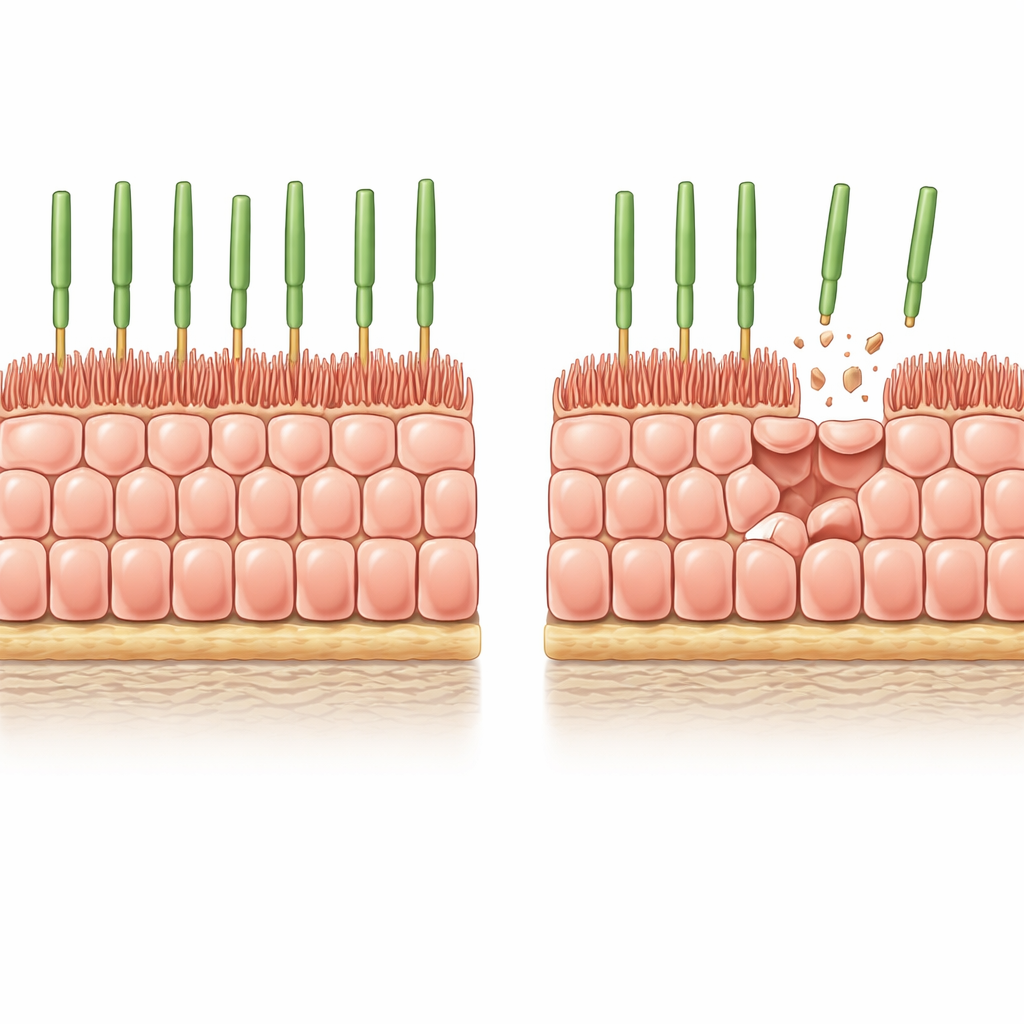
Тщательно продуманная лабораторная модель стареющей ткани глаза
Исследователи начали с RPE, полученных из человеческих стволовых клеток и выращенных в виде однородного, плотно упакованного слоя на мягком, биологически реалистичном геле. В этих условиях клетки прекращали деление, принимали классический «сотовый» рисунок, характерный для здорового RPE, и развивали пальцеподобные микроворсинки на апикальной поверхности, взаимодействующие с фоторецепторами. Чтобы смоделировать постепенную потерю клеток при старении, команда внедрила в клетки управляемый «самоубийственный» переключатель и затем вызвала широкомасштабную, но частичную гибель клеток. В течение нескольких дней примерно 8 % клеток исчезли, и выжившим пришлось растягиваться, чтобы закрыть пробелы без помощи нового клеточного деления.
Как слой клеток перестраивается после утраты
После индуцированного истончения оставшиеся клетки RPE расширились в ширину, но заметно укоротились по высоте, сохраняя объём и распространяясь в стороны, чтобы заделать ткань. Их апикальные микроворсинки уменьшились и стали более неорганизованными, а у некоторых клеток появились толстые актиновые стресс‑фибриллы, проходящие через клетку — черты, также наблюдаемые в старом человеческом RPE. Измерения подтвердили снижение ключевых белков, связанных с микроворсинками, таких как эзрин и его активная фосфорилированная форма. Иными словами, простая потеря соседей была достаточна, чтобы заставить структурно молодые клетки перейти в архитектуру, сильно напоминающую стареющий RPE в глазу.
Когда жёсткость достигается за счёт способности к очистке
Структура ткани важна не только внешне; она определяет функцию. Клетки RPE ежедневно поглощают и переваривают множество фрагментов наружных сегментов фоторецепторов. Используя флуоресцентно меченые фрагменты свиной сетчатки, команда измеряла эту очистительную активность. Слои RPE с пониженной плотностью в целом захватывали меньше фрагментов, но те, которые поглощались, были склонны быть большего размера. Высокорасширенное изображение показало причину: в здоровых слоях апикальная поверхность выпячивалась вверх, образуя хорошо очерченные «чашечки» вокруг каждого фрагмента, поддерживаемые динамичными перестройками актина и миозина. В слоях с пониженной плотностью поверхность выглядела более гладкой и менее деформируемой, с меньшим количеством четких чашеобразных структур и с появлением крупных актиновых выступов, которые, по-видимому, не способствовали захвату частиц.
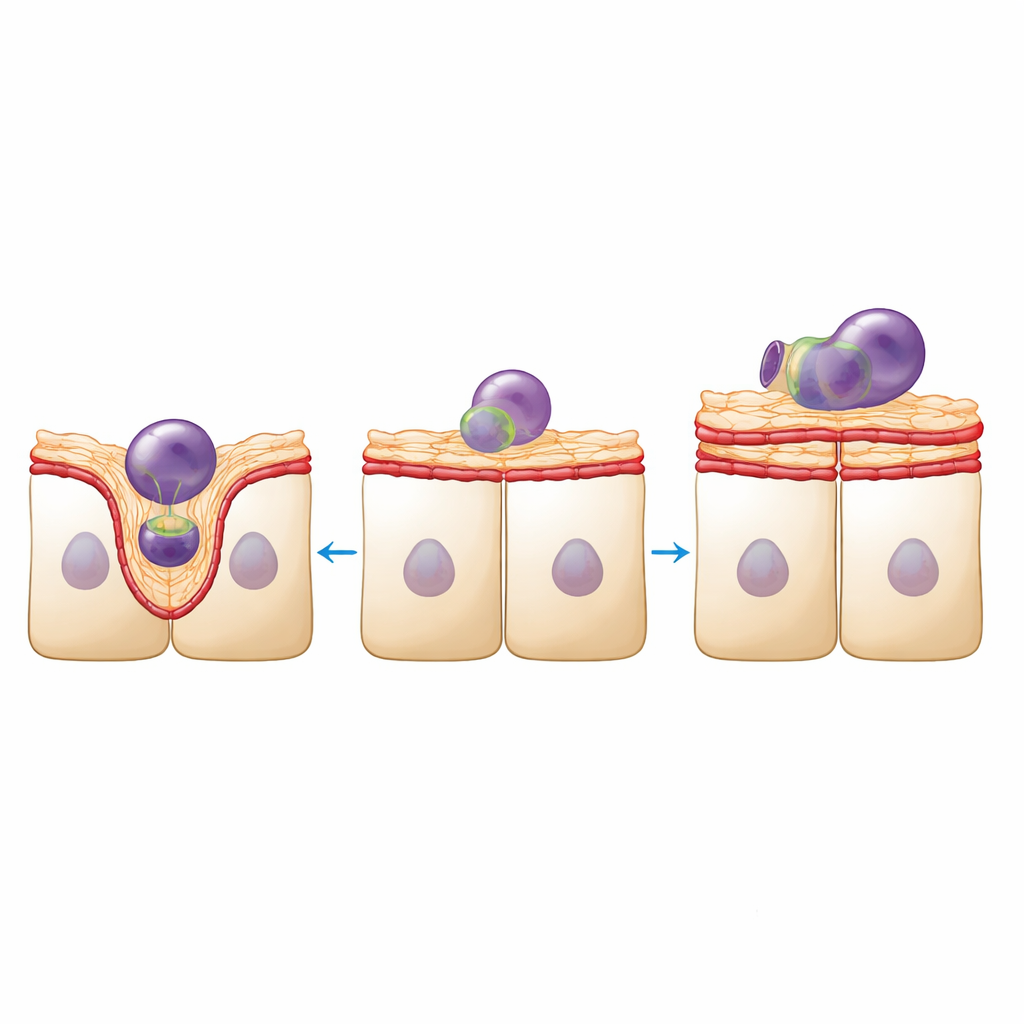
Механическая гомеостаз смещается в сторону жёсткости
Чтобы связать визуальные изменения с механикой, авторы исследовали физические свойства ткани на двух масштабах. Наноиндентация, при которой маленький сферический зонд вдавливается в апикальную поверхность, показала, что слой RPE с пониженной плотностью стал примерно на треть жестче и более упругим как многоклеточный лист. В то же время молекулярные маркеры контрактиility и прочности контактов — фосфорилированная регуляторная субъединица миозина и адгезионный белок винкулин — были обогащены вдоль границ между клетками. Однако методом Бриллюэна‑микроскопии, оптическим способом, чувствительным к локальной жесткости и содержанию воды внутри клеток, было показано, что сама апикальная кортикальная зона механически изменилась и в некоторых отношениях стала мягче. В совокупности эти наблюдения указывают на то, что монослой усиливает свои боковые соединения, чтобы сохранить целостность листа, в то время как апикальная поверхность теряет тонкую микроструктуру, которая обычно позволяет ей изгибаться и образовывать чашечки вокруг частиц.
Регуляторы актина управляют балансом прочности и гибкости
Анализ экспрессии генов выявил широкую перепрограммировку актиновой системы в слоях RPE с пониженной плотностью. Белки, способствующие разветвленным актиновым сетям и перекрестному связыванию, были выше по экспрессии, тогда как несколько форминов, которые стимулируют длинные линейные нити, и эзрин были понижены. Команда затем фармакологически модифицировала эти системы. Ингибирование форминов в нормальном RPE делало слой жестче и увеличивало размер поглощаемых фрагментов, частично имитируя состояние, похожее на старение. В RPE с пониженной плотностью блокировка комплекса Arp2/3, ключевого инициатора разветвленного актина, увеличивала число захватываемых фрагментов и восстанавливала более выраженное выпячивание апикальной поверхности. Эти вмешательства показывают, что изменение нуклеации актина может сдвинуть ткань между более жёсткой, защитной конфигурацией и более деформируемой, благоприятной для фагоцитоза.
Что это значит для стареющих глаз
В совокупности работа демонстрирует, что умеренная потеря клеток сама по себе может сдвинуть ткань RPE в новый механический баланс: лист становится плотнее сшит и жестче в целом, но его верхняя поверхность теряет пластичность, необходимую для эффективного захвата обломков фоторецепторов. Фактически клетки жертвуют способностью выполнять специализированную очистительную функцию ради сохранения целостности ткани. Эта структурная компромисса, вызванная изменениями в актиновом цитоскелете и напряжении в соединениях, а не классическими биохимическими признаками старения, может помочь объяснить, почему стареющий RPE часто выглядит неповрежденным, но функционирует плохо. Понимание и потенциальная настройка этого баланса между стабильностью и гибкостью могут открыть новые пути для сохранения зрения при заболеваниях, таких как возрастная макулярная дегенерация.
Цитирование: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Ключевые слова: пигментный эпителий сетчатки, механика клеток, возрастная макулярная дегенерация, актиновый цитоскелет, фагоцитоз