Clear Sky Science · pl
Utrata komórek zaburza mechaniczną homeostazę, wywołując w in vitro fenotyp przypominający starzenie barwnikowego nabłonka siatkówki
Dlaczego starzejące się komórki oka mają problemy z utrzymaniem ostrości widzenia
W miarę starzenia się wiele osób rozwija zaburzenia widzenia centralnego, często związane z uszkodzeniem cienkiej warstwy komórek w tylnej części oka zwanej barwnikowym nabłonkiem siatkówki (RPE). Komórki te codziennie wspierają światłoczułe fotoreceptory nad nimi, jednak trudno było ustalić, jak samo utracenie komórek wraz z wiekiem zmienia ich stan fizyczny i osłabia ich funkcję. W tym badaniu odtworzono w laboratorium scenariusz przypominający starzenie i wykazano, że utrata nawet umiarkowanej liczby komórek RPE może mechanicznie „przestawić” pozostałą tkankę tak, że staje się ona bardziej sztywna, mniej elastyczna i gorzej radzi sobie z podstawowym zadaniem usuwania odpadów wzrokowych.
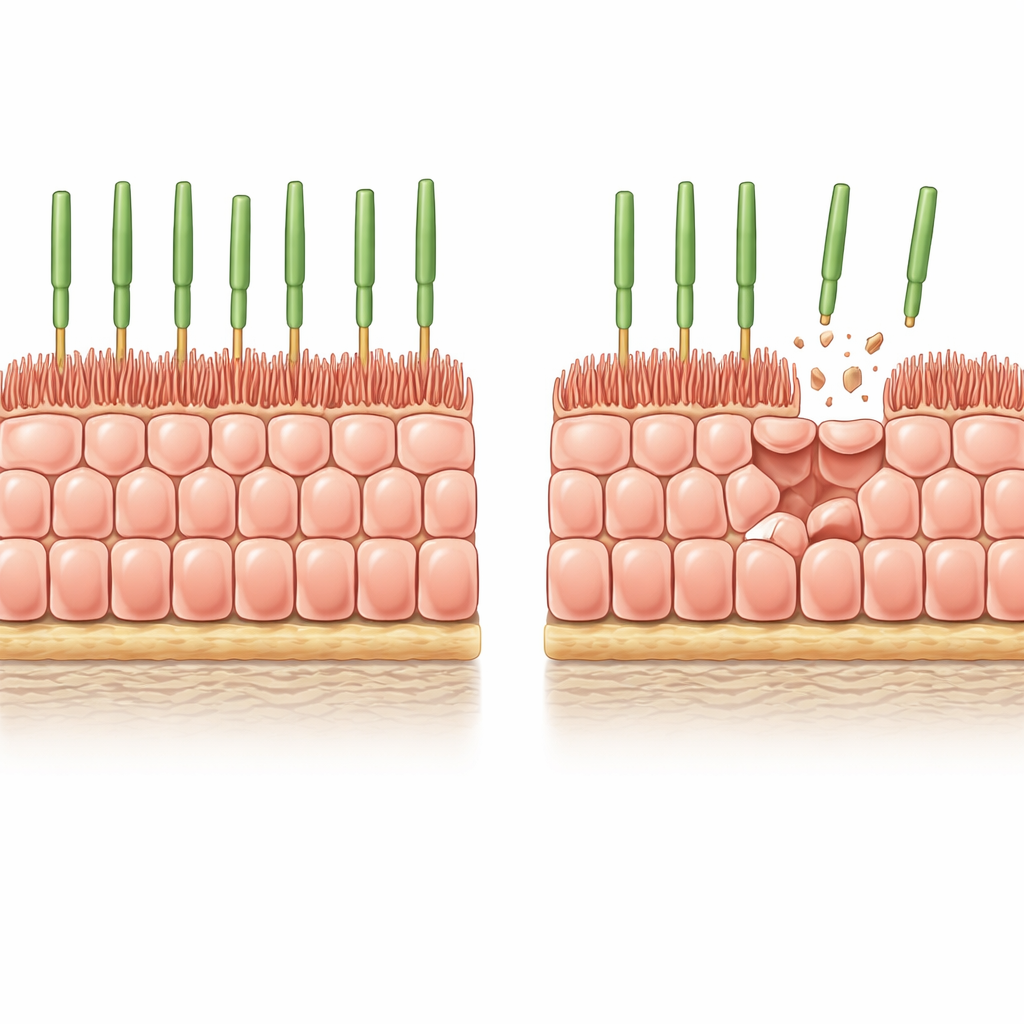
Precyzyjny model laboratoryjny starzejącej się tkanki oka
Naukowcy zaczęli od ludzkich komórek RPE pochodzących z komórek macierzystych, hodowanych jako jednorodna, ciasno upakowana warstwa na miękkim, biologicznie realistycznym żelu. W tych warunkach komórki przestają się dzielić, przyjmują klasyczny wzór plastra miodu charakterystyczny dla zdrowego RPE i rozwijają palczastą mikrokosmki na powierzchni wierzchołkowej, które współdziałają z fotoreceptorami. Aby odtworzyć stopniową utratę komórek zachodzącą w starzejącym się oku, zespół wprowadził do komórek kontrolowany „wyłącznik samobójczy”, a następnie wywołał szeroką, lecz częściową śmierć komórek. W ciągu kilku dni zniknęło około 8% komórek, a ocalałe musiały się rozciągnąć, by przykryć luki bez wsparcia z nowej proliferacji.
Jak warstwa komórek przekształca się po utracie
Po wywołanym przerzedzeniu pozostałe komórki RPE stały się szersze, ale zauważalnie niższe, zachowując objętość i rozciągając się bocznie, by zamknąć ubytki w tkance. Ich wierzchołkowe mikrokosmki zmniejszyły się i uległy dezorganizacji, a niektóre komórki rozwinęły grube włókna aktynowe przebiegające przez ich powierzchnię — cechy również obserwowane w starzejącym się ludzkim RPE. Pomiary potwierdziły redukcję kluczowych białek związanych z mikrokosmkami, takich jak ezryna i jej aktywna, ufosforylowana forma. Innymi słowy, prosta utrata sąsiadów wystarczyła, by strukturalnie młode komórki przyjęły architekturę bardzo podobną do tej widocznej w starym RPE oka.
Gdy sztywność odbywa się kosztem zdolności oczyszczania
Struktura tej tkanki to nie tylko wygląd — warunkuje ona funkcję. Komórki RPE muszą codziennie pochłaniać i trawić niezliczone fragmenty z zewnętrznych segmentów fotoreceptorów. Używając fluorescencyjnie znakowanych fragmentów z wieprzowych siatkówek, zespół zmierzył tę aktywność oczyszczania. Przerzedzone arkusze RPE internalizowały ogólnie mniej fragmentów, lecz te, które zostały pochłonięte, miały tendencję do bycia większymi. Obrazowanie o wysokiej rozdzielczości wyjaśniło przyczynę: w zdrowych arkuszach powierzchnia apikalna wypuklała się, tworząc dobrze zdefiniowane „kielichy” otaczające każdy fragment, podparte przez dynamiczne przestawienia aktyny i miozyny. W przerzedzonych arkuszach powierzchnia wyglądała gładsza i mniej odkształcalna, z mniejszą liczbą wyraźnych kształtów kielichów i pojawieniem się dużych wypustek bogatych w aktynę, które wydawały się nie pomagać w pochłanianiu cząstek.
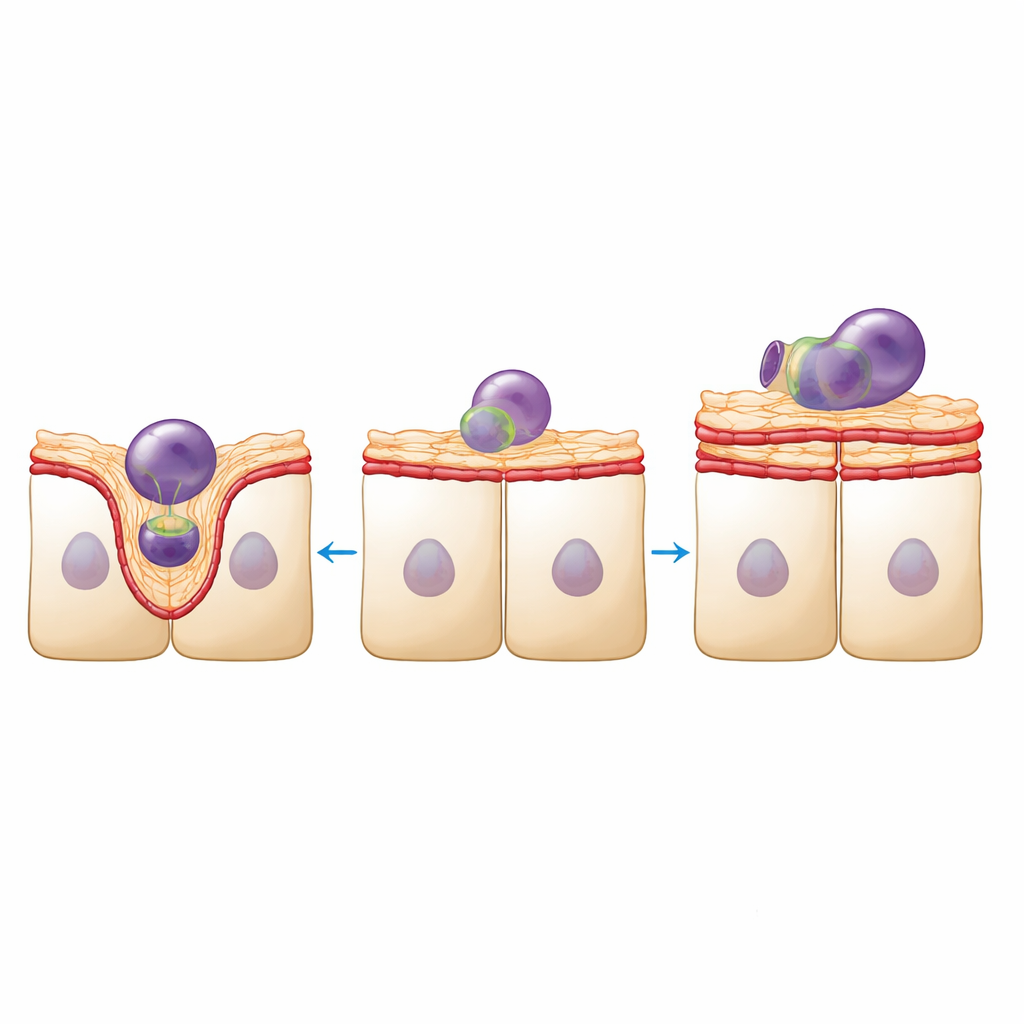
Mechaniczna homeostaza przesuwa się w stronę sztywności
Aby powiązać te zmiany wizualne z mechaniką, autorzy zbadali właściwości fizyczne tkanki na dwóch skalach. Nanoindentacja, która wciska drobny kulisty końcówkę w powierzchnię apikalną, wykazała, że przerzedzone RPE stało się w przybliżeniu o jedną trzecią sztywniejsze i bardziej sprężyste jako arkusz wielokomórkowy. Jednocześnie molekularne markery kurczliwości i siły połączeń — ufosforylowana lekkalancuchowa miozyny oraz białko adhezyjne winkulina — były wzbogacone wzdłuż brzegów międzykomórkowych. Jednak mikroskopia Brillouina, metoda oparta na świetle wykrywająca lokalną sztywność i zawartość wody w komórkach, pokazała, że sama korowa powierzchnia apikalna stała się mechanicznie odmienna i w pewnych aspektach miększa. Razem wyniki te sugerują, że monowarstwa wzmacnia swoje boczne połączenia, by utrzymać integralność arkusza, podczas gdy powierzchnia apikalna traci subtelną mikrostrukturę, która normalnie pozwala jej zginać się i formować kielichy wokół cząstek.
Regulatory aktyny kierują równowagą między wytrzymałością a elastycznością
Analiza ekspresji genów wskazała na szerokie przestawienie układu aktynowego w przerzedzonym RPE. Białka promujące rozgałęzione sieci aktynowe i ich sieciowanie były nadeksprymowane, podczas gdy kilka formin, sprzyjających długim, liniowym filamentom, oraz ezryna były zredukowane. Zespół następnie farmakologicznie modulował te systemy. Hamowanie formin w normalnym RPE usztywniło arkusz i spowodowało, że pochłaniane fragmenty były większe, częściowo naśladując stan przypominający starzenie. W przerzedzonym RPE blokada kompleksu Arp2/3, kluczowego nukleatora rozgałęzionej aktyny, zwiększyła liczbę internalizowanych fragmentów i przywróciła wyraźniejsze wypuklenia powierzchni apikalnej. Te interwencje pokazują, że modulacja nukleacji aktyny może przesuwać tkankę między bardziej sztywną, ochronną konfiguracją a bardziej odkształcalną, sprzyjającą fagocytozie.
Co to oznacza dla starzejących się oczu
Podsumowując, praca pokazuje, że nawet umiarkowana utrata komórek sama w sobie może przesunąć tkankę RPE w nowe mechaniczne równowagowe ustawienie: arkusz staje się mocniej zszyty i sztywniejszy jako całość, podczas gdy jego górna powierzchnia traci plastyczność niezbędną do efektywnego pochłaniania odpadów z fotoreceptorów. W efekcie komórki priorytetowo traktują utrzymanie ciągłości tkanki kosztem wykonywania swojej wyspecjalizowanej funkcji oczyszczania. Ten strukturalny kompromis, napędzany zmianami w cytoszkielecie aktynowym i napięciu połączeń, a nie klasycznymi biochemicznymi uszkodzeniami związanymi ze starzeniem, może pomóc wyjaśnić, dlaczego stare RPE często wygląda nienaruszone, lecz działa słabiej. Zrozumienie i potencjalne korygowanie tej równowagi między stabilnością a elastycznością może otworzyć nowe drogi do zachowania wzroku w schorzeniach takich jak zwyrodnienie plamki związane z wiekiem.
Cytowanie: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Słowa kluczowe: barwnikowy nabłonek siatkówki, mechanika komórek, zwyrodnienie plamki związane z wiekiem, cytoszkielet aktynowy, fagocytoza