Clear Sky Science · de
Verlust von Zellen stört die mechanische Homöostase und treibt ein gealtertes Phänotyp des retinalen Pigmentepithels (RPE) in vitro voran
Warum alternde Zellen im Auge Schwierigkeiten haben, das Sehvermögen klar zu halten
Mit zunehmendem Alter entwickeln viele Menschen Probleme mit dem zentralen Sehen, oft verbunden mit Schäden in einer dünnen Zellschicht auf der Rückseite des Auges, dem retinalen Pigmentepithel (RPE). Diese Zellen arbeiten täglich still im Hintergrund, um die darüber liegenden lichtempfindlichen Photorezeptoren zu unterstützen. Allerdings war schwer zu klären, wie allein der altersbedingte Verlust von Zellen ihren physikalischen Zustand verändert und ihre Funktion beeinträchtigt. Diese Studie stellt ein dem Altern ähnliches Szenario im Labor nach und zeigt, dass bereits der Verlust einer vergleichsweise geringen Anzahl von RPE‑Zellen das verbleibende Gewebe mechanisch „umverdrahten“ kann: es wird steifer, weniger flexibel und schlechter in seiner Kernaufgabe, die visuelle Abfallentsorgung.
Ein sorgfältiges Labor‑Modell gealterten Augengewebes
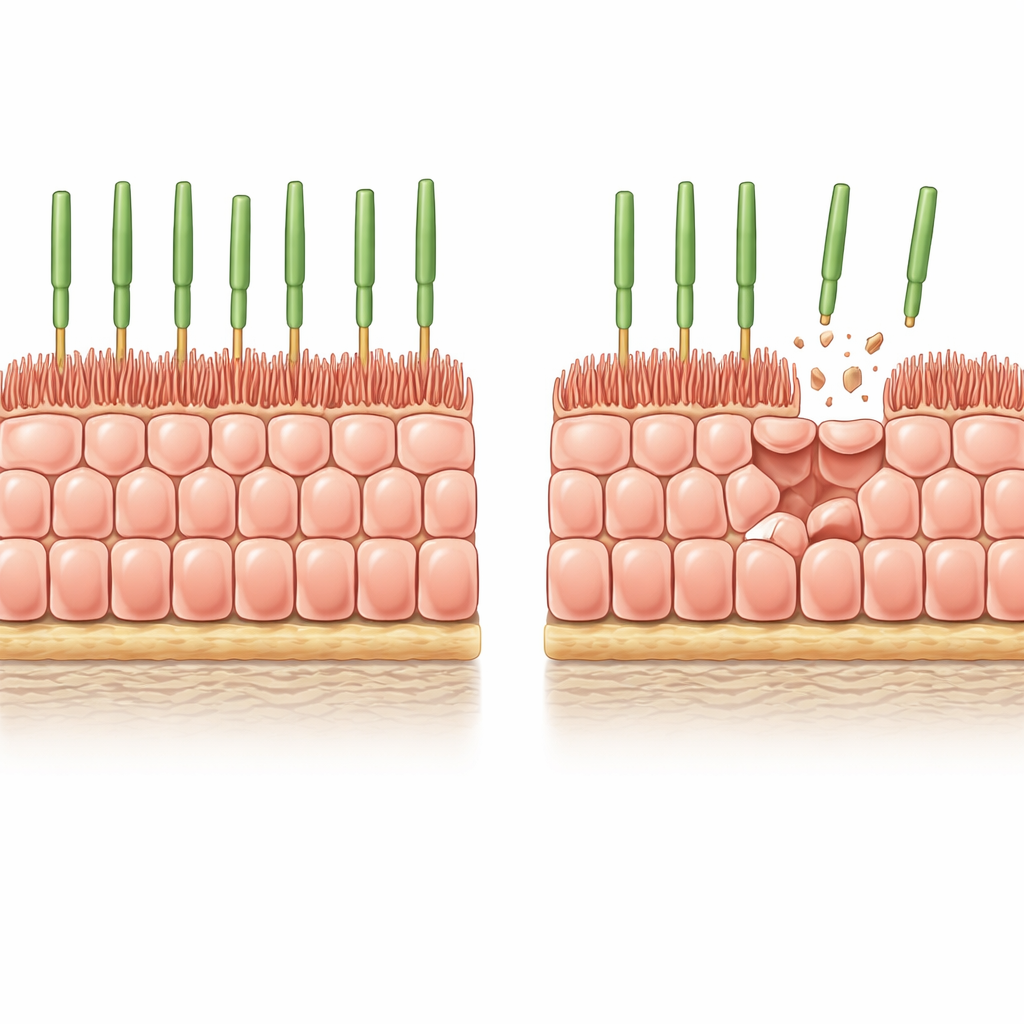
Die Forschenden begannen mit aus menschlichen Stammzellen gewonnenem RPE, das als einheitliches, dicht gepacktes Monolayer auf einem weichen, biologisch realistischen Gel kultiviert wurde. Unter diesen Bedingungen hören die Zellen auf zu teilen, nehmen das klassische sechseckige Muster gesunder RPE an und entwickeln fingerartige Mikrovilli auf ihrer apikalen Oberfläche, die mit Photorezeptoren interagieren. Um den allmählichen Zelltod nachzuahmen, der im alternden Auge auftritt, führte das Team einen kontrollierbaren „Suizid“-Schalter in die Zellen ein und löste dann weit verbreiteten, aber teilweisen Zelltod aus. Innerhalb weniger Tage verschwanden etwa 8 % der Zellen, und die Überlebenden mussten sich ohne neue Zellteilung dehnen, um die Lücken zu schließen.
Wie sich die Zellschicht nach Verlust neu formt
Nach dieser induzierten Ausdünnung wurden die verbleibenden RPE‑Zellen breiter, aber deutlich kürzer, wobei ihr Volumen erhalten blieb und sie sich seitlich ausbreiteten, um das Gewebe zu verschließen. Ihre apikalen Mikrovilli schrumpften und wurden unordentlicher, und einige Zellen entwickelten dicke Aktin‑Stressfasern, die quer über sie verliefen – Merkmale, die ebenfalls in gealtertem menschlichem RPE beobachtet werden. Messungen bestätigten, dass wichtige Mikrovilli‑assoziierte Proteine, wie Ezrin und seine aktive phosphorylierte Form, reduziert waren. Mit anderen Worten war der einfache Verlust von Nachbarzellen ausreichend, um strukturell junge Zellen in eine Architektur zu drängen, die stark der alten RPE im Auge ähnelt.
Wenn Steifigkeit gegen Reinigungsfähigkeit eingetauscht wird
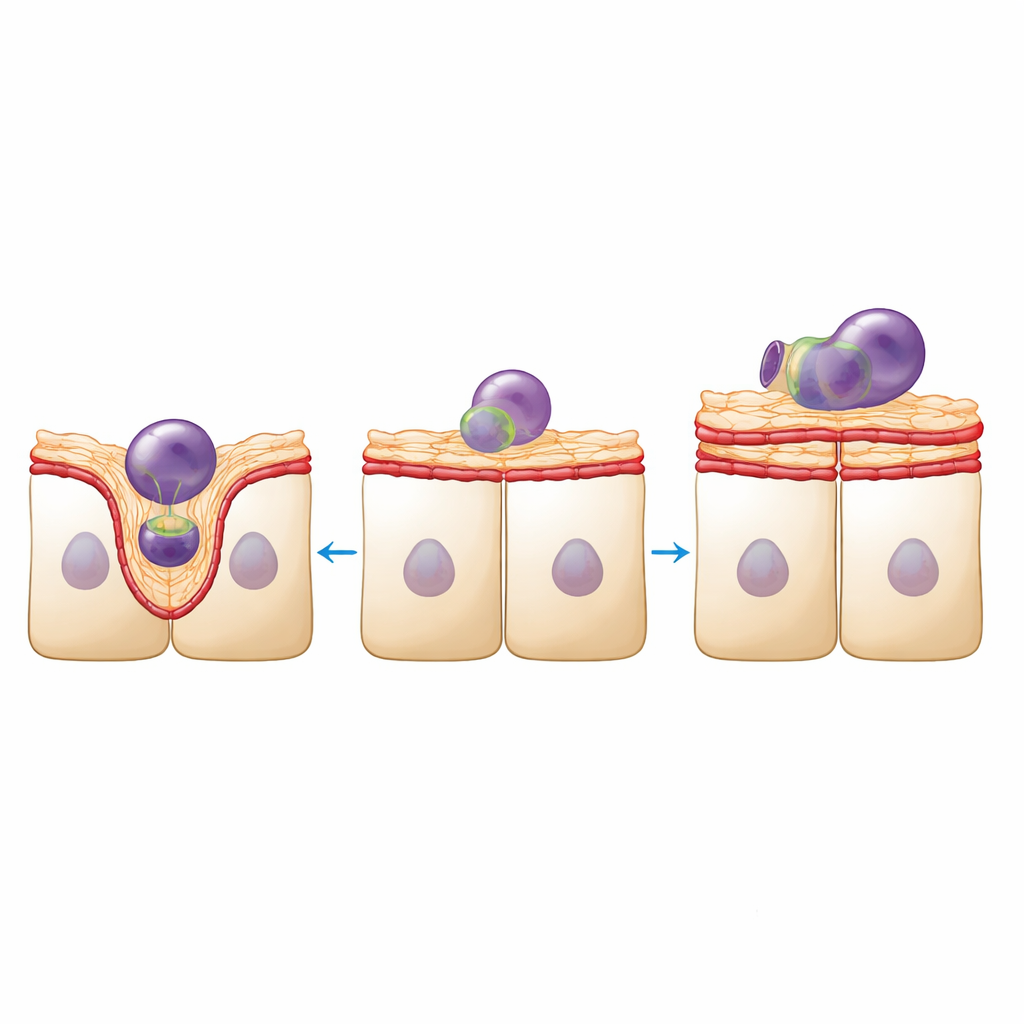
Die Struktur dieses Gewebes betrifft nicht nur das Erscheinungsbild; sie ist grundlegend für die Funktion. RPE‑Zellen müssen täglich unzählige Fragmente der äußeren Segmente der Photorezeptoren aufnehmen und verdauen. Mittels fluoreszenzmarkierter Fragmente aus Schweine‑Retinas maß das Team diese Reinigungsaktivität. Dichtereduzierte RPE‑Schichten internalisierten insgesamt weniger Fragmente, doch die aufgenommenen Fragmente waren tendenziell größer. Hochauflösende Aufnahmen zeigten den Grund: In gesunden Schichten wölbte sich die apikale Oberfläche nach oben und bildete gut definierte Tassen um jedes Fragment, gestützt durch dynamische Umorganisationen von Aktin und Myosin. In dichtereduzierten Schichten wirkte die Oberfläche glatter und weniger verformbar, mit weniger klaren Tassenformen und dem Auftreten großer, aktinreicher Vorwölbungen, die offenbar nicht zur Aufnahme der Partikel beitrugen.
Mechanische Homöostase verschiebt sich in Richtung Steifheit
Um diese sichtbaren Veränderungen mit mechanischen Eigenschaften zu verknüpfen, untersuchten die Autor:innen die physikalischen Eigenschaften des Gewebes auf zwei Skalen. Nanoindentation, bei der eine winzige kugelförmige Spitze in die apikale Oberfläche gedrückt wird, zeigte, dass das dichtereduzierte RPE als mehrzelluläres Blatt etwa um ein Drittel steifer und elastischer wurde. Gleichzeitig waren molekulare Marker für Kontraktilität und Verbindungsstärke – phosphoryliertes Myosin‑Light‑Chain und das Adhäsionsprotein Vinculin – entlang der Zell‑Zell‑Grenzen angereichert. Brillouin‑Mikroskopie, eine lichtbasierte Methode, die lokale Steifigkeit und Wassergehalt innerhalb der Zellen erfasst, zeigte jedoch, dass die apikale Kortikalis mechanisch differenziert und in mancher Hinsicht weicher wurde. Zusammengenommen deuten diese Befunde darauf hin, dass das Monolayer seine lateralen Verbindungen verstärkt, um das Blatt zusammenzuhalten, während die apikale Oberfläche die fein abgestimmte Mikrostruktur verliert, die ihr normalerweise erlaubt, sich zu biegen und Tassen um Partikel zu bilden.
Aktinregulatoren steuern das Gleichgewicht zwischen Stärke und Flexibilität
Genexpressionsanalysen wiesen auf eine umfassende Umverdrahtung der Aktin‑Maschinerie im dichtereduzierten RPE hin. Proteine, die verzweigte Aktinnetzwerke und Verknüpfungen fördern, waren hochreguliert, während mehrere Formine, die lange, lineare Filamente begünstigen, sowie Ezrin herunterreguliert waren. Das Team manipulierte diese Systeme pharmakologisch. Die Hemmung von Forminen in normalem RPE verhärtete das Blatt und vergrößerte die aufgenommenen Fragmente, was den alterungsähnlichen Zustand teilweise nachahmte. In dichtereduzierten RPE erhöhte die Blockade des Arp2/3‑Komplexes, eines wichtigen Auslösers verzweigter Aktinbildung, die Anzahl internalisierter Fragmente und stellte ausgeprägtere Aufwölbungen der apikalen Oberfläche wieder her. Diese Eingriffe zeigen, dass das Einstellen der Aktin‑Nukleation das Gewebe zwischen einer starreren, schützenden Konfiguration und einer verformbareren, phagozytosefreundlichen Lage hin und her verschieben kann.
Was das für alternde Augen bedeutet
In der Summe zeigt die Arbeit, dass bereits ein moderater Zellverlust das RPE‑Gewebe in ein neues mechanisches Gleichgewicht drängen kann: Das Blatt wird stärker zusammengefügt und insgesamt steifer, während seine obere Oberfläche die Plastizität verliert, die nötig ist, um Photorezeptor‑Trümmer effizient zu umschließen. Effektiv priorisieren die Zellen das Zusammenhalten des Gewebes gegenüber ihrer spezialisierten Reinigungsaufgabe. Dieser strukturelle Zielkonflikt, angetrieben durch Veränderungen im Aktin‑Zytoskelett und in der junctionalen Spannung statt durch klassische biochemische Alterungsschäden, könnte erklären, warum gealtertes RPE oft intakt aussieht, aber schlecht funktioniert. Das Verständnis und möglicherweise das gezielte Einstellen dieses Gleichgewichts zwischen Stabilität und Flexibilität könnten neue Wege eröffnen, das Sehvermögen bei Erkrankungen wie der altersbedingten Makuladegeneration zu erhalten.
Zitation: Piskova, T., Kozyrina, A.N., Astrauskaitė, G. et al. Cell loss disrupts mechanical homeostasis to drive retinal pigment epithelium ageing-like phenotype in vitro. Nat Commun 17, 3404 (2026). https://doi.org/10.1038/s41467-026-71493-x
Schlüsselwörter: retinales Pigmentepithel, Zellmechanik, altersbedingte Makuladegeneration, Aktin-Zytoskelett, Phagozytose