Clear Sky Science · zh
定量活体成像揭示 PRICKLE1 在不依赖平面细胞极性下控制连接区神经管形态发生
早期神经形成如何塑造我们的脑与脊髓
在人人胚还不到一粒米大小之前,一片扁平的细胞层必须折叠并封闭成一个空心管,这将发育成脑与脊髓。当这一过程出错时,婴儿可能出生时出现严重的脊柱缺陷。本研究在微小的鹌鹑胚胎中使用先进的活体成像实时观察这一转变,揭示了一种令人惊讶的细胞行为和一个关键控制蛋白,它们共同有助于防止一类特定的脊柱问题。
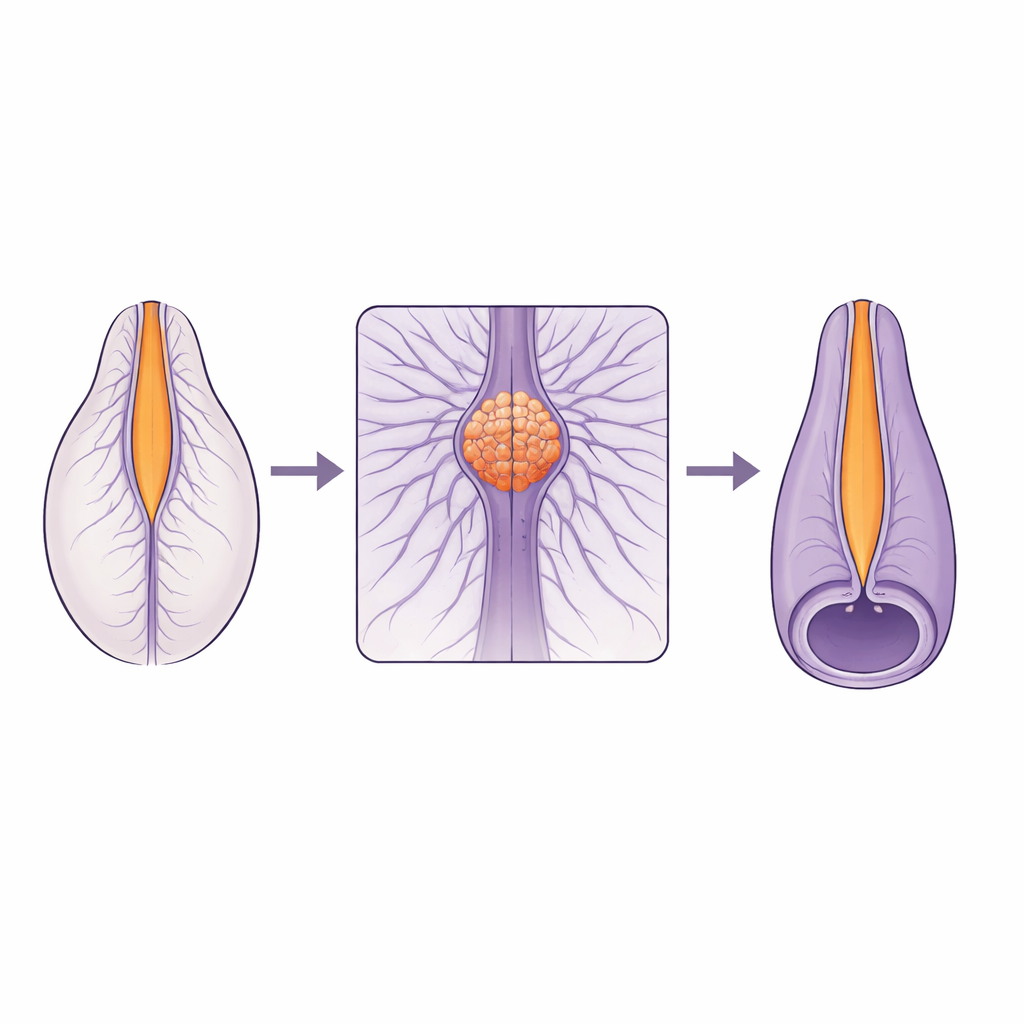
生长中脊柱的一个脆弱连接
脊髓在其纵向并非以单一方式形成。上部通过扁平组织的折叠和闭合形成,而下部则由从内部空化的实心细胞棒形成。这两种构建程序必须在一个称为连接区的小区域平滑地会合并融合。许多人类脊柱缺陷集中出现在该连接附近,表明此处尤其脆弱。然而直到现在,科学家们还缺乏对这一区域在管道闭合过程中细胞如何移动和形变的高分辨率活体观察。
观察细胞如何移动并潜入表面之下
研究者使用了转基因鹌鹑胚,其细胞在显微镜下会发光,使他们能够在数小时内追踪数百个单个细胞。他们发现连接区神经管是通过两种协调的运动形成的。首先,来自两侧的细胞向中线爬行,这种称为中外向会聚(mediolateral convergence)的运动使组织变窄。其次,位于中线处的一条细胞带表现出更戏剧性的行为:这些细胞收缩其顶端(胞顶)表面,然后下沉进入更深的组织,这种行为称为内陷(ingression)。这种内陷类似于上皮-间质转化(EMT),其中有序的片状细胞变得更能自由移动,但在这里发生于仍保留神经身份并主要贡献于脊髓而非其他组织的细胞中。
已知极性蛋白的一个意外角色
早期研究已将一种名为 PRICKLE1 的蛋白与该连接区联系起来。PRICKLE1 通常被认为是平面细胞极性(PCP)系统的一部分,该系统负责细胞的侧向定向并帮助组织伸长。人们本可能预期去除 PRICKLE1 会扰乱这种极性。然而,当团队在连接区特异性降低 PRICKLE1 水平时,通常的极性模式和引导会聚的长肌动蛋白纤维仍大体保持不变。改变的是中央细胞的行为:它们未能收缩胞顶表面,无法正常内陷,神经管后端开口未闭合,导致胚胎出现连接区神经管缺陷。
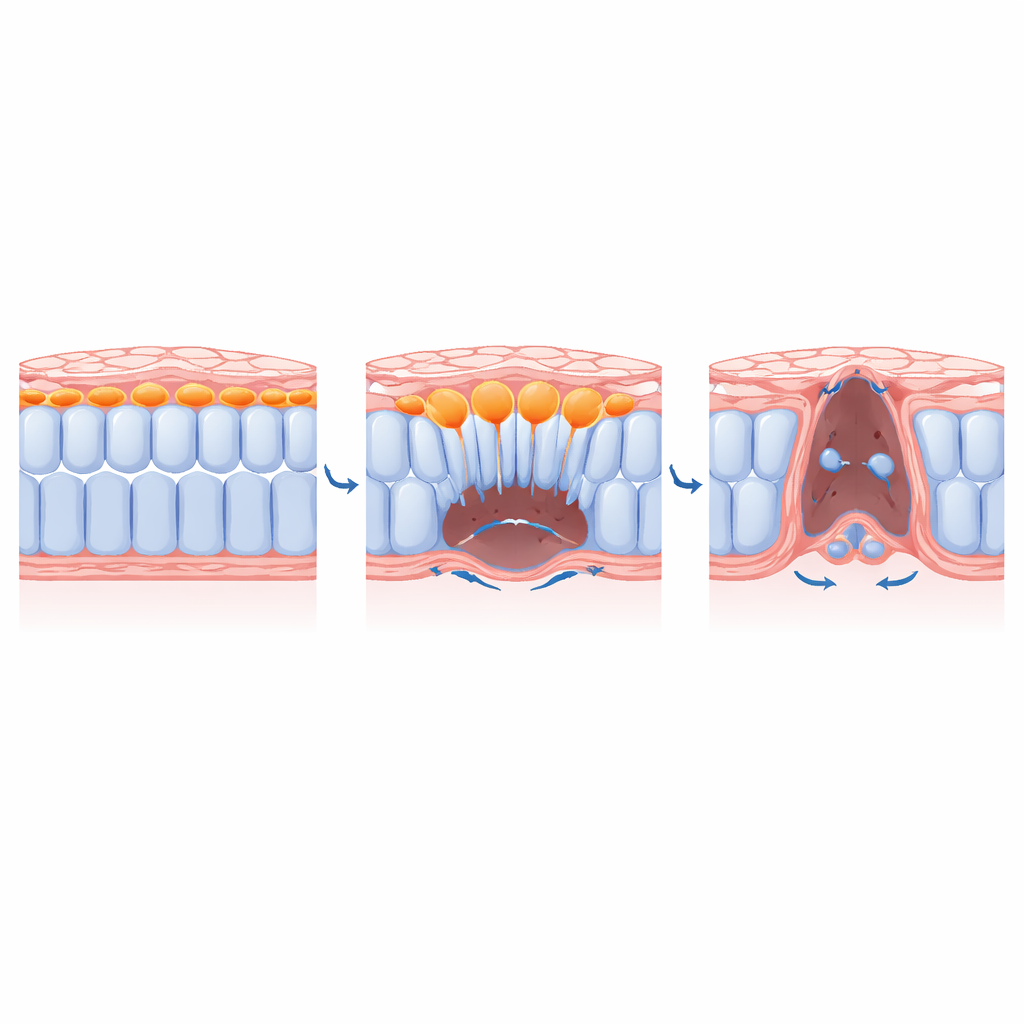
中央细胞如何为邻居腾出空间
通过结合遗传工具、药物,甚至光激活的肌球蛋白抑制剂,研究团队解析了内陷的控制机制。他们显示,诸如转录因子 SLUG 等关键 EMT 调控因子以及来自成纤维细胞生长因子的信号,都是使中央细胞采取伸出性、迁移性形态并降解其下方支持基质所必需的。阻断这些信号会将中央细胞困在背表面附近,阻止它们向腹侧移动。关键的是,当研究者仅在中央细胞中禁用收缩时,这些细胞不再内陷,侧方邻居也无法完全向中线会聚。换言之,中央细胞向内潜入的动作在物理上为剩余的细胞片拉链式闭合清出了空间。
这对人类脊柱缺陷意味着什么
这项工作揭示了 PRICKLE1 在中央细胞顶端皮层具有一个独立于 PCP 的职能:它促进收缩性肌动蛋白和肌球蛋白在胞顶的积累,从而实现胞顶收缩和内陷。缺乏该功能时,即便侧向极性线索仍然存在,中央类似 EMT 的过程也会停滞,神经管在连接处无法闭合。由于人类 PRICKLE1 的突变最常与局灶性脊柱闭合不全——连接区神经管缺陷——相关联,这些发现提供了一个具体的细胞学解释。对非专业读者而言,核心结论是:一小群细胞必须在恰当的时间与位置一方面将其顶部拉紧、一方面潜入表面下,而蛋白 PRICKLE1 是这一动作的关键开关。当该开关失效时,上脊髓与下脊髓之间的连接无法正确形成,从而有助于解释这一特定且严重的先天缺陷类型。
引用: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
关键词: 神经管缺陷, PRICKLE1, 上皮-间质转化, 胚胎发育, 细胞迁移