Clear Sky Science · pl
Obrazowanie ilościowe na żywo ujawnia, że PRICKLE1 kontroluje morfogenezę złącza cewy nerwowej niezależnie od planarnej polarności komórkowej
Jak wczesne formowanie nerwów kształtuje mózg i rdzeń kręgowy
Zanim ludzki zarodek osiągnie rozmiar ziarnka ryżu, płaska warstwa komórek musi się zgiąć i zamknąć w rurę, która stanie się mózgiem i rdzeniem kręgowym. Gdy ten proces przebiega nieprawidłowo, noworodki mogą mieć poważne wady kręgosłupa. W tym badaniu zastosowano nowoczesne obrazowanie na żywo w małych embrionach przepiórki, aby obserwować tę transformację w czasie rzeczywistym, ujawniając zaskakujące zachowanie komórek i kluczowy białkowy regulator, które razem pomagają zapobiegać określonej klasie problemów kręgosłupa.
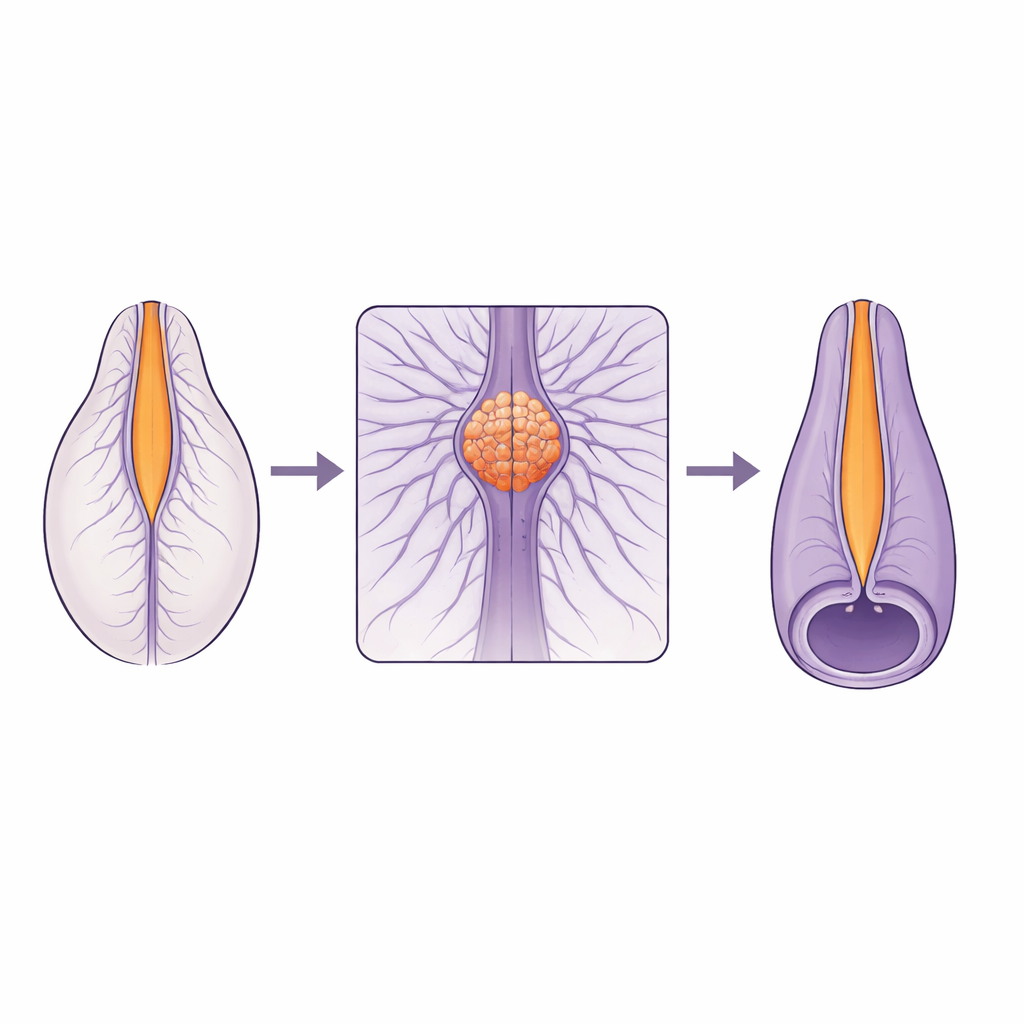
Delikatne złącze w rozwijającym się kręgosłupie
Cewka nerwowa nie powstaje w jeden sposób na całej swojej długości. Część górna tworzy się przez zginanie i zamykanie płaskiej tkanki, podczas gdy część dolna powstaje z litego pręta komórek, który od wewnątrz tworzy jamę. Te dwa programy budowy muszą spotkać się i płynnie połączyć w małym obszarze zwanym strefą złącza. Wiele ludzkich wad kręgosłupa skupia się w pobliżu tego złącza, co sugeruje, że jest ono szczególnie podatne na zaburzenia. Do tej pory jednak naukowcom brakowało żywych, wysokorozdzielczych obrazów pozwalających zrozumieć, jak komórki rzeczywiście przemieszczają się i zmieniają kształt w tej strefie podczas zamykania cewy.
Obserwacja ruchu komórek i ich zanurzania się pod powierzchnię
Naukowcy użyli transgenicznych embrionów przepiórki, których komórki świecą pod mikroskopem, co pozwoliło śledzić setki pojedynczych komórek przez wiele godzin. Stwierdzili, że złącze cewy nerwowej tworzy się przez dwa skoordynowane ruchy. Po pierwsze, komórki z boków wędrują w kierunku linii środkowej — ruch zwany zbieżnością śród‑boczną, który zwęża tkankę. Po drugie, pasmo komórek dokładnie na środku wykonuje coś bardziej dramatycznego: te komórki kurczą swoje powierzchnie szczytowe (apikalne), a następnie opadają pod powierzchnię do głębszych warstw — zachowanie znane jako ingresja. Ta ingresja przypomina przejście nabłonkowo‑mezenchymalne (EMT), w którym uporządkowane, płaskie komórki stają się bardziej ruchliwe, ale tutaj dzieje się to w komórkach, które zachowują tożsamość nerwową i później wnoszą głównie wkład do rdzenia kręgowego, a nie do innych tkanek.
Zaskakująca rola znanego białka polarności
Wcześniejsze prace wskazywały na udział białka PRICKLE1 w tej strefie złącza. PRICKLE1 jest zwykle znany jako element systemu planarnej polarności komórkowej (PCP), który ustawia komórki bocznie i pomaga tkankom wydłużać się. Można by się spodziewać, że usunięcie PRICKLE1 zakłóci tę polarność. Zamiast tego, gdy zespół obniżył poziom PRICKLE1 specyficznie w strefie złącza, typowe wzory polarności i długie pęczki aktyny prowadzące zbieżność pozostały w dużej mierze nienaruszone. Zmieniło się zachowanie komórek środkowych: nie potrafiły one skurczyć powierzchni apikalnych, nie przechodziły prawidłowo ingresji, a tylne ujście cewy nerwowej pozostało niezamknięte, powodując w embrionach wady złącza cewy nerwowej.
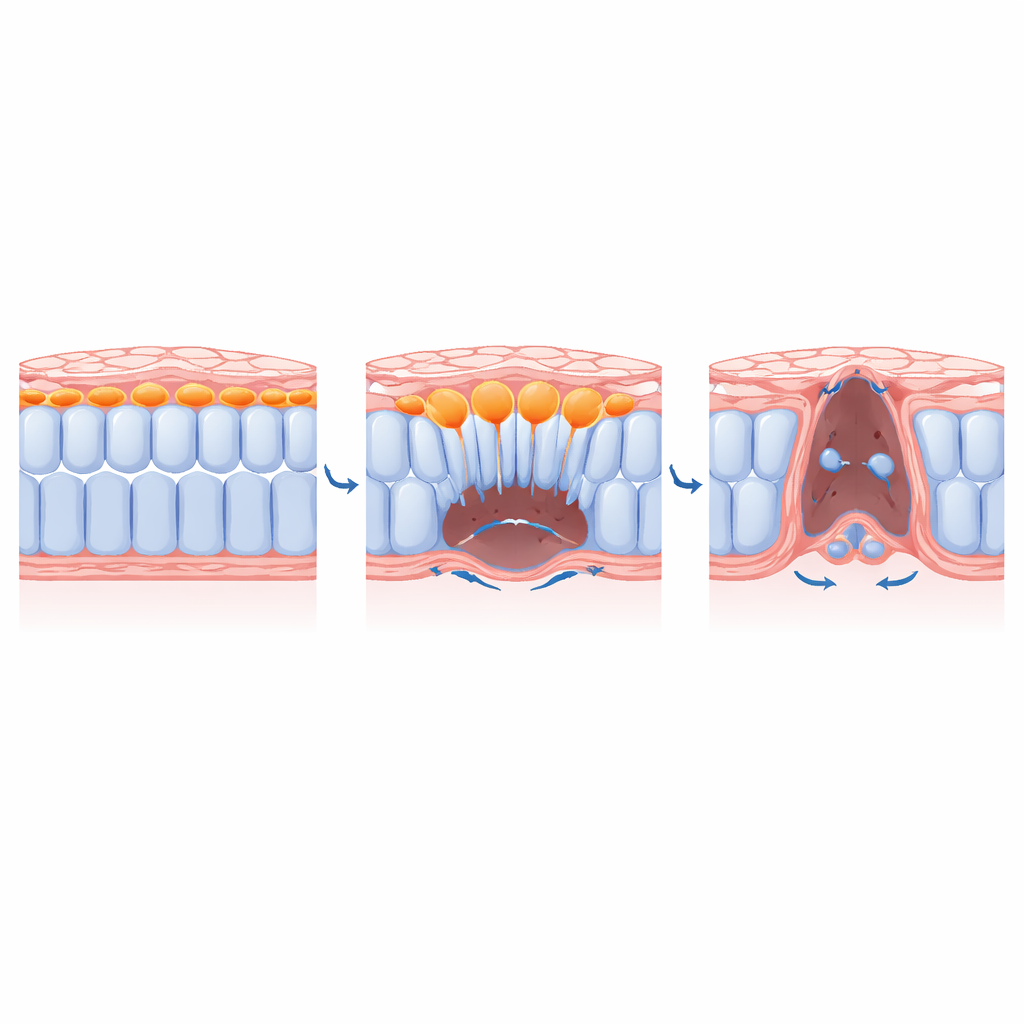
Jak komórki centralne robią miejsce dla sąsiadów
Łącząc narzędzia genetyczne, leki i nawet światłowrażliwe inhibitory miozyny (silnika napędzającego skurcz), zespół rozłożył mechanizm kontroli ingresji. Pokazali, że kluczowi regulatorzy EMT, tacy jak czynnik transkrypcyjny SLUG, oraz sygnały od czynników wzrostu fibroblastów są wymagane, by komórki środkowe przybrały wydłużony, protrazyjny kształt migracyjny i rozłożyły podporowy matrix pod sobą. Blokowanie tych sygnałów uwięziło komórki środkowe blisko powierzchni grzbietowej i uniemożliwiło im przesunięcie się brzusznie. Co kluczowe, gdy badacze wyłączyli skurcz tylko w komórkach środkowych, te komórki przestały ingressować, a sąsiedzi z boków nie mogli w pełni zbiec ku linii środkowej. Innymi słowy, akt zanurzania się komórek centralnych fizycznie oczyszcza przestrzeń, która pozwala pozostałej warstwie zapiąć się jak zamek błyskawiczny.
Dlaczego to ma znaczenie dla ludzkich wad kręgosłupa
Praca ujawnia, że PRICKLE1 pełni niezależną od PCP funkcję w korze apikalnej komórek środkowych: wspiera gromadzenie kurczliwej aktyny i miozyny niezbędnej do apikalnego zwężenia i ingresji. Bez tej funkcji, mimo że boczne sygnały polarności utrzymują się, środkowy proces podobny do EMT zamarza, a cewka nerwowa nie zamyka się w strefie złącza. Ponieważ u ludzi mutacje w PRICKLE1 najczęściej wiążą się z lokalnymi dysrafiami kręgosłupa — wadami złącza cewy nerwowej — te odkrycia dostarczają konkretnego wyjaśnienia na poziomie komórkowym. Dla czytelnika popularnonaukowego kluczowa wiadomość jest taka, że niewielka grupa komórek musi jednocześnie mocno pociągnąć swoje wierzchołki i zanurzyć się pod powierzchnię we właściwym miejscu i czasie, a białko PRICKLE1 jest krytycznym przełącznikiem tego ruchu. Gdy ten przełącznik zawodzi, połączenie między górną a dolną częścią rdzenia kręgowego nie może się prawidłowo utworzyć, co pomaga wyjaśnić konkretną i poważną klasę wad wrodzonych.
Cytowanie: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Słowa kluczowe: wady cewy nerwowej, PRICKLE1, przejście nabłonkowo‑mezenchymalne, rozwój embrionalny, migracja komórek