Clear Sky Science · fr
Imagerie quantitative en direct révèle que PRICKLE1 contrôle la morphogenèse jonctionnelle du tube neural indépendamment de la polarité planaire cellulaire
Comment la formation précoce du système nerveux façonne notre cerveau et notre moelle épinière
Avant même qu'un embryon humain n'atteigne la taille d'un grain de riz, une couche plane de cellules doit se plier et se sceller en un tube creux qui deviendra le cerveau et la moelle épinière. Lorsque ce processus dysfonctionne, des nouveau‑nés peuvent présenter de graves malformations de la colonne. Cette étude utilise l'imagerie en direct de pointe sur de petits embryons de caille pour observer cette transformation en temps réel, révélant un comportement cellulaire surprenant et une protéine clé de contrôle qui, ensemble, contribuent à prévenir une classe spécifique de problèmes spinaux.
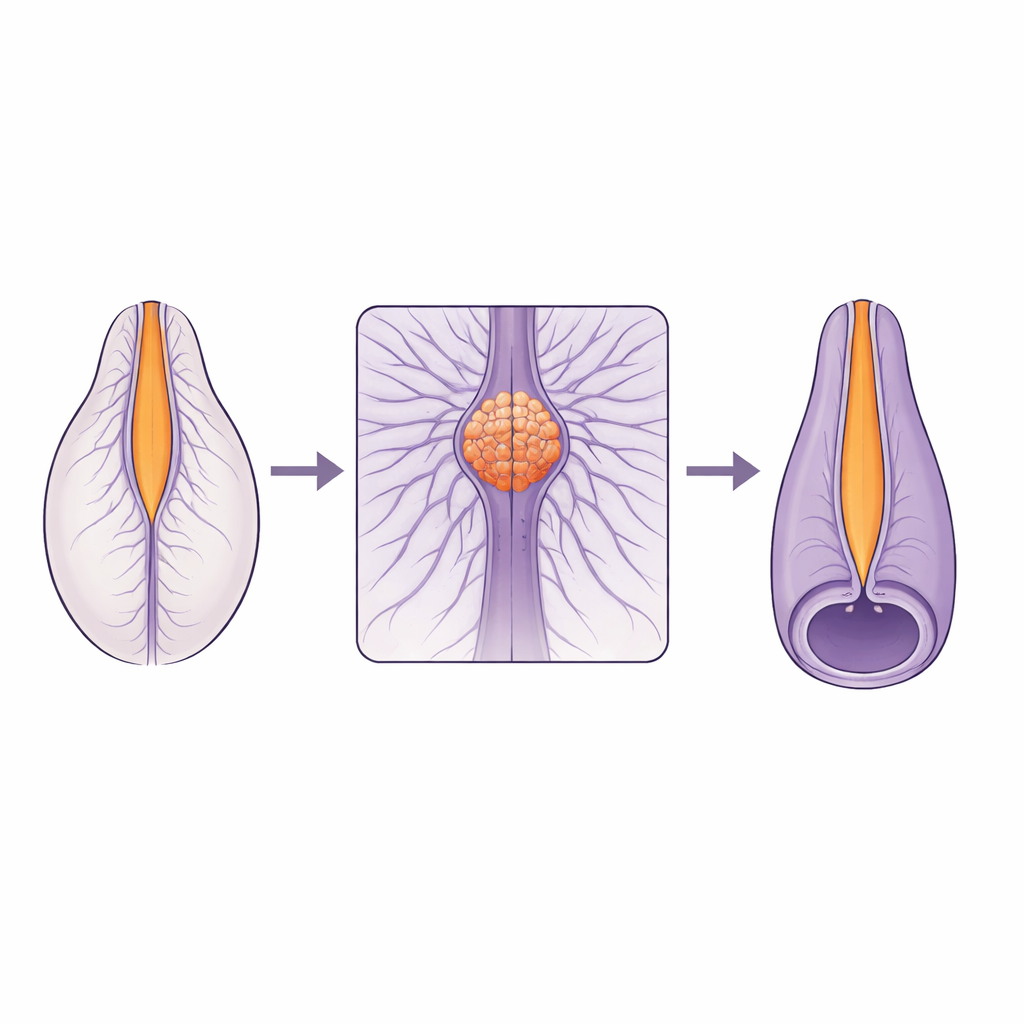
Une jonction délicate dans la colonne en formation
La moelle épinière ne se forme pas de la même manière le long de son axe. La partie supérieure naît par le repliement et la fermeture d'un tissu plat, tandis que la partie inférieure se forme à partir d'une tige solide de cellules qui se cavite de l'intérieur. Ces deux programmes de construction doivent se rencontrer et se fusionner de façon fluide dans une petite zone appelée zone jonctionnelle. De nombreuses malformations humaines de la colonne se concentrent près de cette jonction, ce qui suggère qu'elle est particulièrement vulnérable. Jusqu'à présent, les scientifiques ne disposaient pas des vues en direct à haute résolution nécessaires pour comprendre comment les cellules se déplacent et changent de forme dans cette zone pendant la fermeture du tube.
Observer les cellules se déplacer et plonger sous la surface
Les chercheurs ont utilisé des embryons de caille transgéniques dont les cellules brillent au microscope, ce qui leur a permis de suivre des centaines de cellules individuelles pendant des heures. Ils ont constaté que le tube neural jonctionnel se forme par deux mouvements coordonnés. D'abord, des cellules latérales rampent vers la ligne médiane, un mouvement appelé convergence médio‑latérale qui rétrécit le tissu. Ensuite, une bande de cellules située au centre effectue quelque chose de plus spectaculaire : ces cellules rétrécissent leur surface apicale, puis plongent sous la surface vers les tissus profonds, un comportement connu sous le terme d'ingression. Cette ingression ressemble à une transition épithélio‑mésenchymateuse, où des cellules en feuille ordonnée deviennent plus mobiles, mais ici cela se produit chez des cellules qui conservent une identité neuronale et contribueront principalement à la moelle épinière plutôt qu'à d'autres tissus.
Un rôle surprenant pour une protéine de polarité bien connue
Des travaux antérieurs avaient impliqué une protéine appelée PRICKLE1 dans cette région jonctionnelle. PRICKLE1 est habituellement connue comme faisant partie du système de polarité cellulaire planaire, qui oriente les cellules latéralement et aide les tissus à s'allonger. On pourrait s'attendre à ce que la suppression de PRICKLE1 désorganise cette polarité. Au lieu de cela, lorsque l'équipe a réduit les niveaux de PRICKLE1 spécifiquement dans la zone jonctionnelle, les schémas habituels de polarité et les longs câbles d'actine qui guident la convergence restaient en grande partie intacts. Ce qui a changé, c'est le comportement des cellules médiales : elles n'ont pas réussi à contraindre leurs surfaces apicales, n'ont pas ingressé correctement, et l'orifice postérieur du tube neural est resté ouvert, produisant des défauts jonctionnels du tube neural chez les embryons.
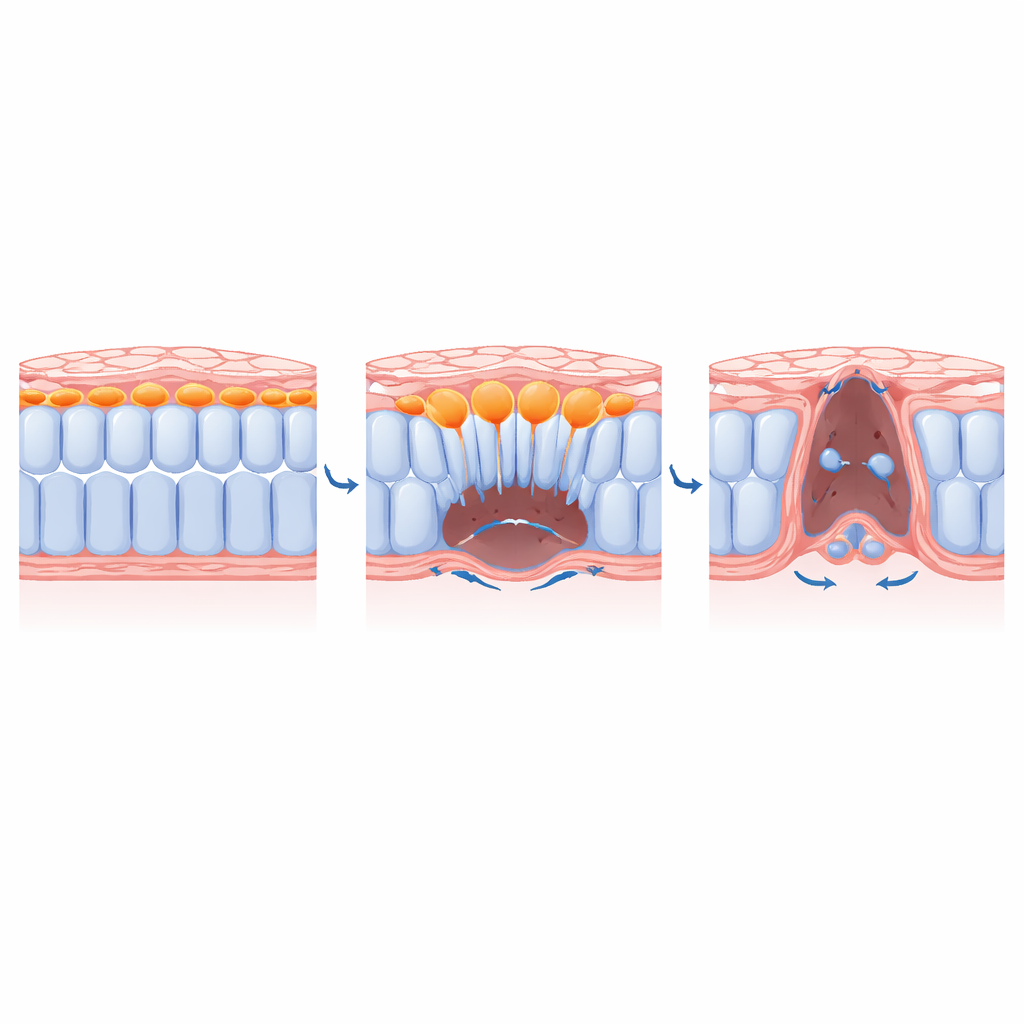
Comment les cellules centrales font de la place pour leurs voisines
En combinant outils génétiques, médicaments et même inhibiteurs de la myosine activés par la lumière, l'équipe a disséqué le contrôle de l'ingression. Ils ont montré que des régulateurs clés de l'EMT tels que le facteur de transcription SLUG et les signaux des facteurs de croissance des fibroblastes sont nécessaires pour que les cellules médiales adoptent une forme protractile et migratoire et dégradent la matrice de soutien en dessous. Le blocage de ces signaux a piégé les cellules médiales près de la surface dorsale et les a empêchées de se déplacer ventralement. De manière cruciale, lorsque les chercheurs ont désactivé la contraction uniquement dans les cellules médiales, ces cellules n'ingressaient plus, et les voisines latérales ne pouvaient pas converger complètement vers la ligne médiane. Autrement dit, l'acte des cellules centrales plongeant vers l'intérieur dégage physiquement l'espace qui permet à la feuille restante de se zipper.
Pourquoi cela importe pour les malformations humaines de la colonne
Ce travail révèle que PRICKLE1 a une fonction indépendante de la PCP à la corticale apicale des cellules médiales : elle favorise l'accumulation d'actine contractile et de myosine nécessaire à la constriction apicale et à l'ingression. Sans cette fonction, même si les indices de polarité latérale persistent, le processus central de type EMT s'arrête et le tube neural ne se ferme pas à la jonction. Parce que les mutations humaines de PRICKLE1 sont le plus souvent associées à des dysraphies spinales localisées — des défauts jonctionnels du tube neural — ces résultats offrent une explication cellulaire concrète. Pour un lecteur non spécialisé, le message essentiel est qu'un minuscule groupe de cellules doit à la fois serrer leur sommet et plonger sous la surface au bon endroit et au bon moment, et que la protéine PRICKLE1 est un commutateur critique pour ce mouvement. Lorsque ce commutateur fait défaut, la jonction entre la partie supérieure et la partie inférieure de la moelle ne peut pas se former correctement, ce qui aide à expliquer une classe spécifique et grave de malformations congénitales.
Citation: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Mots-clés: malformations du tube neural, PRICKLE1, transition épithélio‑mésenchymateuse, développement embryonnaire, migration cellulaire