Clear Sky Science · pt
Imagem ao vivo quantitativa revela que PRICKLE1 controla a morfogênese do tubo neural na zona de junção independentemente da polaridade planar celular
Como a formação inicial do sistema nervoso molda nossos cérebros e medulas
Antes que um embrião humano tenha o tamanho de um grão de arroz, uma folha plana de células precisa dobrar e selar-se em um tubo oco que dará origem ao cérebro e à medula espinhal. Quando esse processo falha, bebês podem nascer com defeitos espinhais graves. Este estudo usa imageamento ao vivo de ponta em embriões de codorna minúsculos para observar essa transformação em tempo real, revelando um comportamento celular surpreendente e uma proteína reguladora chave que juntos ajudam a evitar uma classe específica de problemas espinhais.
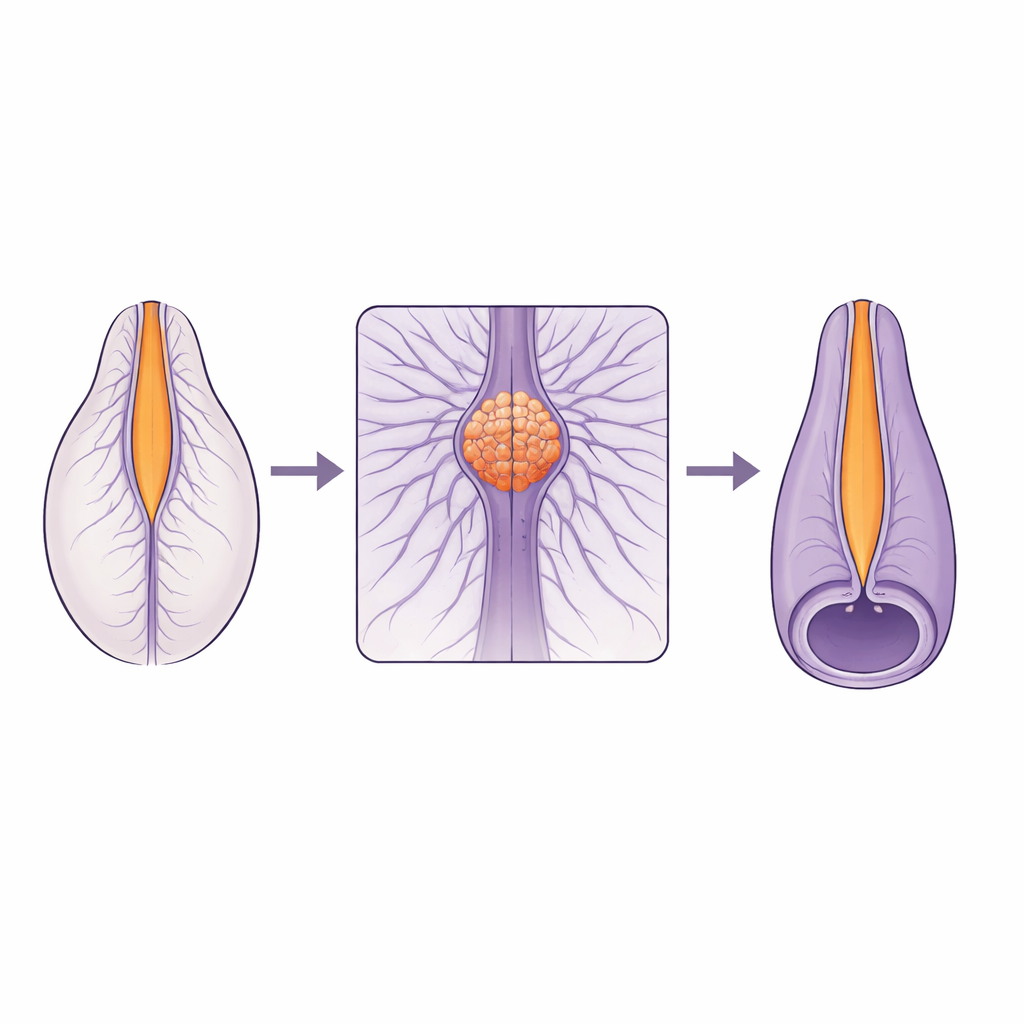
Uma junção delicada na coluna em crescimento
A medula espinhal não se forma de maneira única ao longo de todo o seu comprimento. A região superior surge pelo dobramento e fechamento de um tecido plano, enquanto a parte inferior se origina a partir de uma haste sólida de células que se cavita internamente. Esses dois programas de construção precisam se encontrar e fundir-se suavemente em uma pequena área chamada zona de junção. Muitos defeitos espinhais humanos se concentram perto dessa junção, o que sugere que ela é particularmente frágil. Ainda assim, até agora faltavam aos cientistas vistas ao vivo e de alta resolução necessárias para entender como as células realmente se movem e mudam de forma nessa zona enquanto o tubo se fecha.
Observando células se moverem e mergulharem sob a superfície
Os pesquisadores recorreram a embriões de codorna transgênicos cujas células brilham sob o microscópio, permitindo rastrear centenas de células individuais por horas. Eles descobriram que o tubo neural da junção se forma por meio de dois movimentos coordenados. Primeiro, células das laterais rastejam em direção à linha média, um movimento chamado convergência mediolateral que estreita o tecido. Em segundo lugar, uma faixa de células bem no centro faz algo mais dramático: essas células contraem suas superfícies apicais, depois mergulham abaixo da superfície para o tecido mais profundo, um comportamento conhecido como ingresso. Esse ingresso lembra uma transição epitélio‑mesênquima, na qual células organizadas em folha tornam‑se mais móveis, mas aqui isso ocorre em células que mantêm identidade neural e passam a contribuir principalmente para a medula espinhal em vez de outros tecidos.
Um papel surpreendente para uma proteína de polaridade conhecida
Trabalhos anteriores haviam implicado uma proteína chamada PRICKLE1 nessa região de junção. PRICKLE1 é normalmente conhecida como parte do sistema de polaridade planar celular, que orienta as células lado a lado e ajuda os tecidos a se alongarem. Poder‑se‑ia esperar que remover PRICKLE1 bagunçasse essa polaridade. Em vez disso, quando a equipe reduziu os níveis de PRICKLE1 especificamente na zona de junção, os padrões usuais de polaridade e os longos cabos de actina que guiam a convergência permaneceram em grande parte intactos. O que mudou foi o comportamento das células mediais: elas não conseguiram contrair suas superfícies apicais, não ingressaram adequadamente, e a abertura posterior do tubo neural permaneceu sem fechar, produzindo defeitos do tubo neural na junção nos embriões.
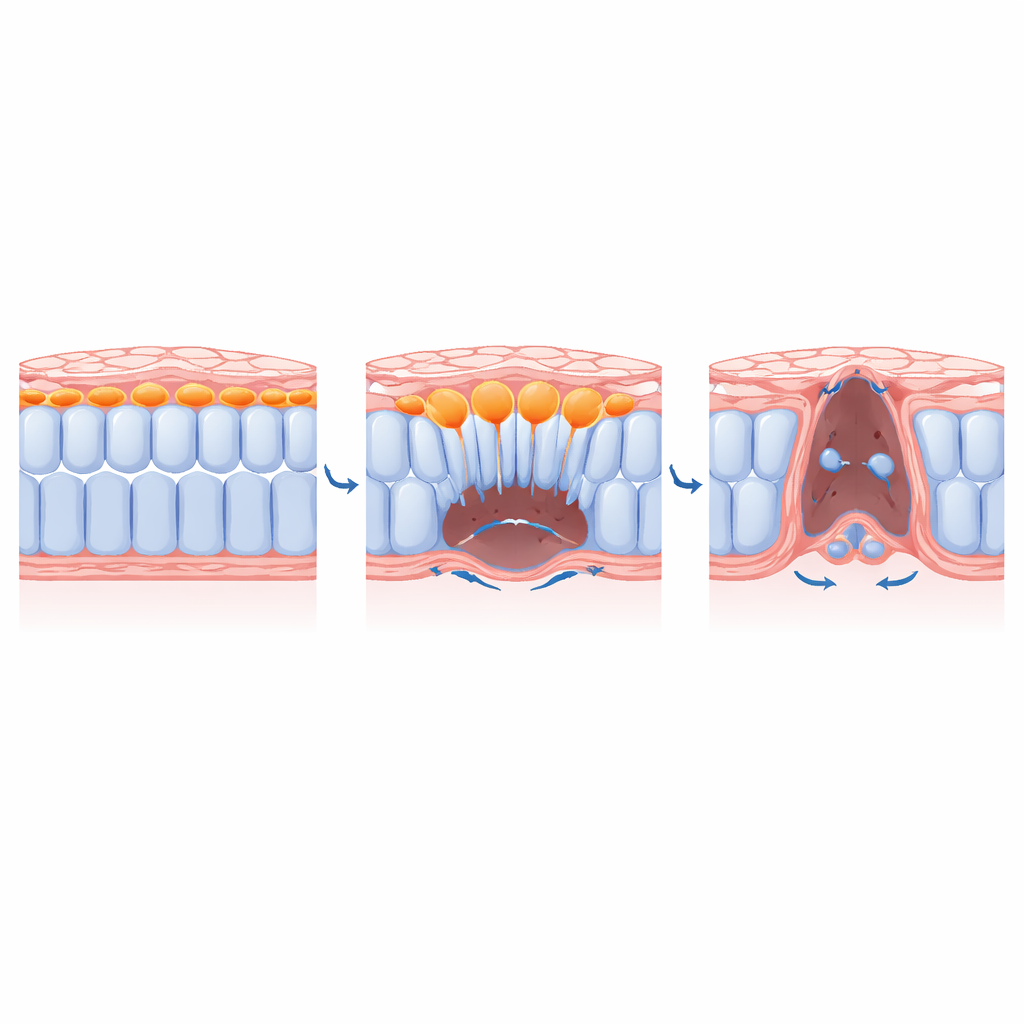
Como as células centrais liberam espaço para as vizinhas
Combinando ferramentas genéticas, fármacos e até inibidores de miosina ativados por luz (o motor que alimenta a contração), a equipe dissecou como o ingresso é controlado. Eles mostraram que reguladores chave da EMT, como o fator de transcrição SLUG, e sinais de fatores de crescimento de fibroblastos são necessários para que as células mediais adotem uma forma protrusiva e migratória e para que degradem a matriz de suporte abaixo delas. Bloquear esses sinais prendeu as células mediais perto da superfície dorsal e impediu que se movessem ventralmente. Crucialmente, quando os pesquisadores desativaram a contração apenas nas células mediais, essas células deixaram de ingressar, e as vizinhas laterais não puderam convergir completamente em direção à linha média. Em outras palavras, o ato de as células centrais mergulharem para dentro limpa fisicamente o espaço que permite que a folha restante se zíper feche.
Por que isso importa para defeitos espinhais humanos
O trabalho revela que PRICKLE1 tem uma função independente da PCP no córtex apical das células mediais: ela promove o acúmulo de actina e miosina contráteis necessários para a constrição apical e o ingresso. Sem essa função, embora os sinais de polaridade lateral persistam, o processo semelhante à EMT central estagna, e o tubo neural falha em fechar na junção. Como mutações humanas em PRICKLE1 são mais frequentemente associadas a disrafias espinhais localizadas — defeitos do tubo neural na junção — esses achados oferecem uma explicação celular concreta. Para um leitor leigo, a mensagem principal é que um pequeno grupo de células deve tanto puxar suas superfícies superiores quanto mergulhar abaixo da superfície no lugar e momento exatos, e que a proteína PRICKLE1 é um interruptor crítico para esse movimento. Quando esse interruptor falha, a união entre a parte superior e inferior da medula não se forma corretamente, ajudando a explicar uma classe específica e séria de defeitos congênitos.
Citação: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Palavras-chave: defeitos do tubo neural, PRICKLE1, transição epitélio‑mesênquima, desenvolvimento embrionário, migração celular