Clear Sky Science · de
Quantitative Live‑Bildgebung zeigt, dass PRICKLE1 die junctionale Neuralrohrmorphogenese unabhängig von planarer Zellpolarität steuert
Wie frühe Nervenbildung unser Gehirn und Rückenmark formt
Bevor ein menschlicher Embryo die Größe eines Reiskorns erreicht, muss ein flaches Zellblatt sich falten und zu einem hohlen Rohr verschließen, das später Gehirn und Rückenmark bildet. Wenn dieser Prozess fehlschlägt, können Neugeborene mit schweren Wirbelsäulenfehlbildungen zur Welt kommen. In dieser Studie wurde modernste Live‑Bildgebung an winzigen Wachtel‑Embryonen eingesetzt, um diese Umgestaltung in Echtzeit zu beobachten. Dabei zeigte sich ein überraschendes Zellverhalten und ein zentrales Steuerprotein, die gemeinsam helfen, eine bestimmte Klasse von Wirbelsäulenproblemen zu verhindern.
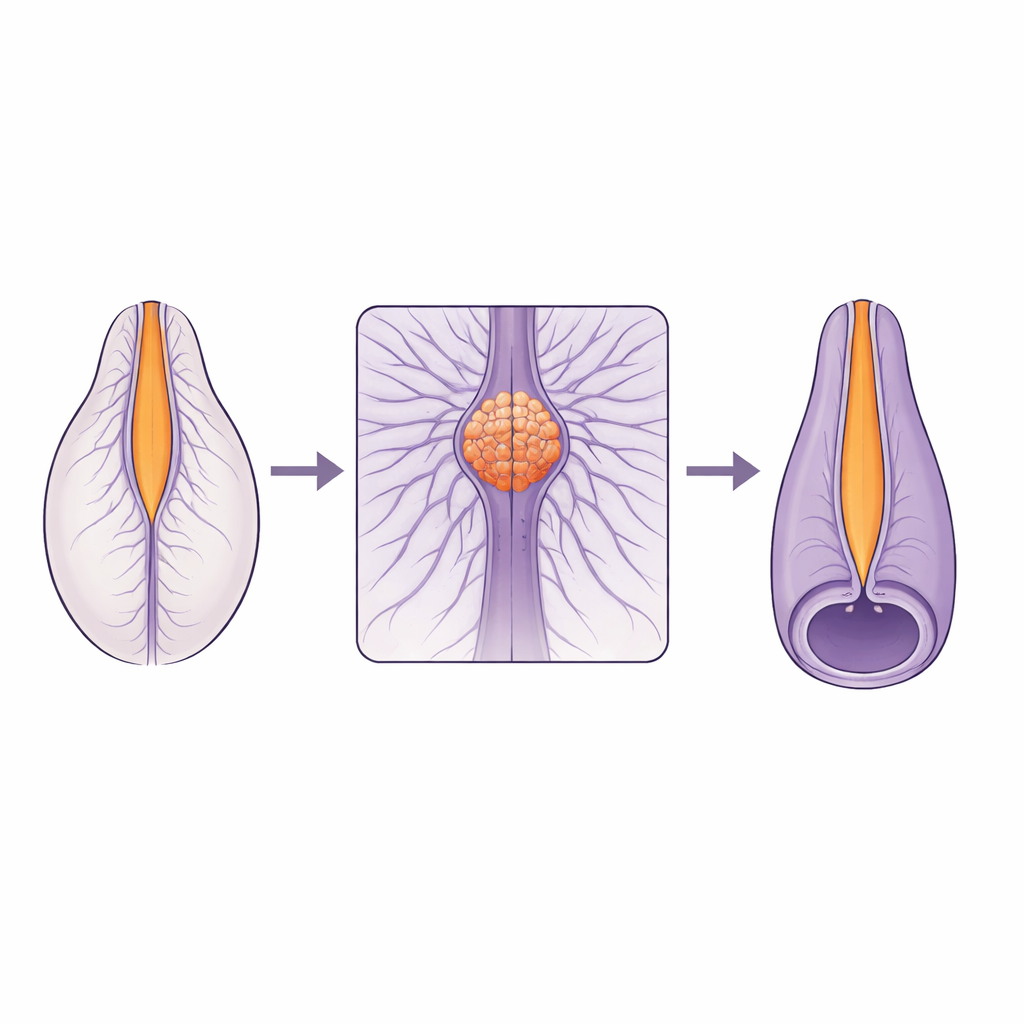
Eine empfindliche Verbindung in der wachsenden Wirbelsäule
Das Rückenmark bildet sich nicht einheitlich entlang seiner Längsachse. Der obere Teil entsteht durch Faltung und Verschluss eines flachen Gewebes, während der untere Teil aus einer festen Zellleiste hervorgeht, die sich von innen aushöhlt. Diese beiden Aufbauprogramme müssen an einer kleinen Region, der sogenannten junctionalen Zone, nahtlos aufeinandertreffen und verschmelzen. Viele menschliche Rückenmarkdefekte treten in der Nähe dieser Verbindung auf, was darauf hindeutet, dass sie besonders anfällig ist. Bislang fehlten jedoch lebende, hochauflösende Aufnahmen, die zeigen, wie sich Zellen in dieser Zone tatsächlich bewegen und ihre Form verändern, während sich das Rohr verschließt.
Zellen beobachten, die sich bewegen und unter die Oberfläche abtauchen
Die Forschenden verwendeten transgene Wachtel‑Embryonen, deren Zellen im Mikroskop leuchten, sodass sie hunderte einzelner Zellen über Stunden verfolgen konnten. Sie stellten fest, dass sich das junctionale Neuralrohr durch zwei koordinierte Bewegungen bildet. Zuerst kriechen Zellen von den Seiten zur Mittellinie, eine Bewegung, die als mediolaterale Konvergenz bezeichnet wird und das Gewebe verengt. Zweitens macht ein Streifen von Zellen genau in der Mitte etwas Dramatischeres: Diese Zellen verkleinern ihre Oberseiten (apikale Flächen) und tauchen dann unter die Oberfläche in tiefere Gewebeschichten ab — ein Verhalten, das als Ingression bekannt ist. Diese Ingression ähnelt einer Epithel‑zu‑Mesenchym‑Transition, bei der geordnete, blattartige Zellen beweglicher werden; hier jedoch behalten die Zellen ihre neuronale Identität und tragen hauptsächlich zum Rückenmark bei, statt zu anderen Geweben zu werden.
Eine überraschende Rolle für ein bekanntes Polaritätsprotein
Frühere Arbeiten hatten ein Protein namens PRICKLE1 in dieser junctionalen Region in Verbindung gebracht. PRICKLE1 ist normalerweise als Teil des Systems der planar‑zell‑Polarität bekannt, das Zellen seitlich ausrichtet und Gewebeverlängerung unterstützt. Man hätte erwarten können, dass das Entfernen von PRICKLE1 diese Polarität durcheinanderbringt. Stattdessen zeigte sich: Wenn das Team PRICKLE1 spezifisch in der junctionalen Zone reduzierte, blieben die üblichen Polaritätsmuster und die langen Actin‑Kabel, die die Konvergenz leiten, größtenteils erhalten. Verändert hatte sich das Verhalten der medialen Zellen: Sie konnten ihre apikalen Flächen nicht verengen, ingressierten nicht korrekt, und der hintere Verschluss des Neuralrohrs blieb offen, was bei den Embryonen zu junctionalen Neuralrohrdefekten führte.
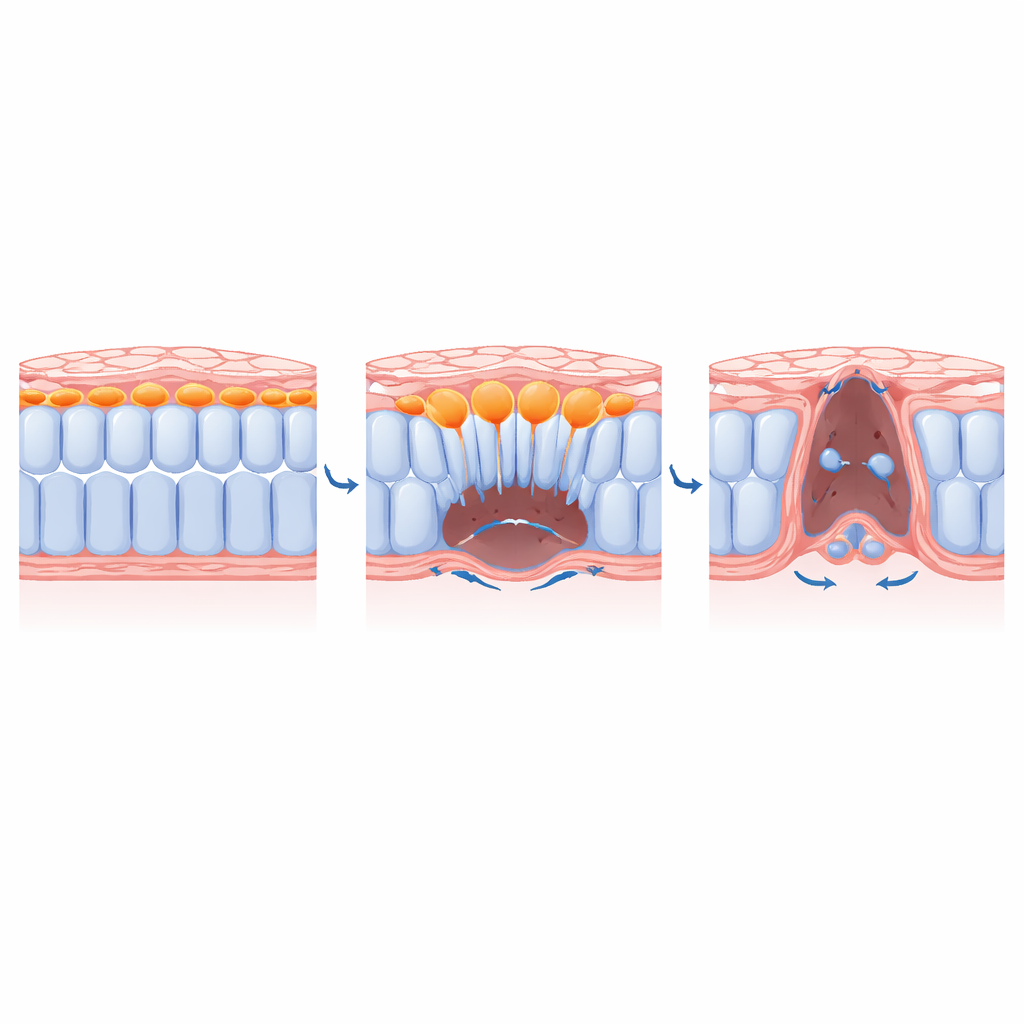
Wie zentrale Zellen Platz für ihre Nachbarn schaffen
Durch die Kombination genetischer Werkzeuge, Wirkstoffe und sogar lichtaktivierbarer Myosin‑Inhibitoren (des Motors, der Kontraktion antreibt) untersuchten die Forschenden, wie Ingression gesteuert wird. Sie zeigten, dass zentrale EMT‑Regulatoren wie der Transkriptionsfaktor SLUG und Signale von Fibroblasten‑Wachstumsfaktoren erforderlich sind, damit mediale Zellen eine protrusive, migrierende Form annehmen und die darunterliegende Stützmatrix abbauen. Das Blockieren dieser Signale fesselte mediale Zellen in der Nähe der dorsalen Oberfläche und verhinderte ihr ventrales Abwandern. Wichtig war: Wenn die Forschenden die Kontraktion nur in den medialen Zellen ausschalteten, ingressierten diese Zellen nicht mehr, und laterale Nachbarn konnten nicht vollständig zur Mittellinie konvergieren. Mit anderen Worten: Das Einwärtstauchen der zentralen Zellen räumt physisch den Raum, der dem verbleibenden Zellblatt ermöglicht, sich wie ein Reißverschluss zu schließen.
Warum das für menschliche Rückenmarksdefekte wichtig ist
Die Studie zeigt, dass PRICKLE1 eine von der PCP getrennte Funktion an der apikalen Cortex‑Region medialer Zellen hat: Es fördert den Aufbau kontraktiler Actin‑ und Myosinstrukturen, die für apikale Kontraktion und Ingression nötig sind. Ohne diese Funktion stockt der zentrale, EMT‑ähnliche Prozess, und das Neuralrohr schließt an der Verbindung nicht, obwohl seitliche Polaritäts‑Hinweise weiterhin bestehen. Da menschliche PRICKLE1‑Mutationen am häufigsten mit lokalisierten spinalen Dysraphien — junctionalen Neuralrohrdefekten — verbunden sind, liefern diese Befunde eine konkrete zelluläre Erklärung. Für eine/n nicht‑Fachleser/in lautet die Kernbotschaft: Eine kleine Zellgruppe muss ihre Oberseiten zusammenziehen und zur richtigen Zeit am richtigen Ort unter die Oberfläche abtauchen, und das Protein PRICKLE1 ist ein entscheidender Schalter für diese Bewegung. Fällt dieser Schalter aus, kann die Verbindung zwischen oberem und unterem Rückenmark nicht richtig entstehen, was erklärt, wie eine spezifische und ernsthafte Klasse von Geburtsfehlern entsteht.
Zitation: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Schlüsselwörter: Neuralrohrdefekte, PRICKLE1, Epithel‑zu‑Mesenchym‑Transition, embryonale Entwicklung, Zellmigration