Clear Sky Science · es
La imagen cuantitativa en vivo revela que PRICKLE1 controla la morfogénesis del tubo neural en la zona de unión independiente de la polaridad celular planar
Cómo la formación temprana del sistema nervioso moldea nuestros cerebros y médula
Antes de que un embrión humano siquiera tenga el tamaño de un grano de arroz, una lámina plana de células debe plegarse y sellarse en un tubo hueco que dará lugar al cerebro y la médula espinal. Cuando este proceso falla, los bebés pueden nacer con graves malformaciones espinales. Este estudio utiliza imágenes en vivo de vanguardia en diminutos embriones de codorniz para observar esta transformación en tiempo real, revelando un comportamiento celular sorprendente y una proteína control clave que, juntas, ayudan a prevenir una clase específica de problemas espinales.
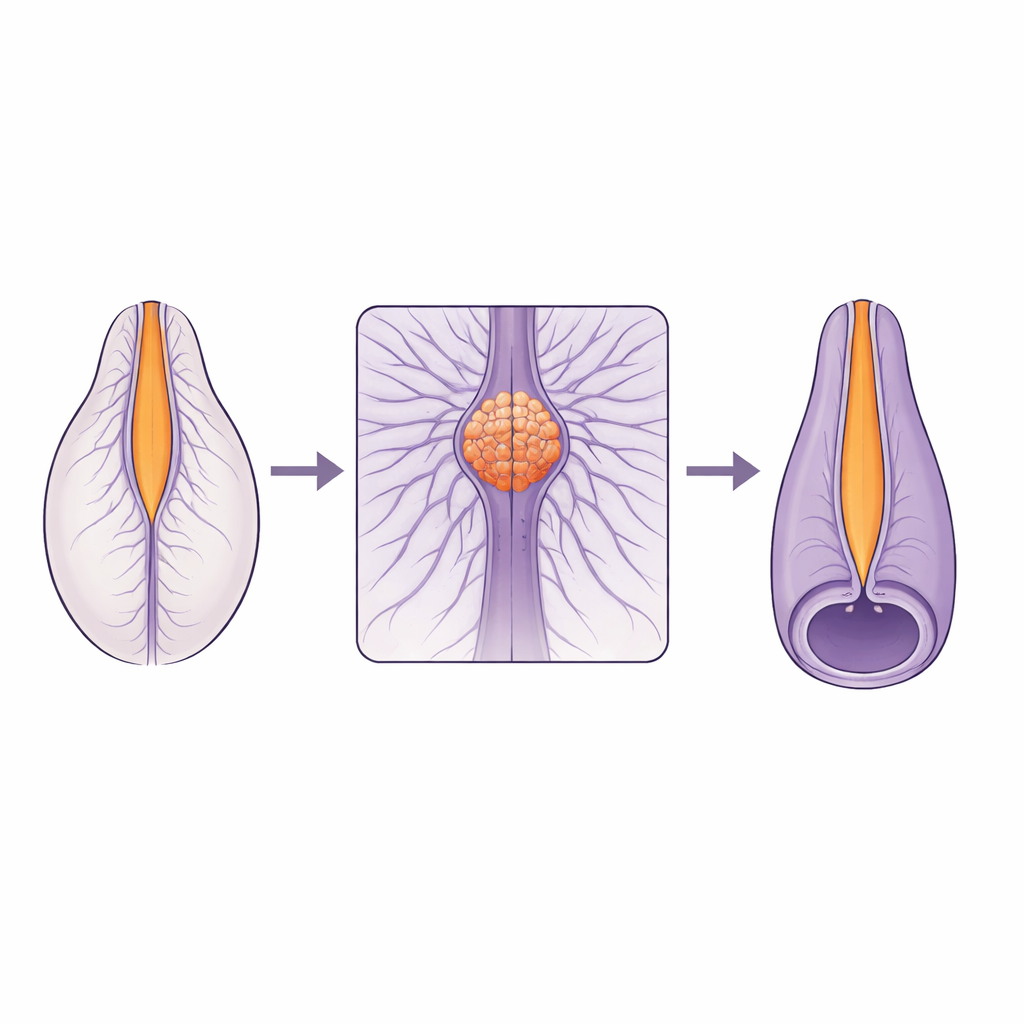
Una unión delicada en la columna en crecimiento
La médula espinal no se forma de la misma manera a lo largo de toda su extensión. La parte superior surge por plegamiento y cierre de un tejido plano, mientras que la parte inferior se forma a partir de una barra sólida de células que se vacía desde su interior. Estos dos programas constructivos deben encontrarse y fusionarse sin fricción en una pequeña área llamada zona de unión. Muchos defectos espinales humanos se concentran cerca de esta unión, lo que sugiere que es especialmente frágil. Sin embargo, hasta ahora, los científicos carecían de las vistas en vivo y de alta resolución necesarias para entender cómo se mueven y cambian de forma las células en esta zona durante el cierre del tubo.
Observando cómo las células se desplazan y se hunden bajo la superficie
Los investigadores recurrieron a embriones de codorniz transgénicos cuyos células brillan bajo el microscopio, lo que les permitió rastrear cientos de células individuales durante horas. Descubrieron que el tubo neural en la zona de unión se forma mediante dos movimientos coordinados. Primero, células de los lados se arrastran hacia la línea media, un movimiento llamado convergencia medio‑lateral que estrecha el tejido. Segundo, una franja de células justo en el centro realiza algo más dramático: estas células contraen sus superficies superiores (apicales) y luego se hunden bajo la superficie hacia tejidos más profundos, un comportamiento conocido como ingresión. Esta ingresión se asemeja a una transición epitelio‑mesénquima, en la que células ordenadas tipo lámina se vuelven más móviles, pero aquí ocurre en células que conservan identidad neural y que contribuyen principalmente a la médula espinal más que a otros tejidos.
Un papel sorprendente para una proteína de polaridad conocida
Trabajos anteriores habían implicado a una proteína llamada PRICKLE1 en esta región de unión. PRICKLE1 se conoce habitualmente como parte del sistema de polaridad celular planar, que orienta a las células lateralmente y ayuda a que los tejidos se alarguen. Podría esperarse que eliminar PRICKLE1 desordenara esa polaridad. En su lugar, cuando el equipo redujo los niveles de PRICKLE1 específicamente en la zona de unión, los patrones habituales de polaridad y los largos cables de actina que guían la convergencia permanecieron en gran medida intactos. Lo que cambió fue el comportamiento de las células mediales: no consiguieron contraer sus superficies apicales, no ingresaron correctamente y la apertura posterior del tubo neural quedó sin cerrar, produciendo defectos del tubo neural en la zona de unión en los embriones.
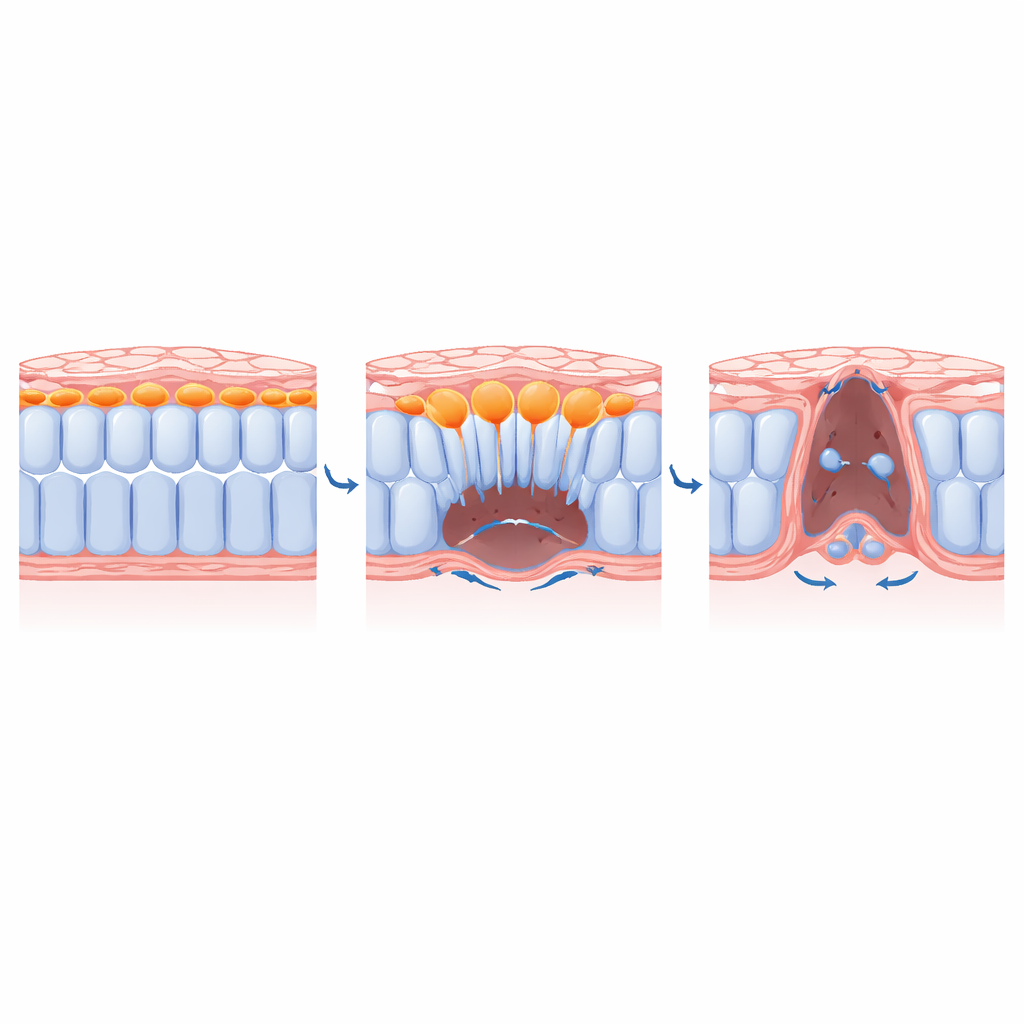
Cómo las células centrales crean espacio para sus vecinas
Combinando herramientas genéticas, fármacos e incluso inhibidores de la miosina activados por luz, el equipo desentrañó cómo se controla la ingresión. Mostraron que reguladores clave de la EMT, como el factor de transcripción SLUG, y señales de factores de crecimiento de fibroblastos son necesarios para que las células mediales adopten una morfología protrusiva y migratoria y para que degraden la matriz de soporte por debajo de ellas. Bloquear estas señales atrapó a las células mediales cerca de la superficie dorsal e impidió que se desplazaran ventralmente. De forma crucial, cuando los investigadores desactivaron la contracción únicamente en las células mediales, esas células dejaron de ingresar y las vecinas laterales no pudieron converger completamente hacia la línea media. En otras palabras, el acto de que las células centrales se hundan hacia el interior despeja físicamente el espacio que permite que la lámina restante se cierre como una cremallera.
Por qué esto importa para los defectos espinales humanos
El trabajo revela que PRICKLE1 tiene una función independiente de la PCP en la corteza apical de las células mediales: promueve la acumulación de actina y miosina contráctil necesaria para la constricción apical y la ingresión. Sin esta función, aunque las señales de polaridad lateral persistan, el proceso tipo EMT central se detiene y el tubo neural no se cierra en la zona de unión. Dado que las mutaciones humanas en PRICKLE1 se asocian con mayor frecuencia a disrafias espinales localizadas —defectos del tubo neural en la zona de unión—, estos hallazgos ofrecen una explicación celular concreta. Para un lector general, la conclusión es que un pequeño grupo de células debe tanto tensar su superficie superior como hundirse bajo la superficie en el lugar y momento adecuados, y que la proteína PRICKLE1 es un interruptor crítico para este movimiento. Cuando ese interruptor falla, la unión entre la porción superior e inferior de la médula no puede formarse correctamente, lo que ayuda a explicar una clase específica y grave de defectos congénitos.
Cita: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Palabras clave: defectos del tubo neural, PRICKLE1, transición epitelio‑mesénquima, desarrollo embrionario, migración celular