Clear Sky Science · nl
Kwantiatieve live‑imaging onthult dat PRICKLE1 junctionele neurale buismorfogenese reguleert onafhankelijk van planare celpolarisatie
Hoe vroege zenuwvorming onze hersenen en ruggengraat vormt
Nog voordat een menselijk embryo zo groot is als een rijstkorrel, moet een vlak vel cellen zich vouwen en sluiten tot een holle buis die later de hersenen en het ruggenmerg wordt. Als dit proces misgaat, kunnen baby’s geboren worden met ernstige wervelafwijkingen. Deze studie gebruikt geavanceerde live‑imaging in piepkleine kwartelembryo’s om deze transformatie in real time te volgen, en onthult een verrassend celgedrag en een belangrijke regelende eiwitfactor die samen helpen een specifieke klasse van ruggenproblemen te voorkomen.
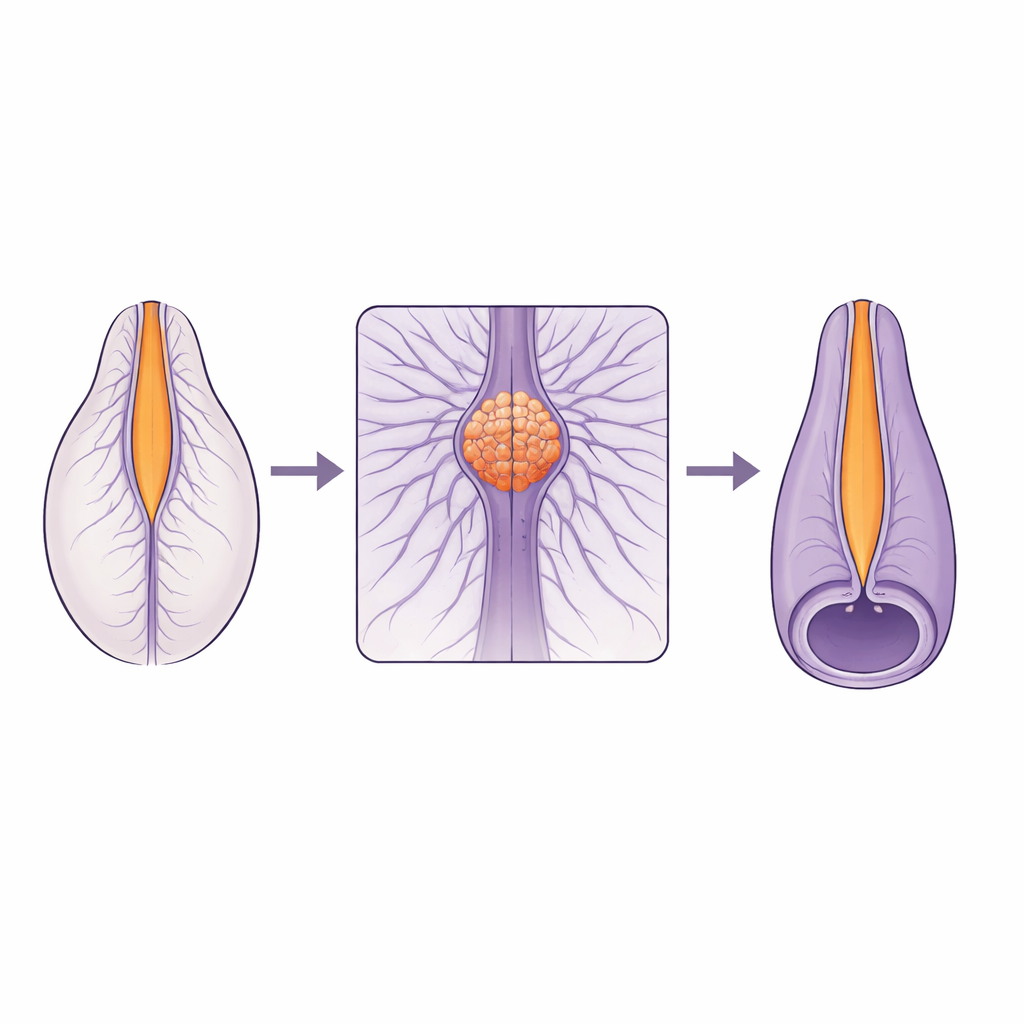
Een kwetsbare verbinding in de groeiende ruggengraat
Het ruggenmerg ontstaat niet op één uniforme manier langs zijn lengte. Het bovenste deel ontstaat door het vouwen en sluiten van een vlak weefsel, terwijl het onderste deel uit een solide staaf cellen ontstaat die van binnenuit een holte vormt. Deze twee bouwprogramma’s moeten soepel samenkomen bij een klein gebied dat de junctionele zone wordt genoemd. Veel menselijke ruggenafwijkingen concentreren zich in de buurt van deze overgang, wat suggereert dat het een bijzonder kwetsbare plek is. Tot nu toe ontbraken echter de live, hoge‑resolutie beelden die nodig zijn om te begrijpen hoe cellen zich in deze zone daadwerkelijk verplaatsen en van vorm veranderen tijdens het sluiten van de buis.
Cellen zien bewegen en onder het oppervlak duiken
De onderzoekers gebruikten transgene kwartelembryo’s waarvan de cellen oplichten onder de microscoop, zodat ze honderden individuele cellen urenlang konden volgen. Ze ontdekten dat de junctionele neurale buis zich vormt via twee gecoördineerde bewegingen. Eerst kruipen cellen van de zijkanten naar de middellijn, een beweging die mediolaterale convergentie wordt genoemd en het weefsel versmalt. Ten tweede doet een strook cellen precies in het midden iets dramatischer: deze cellen verkleinen hun bovenkant (apicale) oppervlak en zakken vervolgens onder het oppervlak in dieper weefsel, een gedrag dat ingression wordt genoemd. Deze ingression lijkt op een epithelium‑naar‑mesenchymale transitie, waarbij ordelijke vel‑achtige cellen vrijer bewegend worden, maar hier gebeurt het in cellen die hun neurale identiteit behouden en voornamelijk bijdragen aan het ruggenmerg in plaats van aan andere weefsels.
Een onverwachte rol voor een bekend polariteitseiwit
Eerder werk had een rol voor het eiwit PRICKLE1 in deze junctionele regio gesuggereerd. PRICKLE1 is normaal gesproken bekend als onderdeel van het planare celpolariteitssysteem, dat cellen zijwaarts oriënteert en weefsels helpt uitrekken. Men zou verwachten dat het verwijderen van PRICKLE1 deze polariteit zou verstoren. In plaats daarvan, toen het team PRICKLE1‑niveaus specifiek in de junctionele zone verminderde, bleven de gebruikelijke polariteitspatronen en lange actinekabels die convergentie sturen grotendeels intact. Wat veranderde, was het gedrag van de mediale cellen: ze slaagden er niet in hun apicale oppervlakken te vernauwen, ingression vond niet goed plaats, en de posterieure opening van de neurale buis bleef ongesloten, wat in de embryo’s tot junctionele neurale buisdefecten leidde.
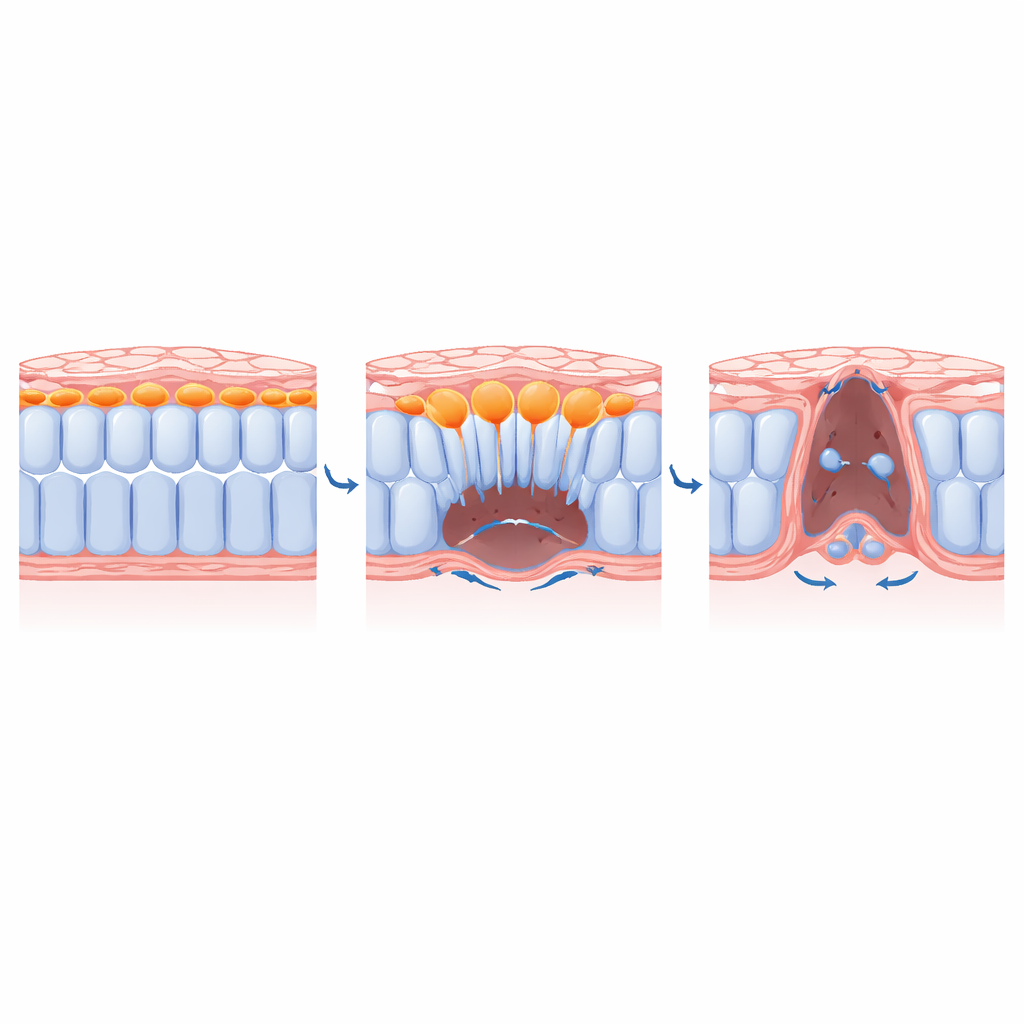
Hoe centrale cellen ruimte maken voor hun buren
Door genetische instrumenten, medicijnen en zelfs licht‑geactiveerde remmers van myosine (de motor die contractie aandrijft) te combineren, ontleedde het team hoe ingression wordt gecontroleerd. Ze toonden aan dat sleutelregulatoren van EMT, zoals de transcriptiefactor SLUG, en signalen van fibroblastgroeifactoren nodig zijn zodat mediale cellen een uitstulpende, migrerende vorm aannemen en de ondersteunende matrix onder hen afbreken. Het blokkeren van deze signalen hield de mediale cellen bij het dorsale oppervlak gevangen en verhinderde dat ze ventraal bewogen. Cruciaal was dat, wanneer de onderzoekers contractie alleen in de mediale cellen uitschakelden, die cellen niet langer ingression uitvoerden en zijdelingse buren niet volledig naar de middellijn konden convergeren. Met andere woorden: de daad van centrale cellen die naar binnen duiken maakt fysiek ruimte vrij waardoor het resterende vel dicht kan ritsen.
Waarom dit belangrijk is voor menselijke rugafwijkingen
Het werk laat zien dat PRICKLE1 een PCP‑onafhankelijke functie heeft aan de apicale cortex van mediale cellen: het bevordert de opbouw van contractiel actine en myosine die nodig is voor apicale vernauwing en ingression. Zonder deze functie stokt het centrale EMT‑achtige proces, en ondanks het voortbestaan van zijwaartse polariteitscue’s sluit de neurale buis bij de junction niet. Omdat menselijke mutaties in PRICKLE1 het vaakst worden geassocieerd met gelokaliseerde spinale dysrafismen — junctionele neurale buisdefecten — bieden deze bevindingen een concrete cellulaire verklaring. Voor een niet‑specialistische lezer is de kernboodschap dat een klein groepje cellen hun toppen zowel strak moet aanspannen als op precies het juiste moment en de juiste plaats onder het oppervlak moet duiken, en dat het eiwit PRICKLE1 een cruciale schakel is voor deze beweging. Faalt die schakel, dan kan de verbinding tussen bovenste en onderste ruggenmerg niet goed vormen, wat helpt verklaren waarom deze specifieke en ernstige klasse van aangeboren afwijkingen optreedt.
Bronvermelding: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Trefwoorden: aangeboren neurale buisafwijkingen, PRICKLE1, epitheel‑naar‑mesenchymale transitie, embryonale ontwikkeling, celmigratie