Clear Sky Science · it
Imaging quantitativo in vivo rivela che PRICKLE1 controlla la morfogenesi della giunzione del tubo neurale indipendentemente dalla Polarità Cellulare Planare
Come la formazione precoce del sistema nervoso modella cervello e midollo
Prima ancora che un embrione umano raggiunga la dimensione di un granello di riso, un foglio piatto di cellule deve piegarsi e sigillarsi in un tubo cavo che diventerà cervello e midollo spinale. Quando questo processo fallisce, i neonati possono nascere con gravi malformazioni spinali. Questo studio usa imaging in vivo all’avanguardia in minuscoli embrioni di quaglia per osservare questa trasformazione in tempo reale, rivelando un comportamento cellulare sorprendente e una proteina di controllo chiave che insieme aiutano a prevenire una specifica classe di problemi spinali.
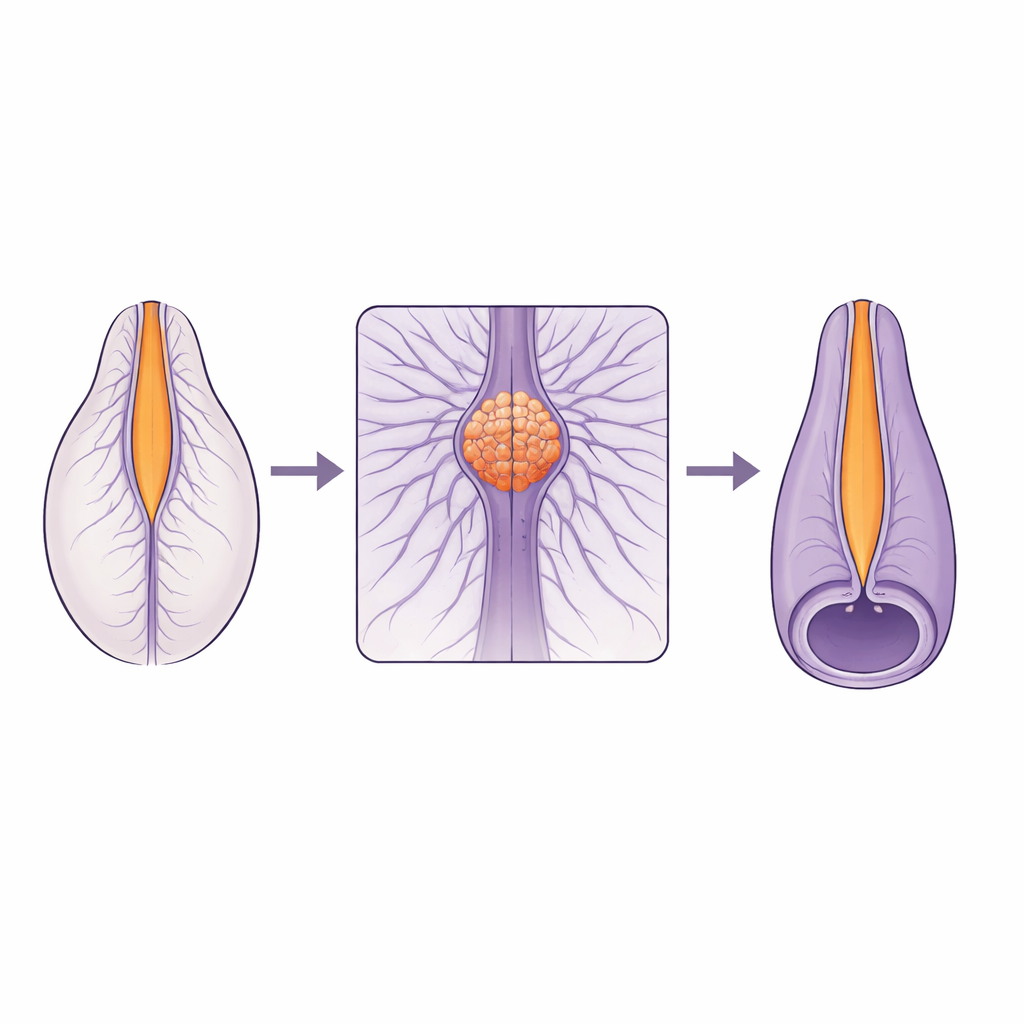
Un’unione delicata nella colonna vertebrale in crescita
Il midollo spinale non si forma nello stesso modo lungo tutta la sua lunghezza. La parte superiore nasce dalla piegatura e chiusura di un tessuto piatto, mentre la parte inferiore si sviluppa a partire da una barra solida di cellule che si svuota dall’interno. Questi due programmi di costruzione devono incontrarsi e fondersi senza soluzione di continuità in una piccola area chiamata zona di giunzione. Molti difetti spinali umani si concentrano vicino a questa giunzione, il che suggerisce che sia particolarmente vulnerabile. Tuttavia fino ad ora mancavano viste in vivo ad alta risoluzione necessarie per capire come le cellule si muovano e cambino forma in questa zona durante la chiusura del tubo.
Osservare le cellule muoversi e tuffarsi sotto la superficie
I ricercatori si sono rivolti a embrioni di quaglia transgenici le cui cellule brillano al microscopio, permettendo di seguire centinaia di singole cellule per ore. Hanno scoperto che il tubo neurale di giunzione si forma attraverso due movimenti coordinati. Innanzitutto, cellule dai lati strisciano verso la linea mediana, un movimento chiamato convergenza medio‑laterale che restringe il tessuto. In secondo luogo, una striscia di cellule proprio al centro compie qualcosa di più drammatico: queste cellule riducono la loro superficie apicale, quindi si immergono sotto la superficie in tessuto più profondo, un comportamento noto come ingression. Questa ingressione assomiglia a una transizione epitelio‑mesenchimale, in cui cellule ordinate a foglio diventano più mobili, ma qui avviene in cellule che mantengono l’identità neurale e contribuiscono principalmente al midollo spinale piuttosto che ad altri tessuti.
Un ruolo sorprendente per una nota proteina della polarità
Lavori precedenti avevano implicato una proteina chiamata PRICKLE1 in questa regione di giunzione. PRICKLE1 è solitamente conosciuta come parte del sistema della polarità cellulare planare, che orienta le cellule lateralmente e aiuta l’allungamento dei tessuti. Si potrebbe immaginare che rimuovere PRICKLE1 scombussoli questa polarità. Invece, quando il team ha ridotto i livelli di PRICKLE1 specificamente nella zona di giunzione, i modelli di polarità abituali e i lunghi fasci di actina che guidano la convergenza sono rimasti per lo più intatti. Ciò che è cambiato è stato il comportamento delle cellule mediali: non sono riuscite a restringere la loro superficie apicale, non hanno inglobato correttamente e l’apertura posteriore del tubo neurale è rimasta non chiusa, producendo difetti del tubo neurale di giunzione negli embrioni.
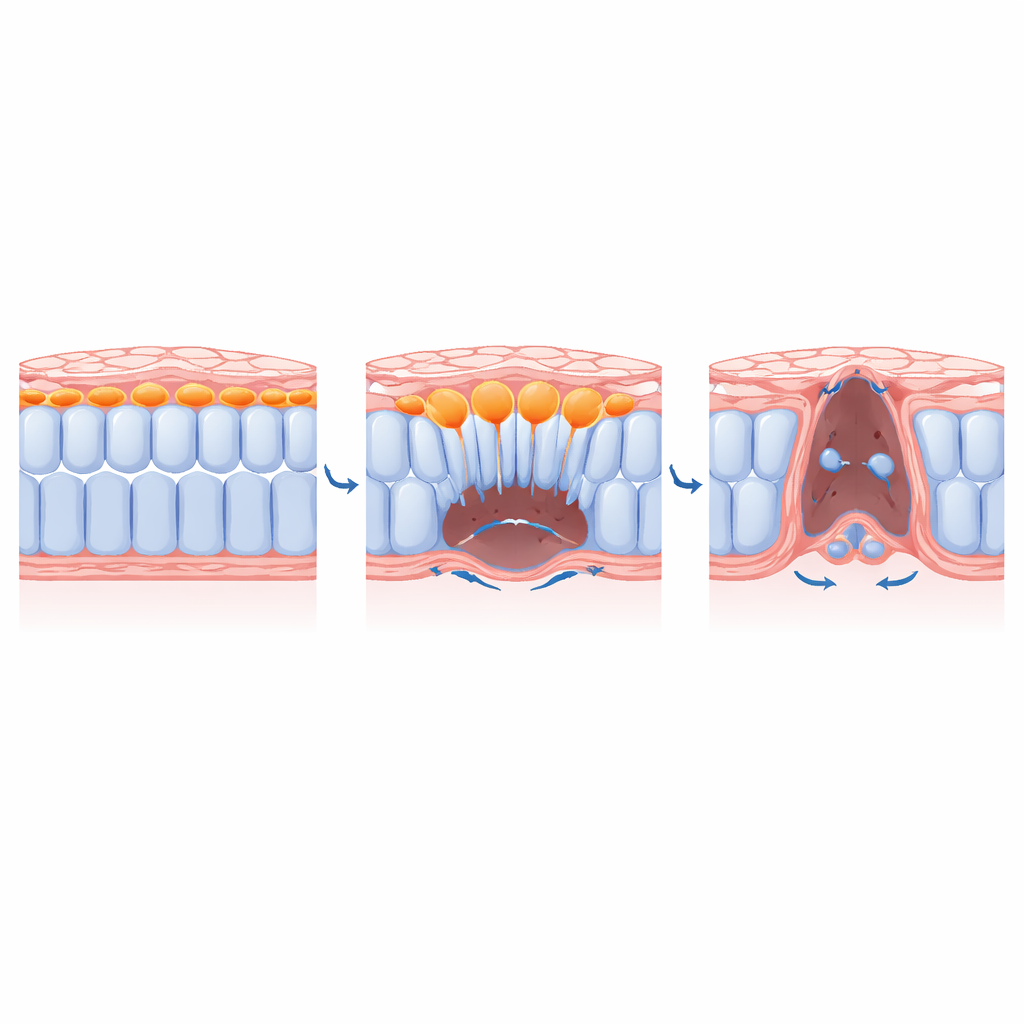
Come le cellule centrali creano spazio per i loro vicini
Combinando strumenti genetici, farmaci e persino inibitori della miosina attivabili con la luce, il team ha analizzato come è regolata l’ingression. Hanno mostrato che regolatori chiave dell’EMT come il fattore di trascrizione SLUG e segnali dai fattori di crescita dei fibroblasti sono necessari perché le cellule mediali adottino una forma protrusiva e migratoria e degradino la matrice di supporto sottostante. Bloccare questi segnali intrappolava le cellule mediali vicino alla superficie dorsale e impediva loro di spostarsi ventralmente. Crucialmente, quando i ricercatori hanno disabilitato la contrazione solo nelle cellule mediali, quelle cellule non hanno più inglobato e i vicini laterali non sono riusciti a convergere completamente verso la linea mediana. In altre parole, l’atto delle cellule centrali che si tuffano verso l’interno libera fisicamente lo spazio che permette al resto del foglio di chiudersi a cerniera.
Perché questo è importante per i difetti spinali umani
Il lavoro rivela che PRICKLE1 ha una funzione indipendente dalla PCP nella corteccia apicale delle cellule mediali: favorisce l’accumulo di actina contrattile e miosina necessario per il restringimento apicale e l’ingression. Senza questa funzione, anche se i segnali di polarità laterale‑laterale persistono, il processo centrale simile all’EMT si blocca e il tubo neurale non riesce a chiudersi nella giunzione. Poiché le mutazioni umane in PRICKLE1 sono spesso associate a disrafismi spinali localizzati — difetti del tubo neurale di giunzione — questi risultati offrono una spiegazione cellulare concreta. Per il lettore non specialistico, il messaggio è che un piccolo gruppo di cellule deve sia tirare stretta la loro superficie apicale sia immergersi sotto la superficie nel posto e nel momento giusti, e che la proteina PRICKLE1 è un interruttore critico per questo movimento. Quando quell’interruttore fallisce, la giunzione tra midollo superiore e inferiore non si forma correttamente, contribuendo a spiegare una specifica e grave categoria di difetti congeniti.
Citazione: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Parole chiave: difetti del tubo neurale, PRICKLE1, transizione epitelio‑mesenchimale, sviluppo embrionale, migrazione cellulare